-
近年来,锑的污染问题日益严重,许多工业过程(如半导体、阻燃剂、合金、催化剂、化工产品等)的生产会向环境中大量的引入锑[1-2],矿山尾矿也是锑污染的主要来源地之一。我国拥有丰富的锑资源,大规模开采的同时也遗留下来大量的废弃尾矿,尾矿中的Sb与Sb化合物随着雨水,地表水浸出,使得矿山排水中含有高浓度的Sb,并通过不断的迁移转化或累积对周围环境和生物造成严重的危害[3]。因此,如何有效地处理含Sb废水一直以来都是各领域所关注的难题。
Sb在水体中常以Sb(Ⅲ)和Sb(Ⅴ)形式存在,其可在不同的pH条件下表现出不同的存在形式[4]。与常规重金属离子不同,Sb在高pH的条件下有着较高的迁移率[5],这一特性使Sb很难通过传统的方法(投加石灰石、白云石)被有效去除。为了解决这一问题,研究人员提出了许多处理锑污染的方法,包括混凝沉淀法[6-7]、膜分离法[8]、微生物法[9]、电化学法[10-11]、离子交换法[12]、吸附法[13-14]等。但是这些方法仍存在操作复杂、工艺成本高、处理浓度低等缺点,无法很好地兼顾对去除效果和二次污染的控制,难以在含锑酸性矿山废水处理中得到广泛推广与应用。据报道[11],Sb(Ⅲ)的毒性的比Sb(Ⅴ)高出10倍以上,因此,将Sb(Ⅲ)转化为Sb(Ⅴ)是实现Sb(Ⅲ)污染控制的一个可行的途径。曹岛等[15]通过H2O2对铜电解液中的Sb(Ⅲ)进行氧化,脱除率可达到68.2%。KONG等[16-17]对黄铁矿(FeS2)在自然酸性环境下发生Fenton反应并有效氧化水体中Sb(Ⅲ)进行了一系列的机理分析与研究。LIU等[11]以FeOCl改性碳纳米管(CNT)滤波器作为功能性阴极,通过流动式电芬顿体系高效地处理300 mL浓度为1 000 μg·L−1的含锑废水,取得了较好的效果。这些研究为我们处理此类废水提供新的方向:通过强氧化性物质(·OH),将Sb(Ⅲ)高效地转化为稳定的高价态,从而降低水体中的毒性,这已成为一种治理酸性矿山废水中Sb(Ⅲ)可行的办法。
本研究设计了一种新型的电芬顿反应器,以酸性矿山废水中的Sb(Ⅲ)为处理目标,考察了各关键参数对去除率的影响,系统地评价了该反应器较传统处理技术的优越性,探讨了其反应机理,并对该反应器在实际废水处理中的应用效果进行了评估,本研究可为含Sb(Ⅲ)酸性矿山废水的处理提供新的解决思路与依据。
全文HTML
-
本研究以湖南某地锑矿浮选废水为例,废水水质:pH=2.4、98.2~102.26 mg·L−1 Sb(Ⅲ)、0.42 mg·L−1 As、0.55 mg·L−1 Fe、0.24 mg·L−1 Mn、0.08 mg·L−1 Cr、0.16 mg·L−1 Zn、30 mg·L−1 COD、3.98 g·L−1
$ {\rm{S}}{{\rm{O}}_4^{2 - }} $ 、51 mg·L−1$ {\rm{C}}{{\rm{O}}_3^{2 - }}$ 、70 mg·L−1$ {\rm{P}}{{\rm{O}}_4^{3 - }}$ 。通过配制模拟含锑废水进行一系列探究。所用试剂(均为分析纯)为酒石酸锑钾(C8H4K2O12Sb2·3H2O,国药)、氯化钾(KCl,国药)、水杨酸(salicylic acid,国药)、苯醌(benzoquinone,国药)、硫酸(H2SO4,国药)、氢氧化钠(NaOH,国药)。实验中所用水均为超纯水(UPH,优普,18.25 MΩ·cm)。 -
电芬顿反应在有机玻璃(PMMA)材质的圆柱形反应器(D=100 mm, H=150 mm)中进行,实验装置如图1所示。装置阴极由Ti网制成(D=40 mm,H=50 mm),并将活性炭纤维毡(ACF)覆于表面,阳极为Fe电极(10 cm×5 cm),正负极分别通过不锈钢电极夹连接至直流电源(MESTEK DP305)上,通过调节阴极最外端侧到阳极板的距离来控制板间距。配制1 L含100 mg·L−1 Sb(Ⅲ)模拟废水,将阴极浸泡在废水中数小时,直至饱和后取出再用。通入电流开始反应后,通过控制变量法,探究关键参数对去除率的影响,每组实验设置3组平行,在不同的时间段内,提取溶液转移至10 mL取样管中并冷藏。
-
反应中电流的调控通过直流稳压电源(MASTEK DP305)完成,溶液pH的测定通过pH计(METTLER S220)测定,采用火焰原子吸收法(AA-3800,上海)检测Sb(Ⅲ)和Sb(Ⅴ)的浓度变化。
1.1. 废水与试剂
1.2. 实验装置与步骤
1.3. 样品分析
-
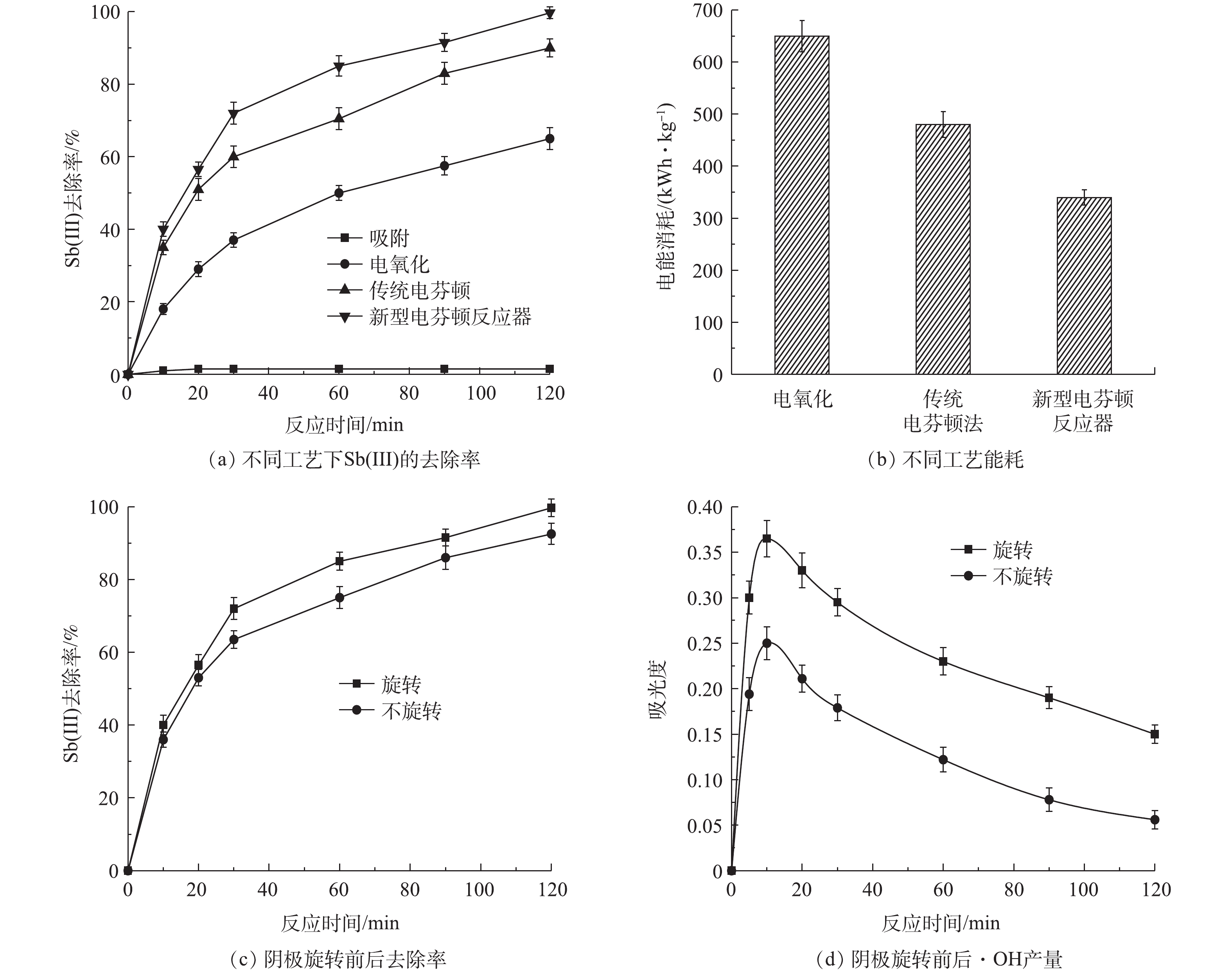
为反映新型电芬顿反应器的效果和优势,对比了不同工艺对Sb(Ⅲ)的处理效果,即吸附、电氧化、传统电芬顿法(10 cm×5 cm ACF作为阴极)的处理效果(见图2)。由图2(a)可知:在吸附条件下,Sb(Ⅲ)的浓度几乎没有变化;在电氧化条件下,Sb(Ⅲ)的去除率约为58%;传统电芬顿法对Sb(Ⅲ)的去除率可以达到90%;而新型电芬顿反应器中Sb(Ⅲ)的去除率可以达到99.7%左右,并且拥有更高的反应速率。此外,处理Sb(Ⅲ)的能耗如图2(b)所示,新型反应器的能耗远小于前二者。这一结果表明,新型电芬顿反应器能够更高效的氧化Sb(Ⅲ),处理效果较其他工艺更好,与其他高级氧化法相比,处理中主要的消耗为电能,这极大地降低了处理成本。
实验考察了阴极旋转在处理过程中起到的作用,结果如图2(c)所示。可以看出,旋转时Sb(Ⅲ)的去除率明显高于未旋转条件下的去除率。以一定量的水杨酸溶液作为羟自由基捕获剂,分别在波长510 nm下对2种条件的电芬顿反应中产生的2,3-二羟基苯甲酸、2,5-二羟基苯甲酸进行检测[18]。可以看出,在旋转条件下,·OH的生成量高于后者(图2(d))。由此可以合理地推测,阴极旋转时可以起到搅拌的作用,同时增强了溶液中的传质速率[19],促进了·OH的产生。此外,通过旋转阴极,使得溶液中的铁絮体沉淀难以附着在ACF表面,使ACF上能够保留更多产生·OH的活性点位[20],进而提升了电芬顿体系的氧化能力。
-
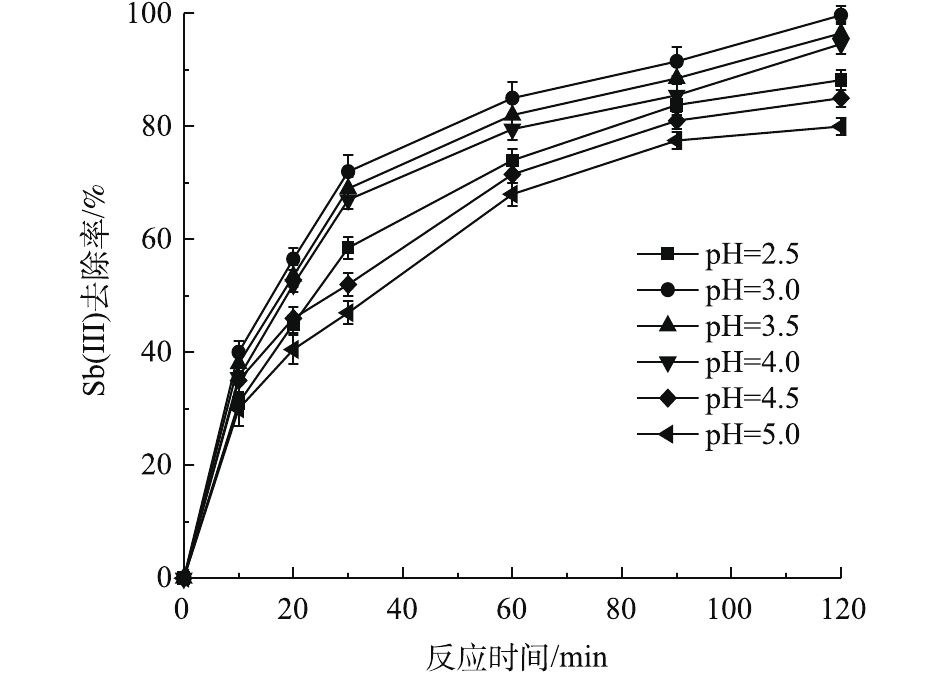
实验考察了初始pH对电芬顿反应的效率的影响。当pH为2.5~5时,pH对废水中Sb(Ⅲ)的去除率的影响结果如图3所示。可以看出:当pH=3时,去除率达到最高,当pH为3.5和4时,去除率稍逊于前者,但仍能保持相当的去除率;但当pH>4时,Sb(Ⅲ)的去除率下降。这是由于:在pH偏低时,H+会与H2O2竞争,阻碍·OH的积累(式(1)),此外,H+还会消耗溶解氧形成H2O[21-22],反应见式(2);而较高的pH条件下,Fe(Ⅱ)易发生水解反应(式(3)),这不利于Fe(Ⅱ)/Fe(Ⅲ)的电化学转化,从而影响了·OH的产生,此外,较高的pH条件同样会抑制H2O2的形成[23-24],反应见式(4)。上述结果表明,在含锑矿山废水呈酸性条件下,该工艺具有较宽的pH适用范围,这可在一定程度上节约成本,不需要花费额外的费用对废水pH进行调节。
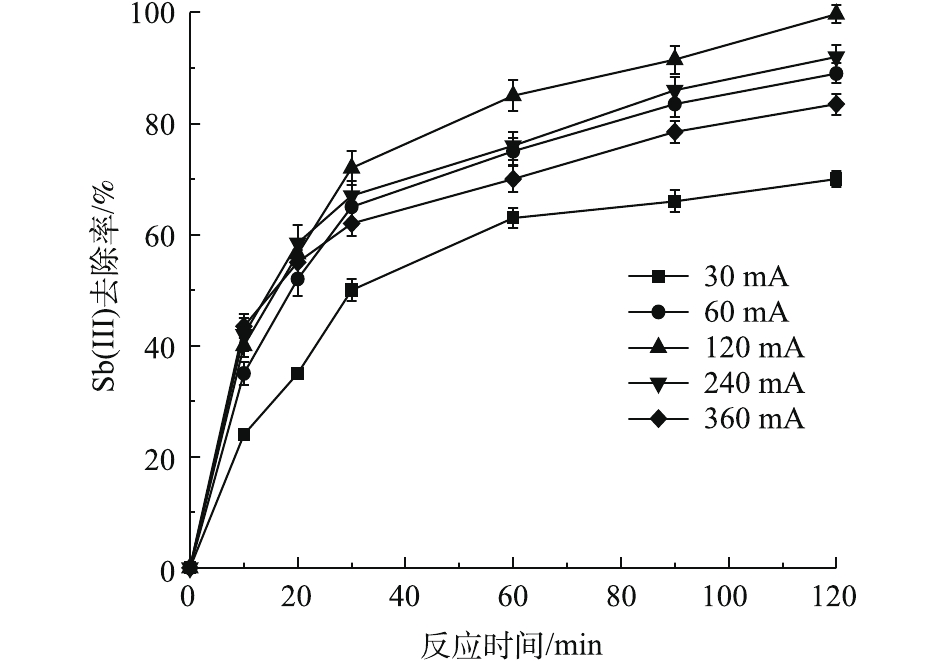
由图4可知,随着初始电流强度(30~360 mA)的上升,Sb(Ⅲ)的去除率呈现先增加后减小的变化趋势。当电流强度为120 mA时(电压为3 V、电流密度为1.91 mA·cm−1),去除率达到99.7%;当施加的电流强度分别增大至240 mA和360 mA时,Sb(Ⅲ)去除率下降(分别为92%和83.5%)。这是由于电芬顿体系的反应速度随着电流强度的上升而上升,但当电流强度过高时,会使电极析氢副反应加剧(式(5)),电流利用效率降低,同时抑制了H2O2在阴极的生成[25-26]。因此,选择电流强度为120 mA,能够最大程度地发挥新型电芬顿反应器的功效。
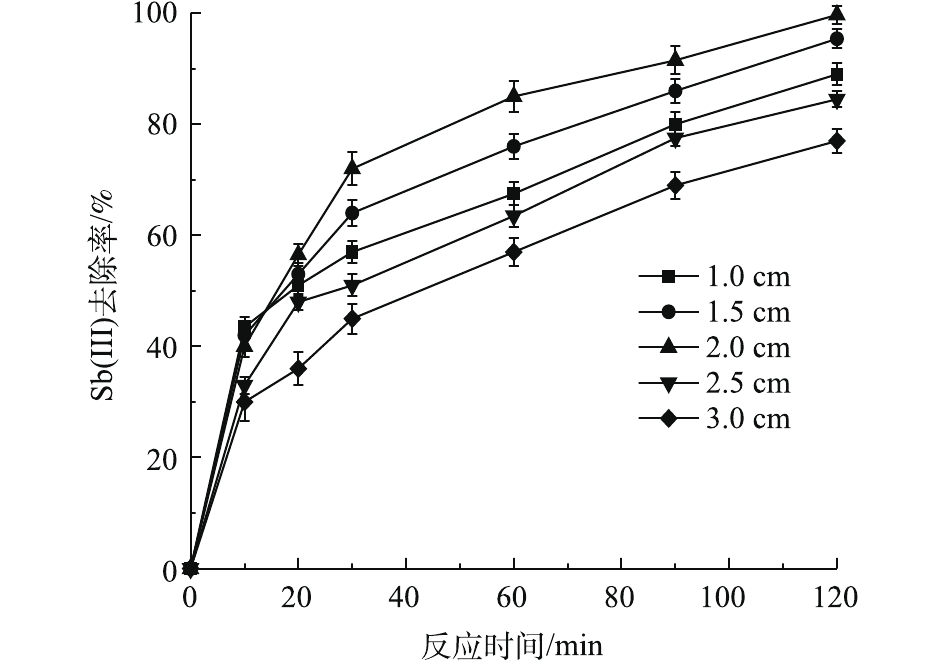
板间距是决定电芬顿处理效率的重要因素之一。本研究考察了板间距在1~3 cm时对Sb(Ⅲ)的去除率的影响情况,结果如图5所示。由图5可知,当板间距为2 cm时,能够达到对Sb(Ⅲ)最佳去除率。这主要是因为:当板间距过近时,阴阳极上的反应会互相干扰,如Fe(Ⅱ)容易被氧化为Fe(Ⅲ) (式(6)),抑制了Fenton反应的效率,影响·OH的生成[27],此外,被氧化的Sb(Ⅴ)会在阴极被还原为Sb(Ⅲ) (式(7)),这使得去除效果难以达到预期目标。板间距距离较远同样不利于提升处理效率,较远的距离会使极板间电阻增大,阻碍了Fe(Ⅲ)向阴极表面的转移再生[28-29],同时,较远的板间距意味着更大的能耗。因此,最佳板间距确定为2 cm。
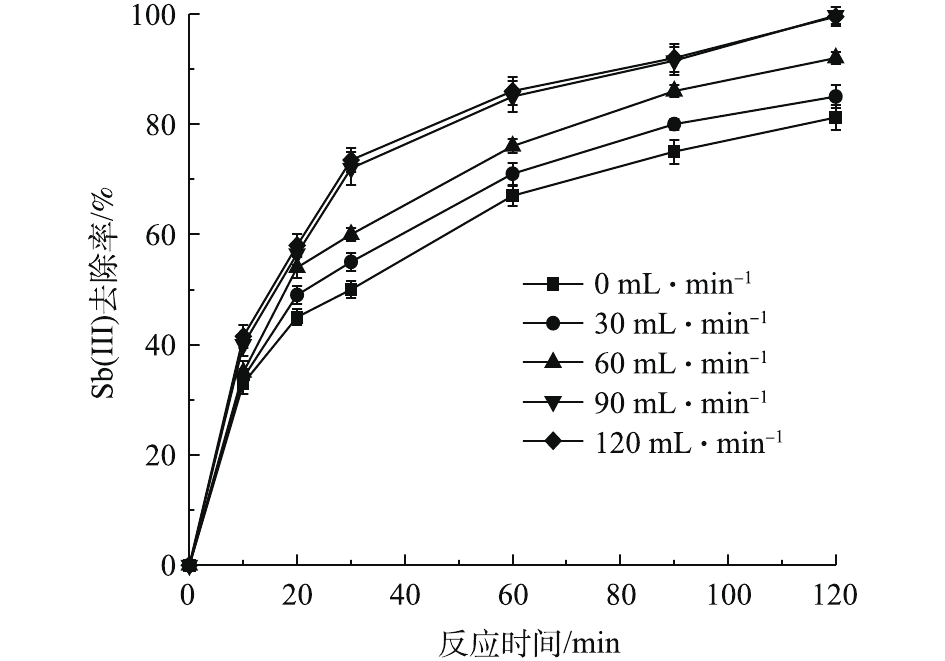
在电芬顿反应中,曝气速率能够通过影响H2O2的生成效率进而影响整体体系的反应速率[30]。图6反映了不同曝气条件下的Sb(Ⅲ)去除率对比结果。可以看出,在曝气条件下的Sb(Ⅲ)去除率明显高于未曝气条件下的去除率。当曝气速率达到90 mL·min−1时,Sb(Ⅲ)去除率约为未曝气状态的1.3倍,这是由于提升曝气速率能够增加溶液中的溶解氧,有利于H2O2的生成[31-33](式(8))。当曝气速率高于90 mL·min−1时,Sb(Ⅲ)的去除率没有进一步提高,这说明90 mL·min−1的曝气速率可以提供充足的溶解氧。因此,最佳曝气速率选择为90 mL·min−1。
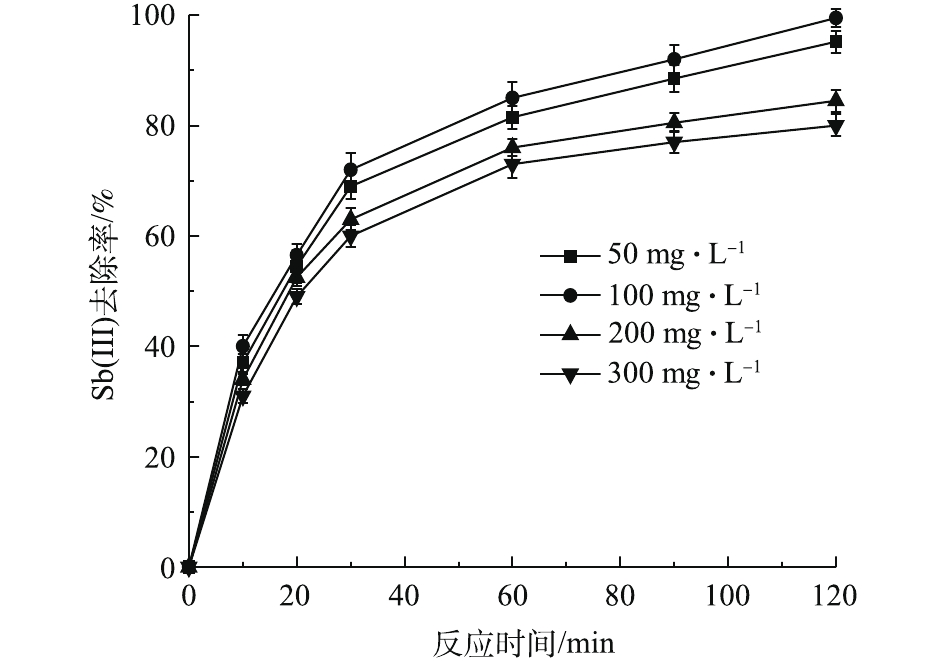
电解质能够有效加强溶液中的导电性,提高处理效率。本研究考察了不同电解质浓度在含Sb(Ⅲ)实际废水处理中的去除效果,结果如图7所示。通过增加KCl的浓度,观察到去除率有所提高,当电解质浓度100 mg·L−1时,去除率达到99.7%。这是由于KCl作为电解质时,随着电流效率的提升,·OH的生成效率随之提高。此外,KCl作为电解质时,能够消除其他物质作为电解质时的不利影响,如
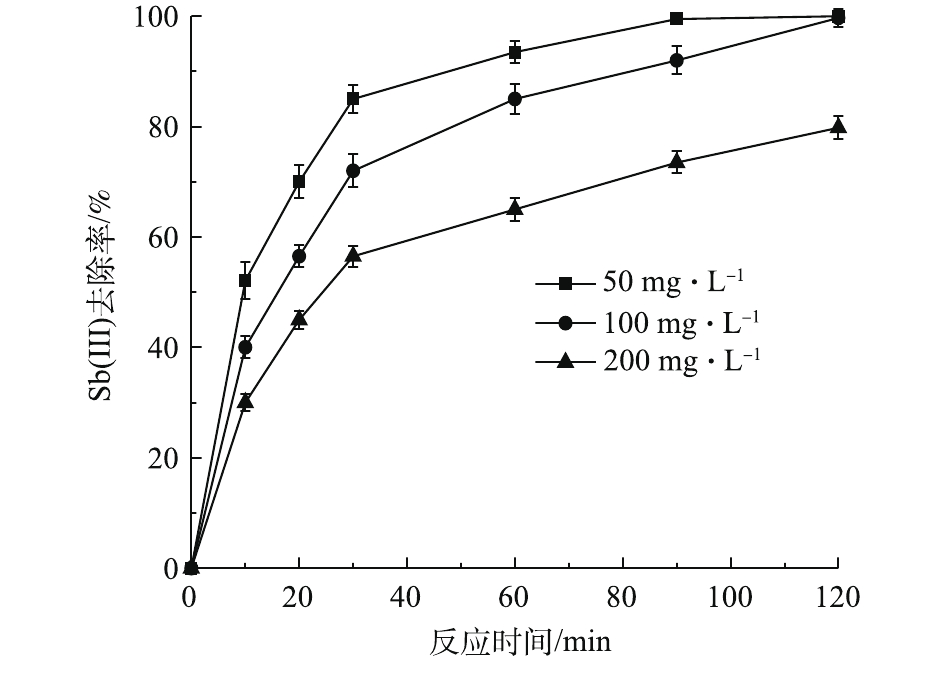
$ {\rm{S}}{{\rm{O}}_4^{2 - }} $ 、$ {\rm{C}}{{\rm{O}}_3^{2 - }}$ 的存在可能会与溶液中的Ca2+等反应生成沉淀,导致电极钝化,所需能耗上升[27]。溶液中Cl−的存在可能会在电流催化下产生具有氧化性的次氯酸(HOCl),促进了Sb(Ⅲ)/Sb(Ⅴ)的转化。但这并不意味着电解质浓度越高越好,过量的KCl电解质将对·OH起到捕获作用,会使去除率显著地降低(图7)。Sb(Ⅲ)初始浓度是评价新型电芬顿反应器处理效率的重要依据。图8为Sb(Ⅲ)初始处理浓度对电芬顿体系中Sb(Ⅲ)去除率的影响。可以看出,当初始浓度低于100 mg·L−1时,Sb(Ⅲ)的去除率更高,并且反应速率更快。而初始浓度较高时,去除率明显下降。这是由于在一定的电流强度下,电芬顿反应中生成·OH的量是恒定的,低浓度条件下,能够快速将Sb(Ⅲ)氧化至Sb(Ⅴ),而在浓度较高的情况下,中间产物的竞争会使得Sb(Ⅲ)的氧化效率有所降低[34-35]。但总的来说,在高浓度条件下,·OH与Sb(Ⅲ)的碰撞概率增加,从而使得Sb(Ⅲ)的绝对去除率上升。
-
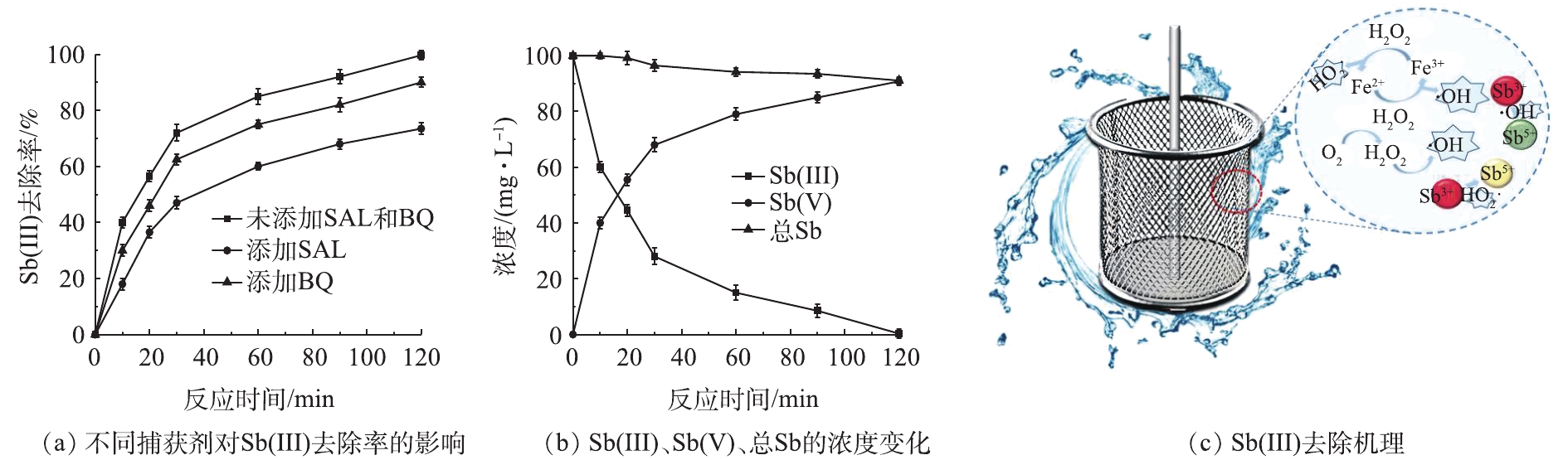
为了探究电芬顿反应对Sb(Ⅲ)的去除机理,设计了一系列的对照实验。通过配制一定量相同浓度的水杨酸(SAL)和苯醌(BQ)溶液,分别投加至溶液中,启动反应,考察Sb(Ⅲ)的去除机理(见图9)。由图9(a)可知,当加入水杨酸作为·OH捕获剂后,Sb(Ⅲ)去除率迅速下降至72.5%。这说明·OH在去除Sb(Ⅲ)的过程中起主要的作用。而除了·OH外,当加入苯醌溶液后,Sb(Ⅲ)去除率下降至90%,这证明过氧化羟自由基HO2·也能对Sb(Ⅲ)/Sb(Ⅴ)的转化起到一定的作用,二者协同作用促进了Sb(Ⅲ)的去除。另外,本研究对阳极的电絮凝作用进行了探讨。在相同浓度的废水中投加0.5 mmol·L−1氯化铁(FeCl3·6H2O),搅拌2 h后,观察到溶液中Sb(Ⅲ)的去除率约为4%,这表明Fe(Ⅲ)在溶液中,除了参与Fenton反应外,还对Sb(Ⅲ)存在一定的凝聚效果。
通过测定废水中Sb类物质浓度随时间的变化,进一步验证Sb(Ⅲ)向Sb(Ⅴ)的转化。如图9(b)所示,反应开始后,Sb(Ⅲ)浓度明显下降,而Sb(Ⅴ)不断上升,这种变化证明了电芬顿体系对Sb(Ⅲ)的氧化能力。在反应终点,总Sb的下降可能是因为一定量的Sb(Ⅴ)在铁絮凝作用下被吸附,以及在阴极表面被还原成Sb。去除过程可以合理地总结为:溶液中的O2在阴极表面还原生成H2O2(式(8)),阳极铁电极氧化产生的Fe(Ⅱ)迅速与H2O2反应产生·OH(式(9)),Fe(Ⅲ)在阴极被还原为Fe(Ⅱ)重新参与Fenton反应,同时会与H2O2反应生成HO2·(式(10)~式(13)),·OH与HO2·协同对Sb(Ⅲ)进行高效氧化(式(14)~式(15)),从而达到对污染物的去除效果(如图9(c)所示)。
-
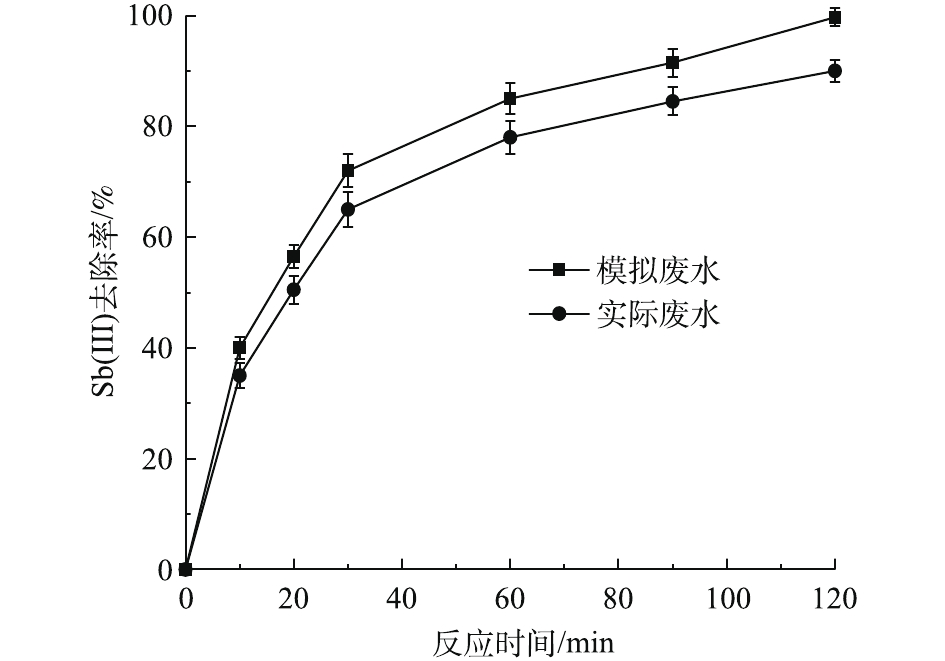
为了验证新型电芬顿反应器在实际废水处理中的可行性,本研究对其在模拟废水与实际废水中的去除率进行了对比,结果如图10所示。可以看出,在最佳反应条件下,实际废水中新型电芬顿反应器对Sb(Ⅲ)的去除率能达到89%,去除率的下降可以用实际废水中其他离子之间对·OH和HO2·的竞争来说明,如Fe(Ⅱ)和As(Ⅲ)等。此外,溶液中的
$ {\rm{C}}{{\rm{O}}_3^{2 - }}$ 、$ {\rm{P}}{{\rm{O}}_4^{2 - }}$ 可能在一定程度上对电芬顿体系中Fe(Ⅱ)/Fe(Ⅲ)的循环起到阻碍作用。此结果表明,新型电芬顿反应器在实际废水处理中仍能保持良好的Sb(Ⅲ)去除率,因此,其可以作为一种高效、应用前景广阔的处理酸性矿山废水中Sb(Ⅲ)的技术。
2.1. 新型电芬顿反应器的优点
2.2. 操作参数的影响
2.3. Sb(Ⅲ)的去除机理
2.4. 实际废水处理
-
1)以电芬顿反应为基础,设计了一种新型阴极旋转式电芬顿反应器,用来处理酸性矿山废水中的Sb(Ⅲ)。相较于传统的电化学处理方法,新型电芬顿反应器处理效率更高,能耗更低。阴极旋转增大了·OH的产量,提升了Sb(Ⅲ)的去除率。
2)·OH和HO2·能够协同作用,共同提高Sb(Ⅲ)的去除效果。在电流强度为120 mA、pH=3、板间距为2 cm、曝气速率为90 mL·min−1、电解质浓度为100 mg·L−1的最佳反应条件下,废水中Sb(Ⅲ)的去除率能够达到99.7%以上。
3)新型电芬顿反应器在实际废水的处理中能够取得很好的效果,Sb(Ⅲ)去除率达到89%以上。




 下载:
下载: