-
近年来,新污染物在水环境中频繁检出,对水生态和人类健康造成了很大的威胁[1 − 2]. 其中,作为一种广谱类抗生素药物,氟苯尼考(FLO)被广泛应用于水产养殖业中[3],未经有效处理直接排放等都将造成水体污染,文献报道其在河流等水体中被检出[4]. 由于新污染物FLO化学结构稳定、生物降解性差导致传统水处理工艺难以高效降解去除[5],因此开发安全高效的去除抗生素的废水处理技术十分关键.
高级氧化技术(AOPs)能够产生高氧化活性的自由基,从而将目标污染物转化为小分子,以实现大多数有机污染物的降解[6]. 而基于活化过一硫酸盐(PMS)的AOPs,由于效率、活性高等特点引起研究者的广泛关注[7]. 其具有的稳定化学性能、易于储存和运输等优点,可显著降低废水处理的成本[8]. 而单独的PMS对于抗生素污染物的降解能力通常有限[9],可通过过渡金属离子等均相反应来高效活化PMS[10]. 同时,相较于均相体系,以过渡金属氧化物作为催化剂的非均相体系更具有可回收性、较高的热稳定性等优势,被广泛研究[11]. 具有多种价态的金属元素锰,在各种过渡金属氧化物中,其锰氧化物(MnOx)是一种高反应活性的金属氧化物,被应用于处理污染物,但是MnOx易团簇可能抑制其催化活性[12]. 为克服这一缺点,目前已有研究将MnOx负载到活性炭、生物炭、碳纳米管等材料上,用于提高MnOx的分散性、稳定性、和催化活性[13 − 14]. 海藻酸钠(SA)作为一种天然多糖,可以与多种金属阳离子(如铁离子,锰离子等)交联形成性能稳定的凝胶[15],将其作为煅烧前驱体,形成的碳复合材料可以有效避免金属氧化物的团聚[16],促进金属氧化物颗粒的稳定分散[17],有效提高了催化活性.
因此,本研究采用海藻酸钠与锰离子交联,煅烧制备了锰氧化物/碳(MnO/C)材料,并对其进行X-射线衍射(XRD)、扫描电镜(SEM)表征,将其应用于活化PMS降解FLO. 同时,分别考察了MnO/C材料和PMS的投加量,以及FLO溶液的pH值对其降解FLO性能的影响,并通过淬灭实验、电子顺磁共振(EPR)测试来分析体系中存在的自由基种类,利用液相色谱-质谱联用(LC-MS)技术解析FLO的降解路径. 最后,将其应用于降解大环内酯类的红霉素(ERY)、磺胺类的磺胺甲恶唑(SMX)和磺胺甲氧嘧啶(SDM)以及喹诺酮类的氧氟沙星(OFL)等典型抗生素以检查其适用性.
-
实验中所用的四水合氯化锰、海藻酸钠、盐酸普萘洛尔、氟苯尼考、组氨酸、盐酸羟胺、磺胺甲恶唑、2,2,6,6-四甲基哌啶、二氧化锰、一氧化锰、红霉素、磺胺甲氧嘧啶、氧氟沙星均购自上海麦克林生化股份有限公司,甲醇、乙腈、乙酸铵、过硫酸氢钾复合盐、氢氧化钠、硫酸、叔丁醇均由西陇科学股份有限公司提供. 实验过程所有用水均为超纯水,所用试剂均为分析纯.
-
将海藻酸钠粉分散在去离子水中,均匀搅拌直至透明黏状,得到2% W/V的海藻酸钠溶液. 将其均匀滴加至浓度为0.1 mol·L−1的四水合氯化锰(MnCl2·4H2O)溶液中,交联形成海藻酸锰水凝胶小球,固化水凝胶小球24 h后用纯水洗净,在−20 ℃下冷冻,得到海藻酸锰气凝胶(Mn-SA). 将Mn-SA在900 ℃氮气氛围中以10 ℃·min−1的加热速率煅烧1 h,冷却至室温后,研磨得到MnO/C材料. 另外,将Mn-SA在空气氛围下煅烧1 h得到对比材料MnO,并将购入的MnO和MnO2命名为MnO-B和MnO2-B作为锰氧化物的性能对比材料.
-
在D8 ADVANVE上进行X射线粉末衍射(XRD)测试,操作电压与电流分别为40 mA和40 kV,扫描速度为5 (°)·min−1,步长0.02°,衍射角范围2θ = 10°−80°;采用场发射扫描电镜(SEM,Regulus
8100 )观察形貌;以2,2,6,6-四甲基哌啶(TEMP)和5,5-二甲基-1吡咯啉(DMPO)为捕获剂,在MS 5000X上进行电子顺磁共振(EPR)测试,鉴定体系中存在的自由基种类,其中测定超氧自由基时采用甲醇作为体系溶剂,使用有机元素分析仪(EA)在氧气和氮气条件下对材料中碳的含量进行测定.样品均采用高效液相色谱法(LC1260, Agilent)检测目标污染物中FLO的残余浓度,配备紫外检测器和Agilent Zorbax SB-C18色谱柱(4.6 mm×150 mm, 5 μm),其中紫外检测波长为224 nm,以甲醇和超纯水(4:6)为流动相,进样量为10 μL,柱温为30 ℃. 磺胺甲氧嘧啶(SDM)、红霉素(ERY)、氧氟沙星(OFL)、磺胺甲恶唑(SMX)均以乙腈和乙酸铵(3:7)为流动相,进样量为10 μL,柱温为35 ℃,其中,SDM、ERY、OFL、SMX的检测波长分别为:270 nm、210 nm、294 nm、270 nm.
FLO降解的中间产物的鉴定是在超高效液相色谱-串联质谱(UPLC-MS)系统(AB SciexTripleTOF
5600 )上进行的,该系统配备了负离子扫描模式下的四极飞行时间(QTOF)检测器. 分析物的分离是在反相C18柱上以0.8 mL·min−1的流速进行的,流动相为甲醇和水,二者的比例为3:7. 最后,使用Qualitative Analysis 10.0软件分析确认降解产物.进行数据分析时,使用修正后的动力学速率常数(kvalue)对活化PMS去除FLO的降解动力学进行评价[18]. 通过将拟合后的有机污染物的速率常数(k)除以催化剂的剂量(d)和氧化剂浓度(C1),再乘以有机污染物浓度(C0),计算出修正kvalue,计算公式如下:
-
在FLO溶液中加入一定量的催化剂和一定浓度的PMS在室温条件下进行降解反应,并在相同条件下探究溶液pH对降解体系的影响,通过降解不同抗生素以证明该体系具有普适性. 实验过程中,每隔一段时间(0、5、10、15、30、45、60 min),提取1 mL溶液经过0.22 μm聚四氟乙烯过滤器过滤后,立即加入盐酸羟胺终止反应,待测.
具体实验条件为:在10 mg·L−1 FLO、0.2 mmol·L−1 PMS、0.2 g·L−1 MnO/C、溶液pH = 7条件下探究其降解FLO的性能;在实验条件为0.2 g·L−1 MnO/C、溶液pH = 7的条件下,将PMS浓度设置为0.1、0.2、0.3、0.4 mmol·L−1,以探究PMS的最优条件;在0.3 mmol·L−1 PMS、溶液pH = 7的条件下,分别向体系中投加0、0.1、0.2 g·L−1 MnO/C材料,用于研究材料用量对降解FLO的影响;除此之外,在0.3 mmol·L−1 PMS、0.2 g·L−1 MnO/C的条件下,用稀硫酸和氢氧化钠调节体系溶液pH值,分别为3、5、7、9、11,以探究溶液pH值对降解污染物的影响;在实验条件为:0.2 g·L−1 MnO/C、0.3 mmol·L−1 PMS、溶液pH = 7的条件下探究其对不同抗生素的降解效果,使用的抗生素浓度均为10 mg·L−1. 淬灭实验中采用分别添加10 mmol·L−1的组氨酸(His)和叔丁醇(TBA)对MnO/C-PMS体系进行淬灭.
-
制备的材料的XRD表征结果如图1(a)所示. 由图1(a)可见,MnO/C和MnO在2θ = 34.20°、39.69°、57.39°、68.52°和72.03°均出现了明显的衍射峰,分别对应MnO(PDF标准卡片 ICDD 065-0638)的(111)、(200)、(220)、(311)和(222)晶面. 在MnO/C的XRD图谱上观察到在2θ = 24°出现鼓包峰,这可能是因为MnO/C材料中存在无定形碳[19]. 通过有机元素分析仪(EA)测定其可能的元素组分,其中碳在MnO/C的占比为35.7%,证明该材料中含有碳. 图1(b)通过扫描电子显微镜(SEM)观察样品MnO/C的形貌,发现MnO/C材料为细碎颗粒状,大小不一,表面粗糙不平,这可能使得其具有更大的反应面积和更密集的接触面积有利于提供反应活性位点[20].
-
首先,探究MnO/C是否能够活化PMS降解FLO. 如图2(a)所示,仅PMS体系对FLO的降解效果不理想,60 min时仅为2%. 在仅MnO/C体系下,15 min时FLO的去除效率达到34%,60 min时提高至69%,这可能是由于MnO/C复合材料具有较大的比表面积(361.5 m2·g−1),其对污染物具有一定的吸附能力[14]. 而在PMS和MnO/C共存的体系中,FLO去除的速率显著提升,15 min内达到了70%,并达到平衡.
探究PMS浓度对MnO/C性能的影响. 如图2(b)所示,当PMS浓度由0.1 mmol·L−1增加到0.2 mmol·L−1时反应速率明显增加,并在15 min时迅速达到平衡. 对不同PMS浓度体系进行拟合,对应的反应速率常数如图2(c)所示,分别为:k0.3(0.143 min−1)>k0.4(0.102 min−1)>k0.2(0.075 min−1)>k0.1(0.042 min−1),在PMS为0.3 mmol·L−1下,其去除FLO的速率最快,当PMS的浓度超过该浓度后,体系去除FLO的效率不再提升. 这可能是因为吸附在MnO/C材料表面的PMS分子趋于饱和[21],过量将不再提高FLO的降解率. 因此,选用0.3 mmol·L−1 PMS作为实验的最佳用量. 进一步探究MnO/C用量对FLO降解效率的影响,由图2(d)可知,未投加MnO/C的体系中,相较于图2(a),PMS从0.2 mmol·L−1提升至0.3 mmol·L−1,FLO去除效率仅提高3%,少量去除可能是因为PMS自身分解生成的活性氧物种增加所致[22]. 而在PMS和MnO/C共存的体系中,MnO/C用量为0.2 g·L−1时,其降解FLO的速率和效率明显优于MnO/C用量为0.1 g·L−1时,在15 min内降解85%的FLO. 这可能是由于随着MnO/C的用量提升,可供激活PMS的活性位点也在增加[23],从而提升了FLO的降解效率. 因此,选择0.2 g·L−1的MnO/C用量作为实验最佳用量.
溶液pH值对污染物的去除具有重要影响,因此,探究不同pH值对MnO/C-PMS体系降解FLO的影响. 如图2(e)所示,体系的pH值会对MnO/C催化剂降解FLO的实验产生较大的影响. 在MnO/C-PMS体系中,pH值为7时反应15 min降解了8.5 mg·g−1的FLO,经计算其kvalue值为23.83 min−1·mol·L−1. 同时,在酸性条件下(pH值为3和5时),MnO/C也高效活化了PMS,30 min内FLO的降解率均可达85%以上. 在碱性条件下,FLO的降解效率和速率虽仍有效果,但显著下降,在30 min内去除率仅为50%左右. 实验结果表明,反应速率随着反应体系pH的升高而下降,这可能是由于锰氧化物的催化效果受pH的影响较大. 以Mn2+形式存在的锰在酸性环境下更容易被氧化成Mn3+[24]. 该转化过程可能有利于促进水分子与Mn3+反应产生单线态氧(1O2),从而提高催化活性. 而在碱性条件下,锰离子的氧化还原反应可能受到抑制,这可能是因为Mn2+在碱性环境中会形成氢氧化锰沉淀,Mn2+的浓度下降影响了Mn3+的生成,从而导致活性氧的生成效率降低[25]. 综上,MnO/C-PMS体系能够在pH范围为3—7的条件下有效活化PMS,实现对FLO的高效去除. 结合实际水体条件以及MnO/C的性能测试,选用pH = 7用于后续机理研究.
为了判别所制备MnO/C材料的优异性能,进一步对比同等反应条件下,MnO(空气煅烧Mn-SA制得,作为同条件下制的未含碳的MnO)、MnO/C-B及MnO2-B活化PMS降解FLO的效果,结果如图2(f)所示,MnO-B-PMS体系、MnO2-B-PMS和MnO-PMS体系对FLO几乎没有去除效果,在60 min内降解率均低于17%,这可能是因为单一金属氧化物颗粒团聚,使锰氧化物体系降解污染物效率不高[14,26]. 表明了以水凝胶作为前驱体制备的MnO/C材料,在煅烧碳化过程中,金属可以有效分散在碳上. 该锰与碳相结合的策略可以有效提高锰氧化物的催化活性. 进一步对比已报道的催化剂活化PMS去除FLO研究可知,相较于LaMBC(kvalue=0.41 min-1·mol·L−1)[27]、Co3O4-BC(kvalue=0.99 min−1·mol·L−1)[28],本文的kvalue值达到了23.83 min−1·mol·L−1,MnO/C展现出了较大的性能优势,表明该材料能够在较低的材料用量(0.2 g·L−1)和PMS浓度(0.3 mmol·L−1)下高效活化PMS降解FLO.
-
通过EPR的测试鉴定体系中的活性氧物种,结果如图3(a、b)所示,以DMPO为捕获剂时,未检测到DMPO-·OH、DMPO-SO4·-和DMPO-· O2−的特征信号峰,表明该体系过程中可能产生的·OH、SO4·-和·O2−较少或极易被转化而未检测到. 而以TEMP为捕获剂时,该体系检测到1O2,说明催化剂MnO/C活化PMS过程中生成了1O2. 因此,认为·OH、SO4·-和·O2−并不是该体系中的主要活性自由基,而生成的1O2在去除FLO的过程中可能发挥主要作用[27]. 为进一步探究MnO/C催化剂活化PMS的机理,进行自由基的淬灭实验. 其中,叔丁醇(TBA)用于淬灭体系中可能存在的·OH和SO4·-[29],其结果如图3(c)所示. TBA的引入使FLO的降解速率下降,k值由0.143 min−1变化为0.049 min−1,但在60 min内仍保持85%的去除效率. 这可能是由于反应过程中生成少量的·OH和SO4·-,对反应有一定影响,但并不是影响FLO去除的主要活性自由基. 将作为1O2淬灭剂的组氨酸[30]引入到体系中,在60 min时FLO的降解率仅为13%. 对比未加入淬灭剂的体系(85%),组氨酸的引入显著抑制了FLO的降解. 因此,结合EPR的测试结果(图3(a)),认为在MnO/C-PMS体系中,1O2可能是主导FLO降解过程的主要活性物种.
综上所述,以Mn-SA为前驱体煅烧制备的MnO/C复合材料中锰作为催化活性中心,能够有效激活PMS(反应方程式1、2),形成的SO5−能够与水反应进一步生成1O2(反应方程式3),形成的1O2用于降解FLO等新兴有机污染物. 另外,过程中形成的SO4−·会与水作用,转变为其他物质(反应方程式4)[31]. 对比不同的锰氧化物和已报道的文献可知,Mn-SA作为煅烧前驱体可以有效促进金属氧化物颗粒稳定分散在碳上,该复合材料提高了MnO的催化活性,更有利于活化PMS产生1O2,具体机理如图4所示.
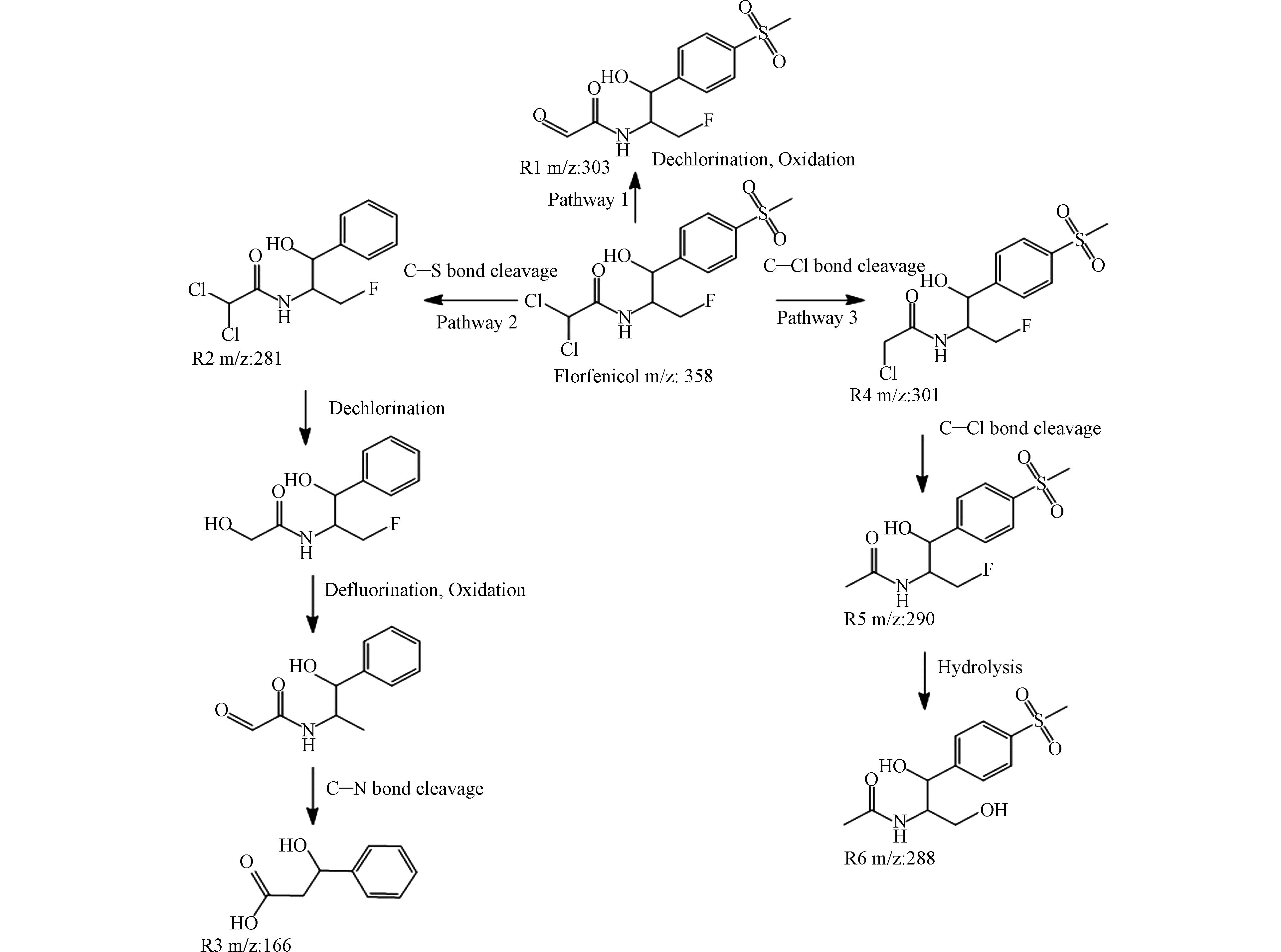
测定反应过程生成的中间产物可以进一步分析FLO的降解路径,本文采用LC-MS检测MnO/C-PMS体系中,FLO降解生成的中间产物. 反应过程中,除了FLO之外,分别检出了R1、R2、R3、R4、R5、R6等6种物质(图5),进一步推测FLO的降解路径,如图5所示. FLO的降解路径包括水解、羟基化、脱氟、脱氯氧化[32 − 35]. 其中,路径1是通过活性氧的作用实现脱氯、氧化,产生小分子产物及氯离子[32],而在路径2中,R2-R3的过程是由于C—S键受到攻击断裂,而后实现脱氯氧化,进一步促进脱氟,形成分子量更小的产物[33]. 路径3中,C—C键先行断裂,产生R4,而后进一步脱氯产生R5[34]. 从R5到R6的过程主要是由于FLO完全脱氯后会产生的自发水解反应,使得产物进一步的分解[35]. 该实验结果证明,MnO/C-PMS体系选择性产生的1O2可以有效帮助FLO进行脱卤和氧化,产生分子量更小的产物.
-
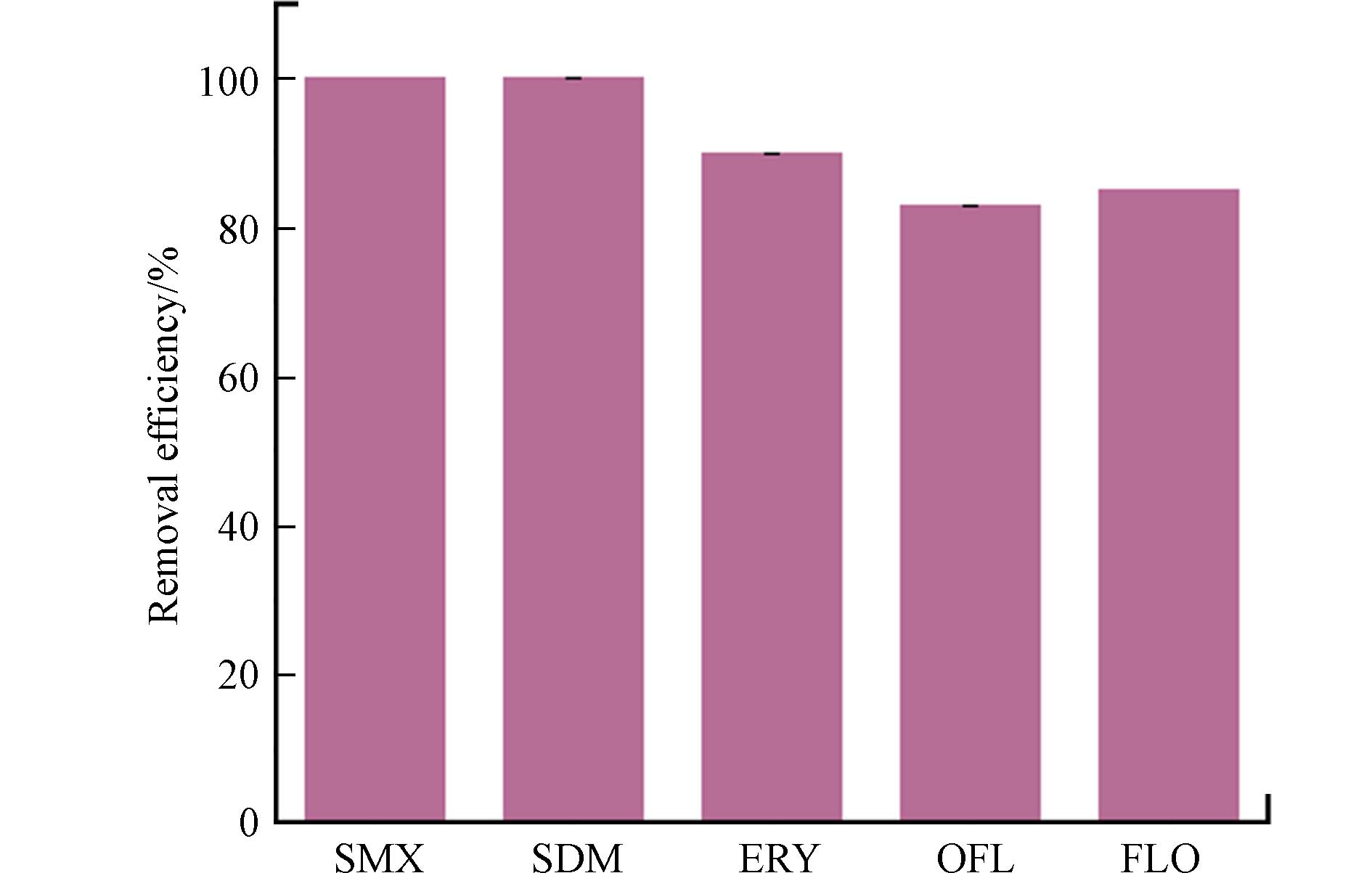
为了测试MnO/C-PMS体系对不同污染物的降解效果,选取了大环内酯类的ERY(红霉素)、磺胺类的SMX(磺胺甲恶唑)和SDM(磺胺甲氧嘧啶)以及喹诺酮类的OFL(氧氟沙星)作为不同种类的抗生素进行MnO/C活化PMS性能测试研究. 如图6所示,该体系对SDM、SMX均有较好的去除效果,降解效率均达到了100%,ERY的降解率为90%,OFL的降解率为83%. 由结果可知,该体系对新污染物均具有良好的降解效果(均>83%),能够满足不同类型的抗生素的处理要求,对新污染物的去除具有良好的应用潜力和适用性.
-
采用绿色环保的海藻酸锰水凝胶小球作为前驱体,并冷却干燥煅烧衍生制备碳负载一氧化锰(MnO/C)的复合材料,可以有效将MnO分散在碳上,使其表现出较高的催化活性,通过活化PMS可以高效去除抗生素等新污染物. MnO/C-PMS体系在15 min内降解了8.5 mg·g−1 (kvalue=23.83 min−1·mol·L−1)的FLO. 其机理主要为选择性生成1O2的非自由基路径实现降解,对FLO的降解机理主要包括脱卤和氧化过程. 同时,该体系对磺胺类的磺胺甲氧嘧啶(SDM)、大环内酯类的红霉素(ERY)和喹诺酮类的氧氟沙星(OFL)等典型新污染物均具有良好的降解效果. 本文中的金属锰与海藻酸钠交联煅烧形成的MnO/C复合材料为高级氧化水处理的绿色过程提供了策略,具有潜在的应用价值.
锰氧化物/碳活化过硫酸盐选择性生成单线态氧降解水中氟苯尼考
Research on the selective generation of singlet oxygen from manganese oxide/carbon activated persulfate for the degradation of florfenicol in water
-
摘要: 为实现养殖废水中的新污染物氟苯尼考(FLO)的高效降解,本研究制备了锰氧化物/碳材料(MnO/C)用于活化过一硫酸盐(PMS)去除FLO. 首先,考察了PMS用量、MnO/C用量、溶液pH值等对水中FLO去除的影响. 结果表明,在PMS浓度为0.3 mmol·L−1、MnO/C用量为0.2 g·L−1、FLO浓度为10 mg·L−1,pH值为7时,15 min内降解了8.5 mg·g−1 (kvalue=23.83 min−1·mol·L−1)的FLO. 并通过自由基淬灭实验及电子顺磁共振测试(EPR)分析表明,MnO/C-PMS体系中主要以单线态氧(1O2)的非自由基路径催化降解FLO,液质分析结果可知,MnO/C-PMS对FLO的降解机理主要包括脱卤和氧化. 且该体系对磺胺类的磺胺甲氧嘧啶(SDM)、大环内酯类的红霉素(ERY)和喹诺酮类的氧氟沙星(OFL)等典型新污染物均具有良好的降解效果(均>83%). 因此,MnO/C在活化PMS上表现出对新污染物良好的降解能力,具有潜在应用性.
-
关键词:
- 氟苯尼考 /
- 锰氧化物/碳复合材料 /
- 过一硫酸盐 /
- 非自由基路径 /
- 高级氧化
Abstract: In order to efficiently degrade the new pollutant florfenicol (FLO) in aquaculture wastewater, this study prepared carbon-coated manganese oxide materials (MnO/C). Firstly, the effects of PMS concentration, MnO/C concentration, solution pH value on the removal of FLO were discussed, respectively. The degradation rate of FLO was 8.5 mg·g−1 in 15 min (kvalue=23.83 min−1·mol·L−1), under the experimental conditions: FLO concentration was 10 mg·L−1, PMS concentration was 0.3 mmol·L−1, MnO/C concentration was 0.2 g·L−1 and pH = 7. It was demonstrated by radical scavenger experiment, electron paramagnetic resonance (EPR) tests, and liquid chromatography-mass spectrometry (LC-MS) analysis. The non-radical pathways (1O2 oxidation) dominated in the MnO/C-PMS and FLO are primarily dehalogenation and oxidized. Subsequently, The system also demonstrates effective degradation of typical emerging contaminants such as sulfamethoxypyridazine (SDM), erythromycin (ERY), and ofloxacin (OFL), with degradation rates all exceeding 83%. Therefore, MnO/C exhibits strong potential for the activation of PMS and degradation of organic pollutants, showing promising application prospects. -

-
图 2 MnO/C-PMS反应体系降解FLO(a)、不同PMS浓度FLO降解效率的影响(b)及其拟合结果(c)、MnO/C用量对FLO降解效率的影响(d)、溶液pH对FLO降解效率影响(e)、不同材料降解FLO的性能(f)
Figure 2. Degradation of FLO in the MnO/C-PMS system (a); Effect of different PMS concentrations on FLO degradation efficiency (b) and its fitting results(c); Effect of MnO/C dosage on FLO degradation efficiency (d); Effect of initial pH on FLO degradation efficiency (e); Performance of different materials in FLO degradation (f)
-
[1] YU L H, ZHENG S, GAO Q. Government environmental regulation strategy for new pollutants control in mariculture[J]. Marine Policy, 2023, 150: 105545. doi: 10.1016/j.marpol.2023.105545 [2] CABELLO F C. Heavy use of prophylactic antibiotics in aquaculture: a growing problem for human and animal health and for the environment[J]. Environmental Microbiology, 2006, 8(7): 1137-1144. doi: 10.1111/j.1462-2920.2006.01054.x [3] ORLANDO E A, COSTA ROQUE A G, LOSEKANN M E, et al. UPLC–MS/MS determination of florfenicol and florfenicol amine antimicrobial residues in Tilapia muscle[J]. Journal of Chromatography B, 2016, 1035: 8-15. doi: 10.1016/j.jchromb.2016.09.013 [4] OLIVEIRA A S, ALVES M, LEITÃO F, et al. Bioremediation of coastal aquaculture effluents spiked with florfenicol using microalgae-based granular sludge–a promising solution for recirculating aquaculture systems[J]. Water Research, 2023, 233: 119733. doi: 10.1016/j.watres.2023.119733 [5] ESMAILI Z, CHESHMBERAH F, SOLAIMANY NAZAR A R, et al. Treatment of florfenicol of synthetic trout fish farm wastewater through nanofiltration and photocatalyst oxidation[J]. Environmental Technology, 2017, 38(16): 2040-2047. doi: 10.1080/09593330.2016.1245359 [6] BABU PONNUSAMI A, SINHA S, ASHOKAN H, et al. Advanced oxidation process (AOP) combined biological process for wastewater treatment: A review on advancements, feasibility and practicability of combined techniques[J]. Environmental Research, 2023, 237: 116944. doi: 10.1016/j.envres.2023.116944 [7] XIAO S, CHENG M, ZHONG H, et al. Iron-mediated activation of persulfate and peroxymonosulfate in both homogeneous and heterogeneous ways: A review[J]. Chemical Engineering Journal, 2020, 384: 123265. doi: 10.1016/j.cej.2019.123265 [8] ZHAO X, AN Q D, XIAO Z Y, et al. Seaweed-derived multifunctional nitrogen/cobalt-codoped carbonaceous beads for relatively high-efficient peroxymonosulfate activation for organic pollutants degradation[J]. Chemical Engineering Journal, 2018, 353: 746-759. doi: 10.1016/j.cej.2018.07.171 [9] ANJORIN E O, ALFRED M O, SOTUNDE B, et al. Overview of the mechanism of degradation of pharmaceuticals by persulfate/peroxysulfate catalysts[J]. ChemBioEng Reviews, 2024, 11(4): e202300079. doi: 10.1002/cben.202300079 [10] YANG Y Y, ZHANG P P, HU K S, et al. Sustainable redox processes induced by peroxymonosulfate and metal doping on amorphous manganese dioxide for nonradical degradation of water contaminants[J]. Applied Catalysis B: Environmental, 2021, 286: 119903. doi: 10.1016/j.apcatb.2021.119903 [11] LIN K Y , CHEN Y C, LIN Y F. LaMO3 perovskites (M=Co, Cu, Fe and Ni) as heterogeneous catalysts for activating peroxymonosulfate in water[J]. Chemical Engineering Science, 2017, 160: 96-105. [12] WANG Y X, XIE Y B, CHEN C M, et al. Synthesis of magnetic carbon supported manganese catalysts for phenol oxidation by activation of peroxymonosulfate[J]. Catalysts, 2017, 7(1): 3. [13] ORGE C A, ÓRFÃO J J M, PEREIRA M F R. Composites of manganese oxide with carbon materials as catalysts for the ozonation of oxalic acid[J]. Journal of Hazardous Materials, 2012, 213: 133-139. [14] 李珏秀, 施启旭, 赵锐, 等. 锰基催化剂用于活化过硫酸盐降解有机废水的研究进展[J]. 环境化学, 2023, 42(11): 3861-3877. doi: 10.7524/j.issn.0254-6108.2023011704 LI J X, SHI Q X, ZHAO R, et al. Research progress on manganese based catalysts for activating persulfate degradation of organic wastewater[J]. Environmental Chemistry, 2023, 42(11): 3861-3877 (in Chinese). doi: 10.7524/j.issn.0254-6108.2023011704
[15] LIU L, LIU Z, CHEN Y, et al. In-situ synthesis of manganese oxide-carbon nanocomposite and its application in activating persulfate for bisphenol F degradation[J]. Science of the Total Environment, 2021, 772: 144953. doi: 10.1016/j.scitotenv.2021.144953 [16] DO S H, KWON Y J, BANG S J, et al. Persulfate reactivity enhanced by Fe2O3-MnO and CaO-Fe2O3-MnO composite: Identification of composite and degradation of CCl4 at various levels of pH[J]. Chemical Engineering Journal, 2013, 221: 72-80. doi: 10.1016/j.cej.2013.01.097 [17] DIAO Z H, QIAN W, GUO P R, et al. Photo-assisted degradation of bisphenol A by a novel FeS2@SiO2 microspheres activated persulphate process: Synergistic effect, pathway and mechanism[J]. Chemical Engineering Journal, 2018, 349: 683-693. doi: 10.1016/j.cej.2018.05.132 [18] ZHOU Q X, SONG C L, WANG P F, et al. Generating dual-active species by triple-atom sites through peroxymonosulfate activation for treating micropollutants in complex water[J]. Proceedings of the National Academy of Sciences of the United States of America, 2023, 120(13): e2300085120. [19] 郑佳慧, 王嘉妮, 柯佳琪, 等. 碳氮包覆纳米Fe3O4的非自由基路径光催化去除养殖废水中四环素的机制研究[J]. 环境科学研究, 2023, 36(7): 1306-1316. ZHENG J H, WANG J N, KE J Q, et al. Mechanism of tetracycline removal from aquaculture wastewater by carbon nitrogen coated nano-Fe3O4 via non-free radical photocatalysis[J]. Research of Environmental Sciences, 2023, 36(7): 1306-1316 (in Chinese).
[20] LING C Y, QIN X Z, JIANG L J, et al. Investigation of the Effect of Manganese Oxides on the Reduction of Hexavalent Chromium by Sodium Alginate-Dispersed Nano-Zero-Valent Iron and the Mechanism[J]. Water Air Soil Pollut, 2023, 234(3): 187. doi: 10.1007/s11270-023-06209-8 [21] HUANG G X, WANG C Y, YANG C W, et al. Degradation of Bisphenol A by peroxymonosulfate catalytically activated with Mn1.8Fe1.2O4 nanospheres: Synergism between Mn and Fe[J]. Environmental Science & Technology, 2017, 51(21): 12611-12618. [22] HU P D, LONG M C. Cobalt-catalyzed sulfate radical-based advanced oxidation: A review on heterogeneous catalysts and applications[J]. Applied Catalysis B: Environmental, 2016, 181: 103-117. doi: 10.1016/j.apcatb.2015.07.024 [23] YAO J Y, WU N N, TANG X S, et al. Methyl phenyl sulfoxide (PMSO) as a quenching agent for high-valent metal-oxo species in peroxymonosulfate based processes should be reconsidered[J]. Chemical Engineering Journal Advances, 2022, 12: 100378. doi: 10.1016/j.ceja.2022.100378 [24] DENG J, GE Y J, TAN C Q, et al. Degradation of ciprofloxacin using α-MnO2 activated peroxymonosulfate process: Effect of water constituents, degradation intermediates and toxicity evaluation[J]. Chemical Engineering Journal, 2017, 330: 1390-1400. doi: 10.1016/j.cej.2017.07.137 [25] HUANG J Z, ZHONG S F, DAI Y F, et al. Effect of MnO2 Phase Structure on the Oxidative Reactivity toward Bisphenol A Degradation[J]. Environmental Science & Technology, 2018, 52(19): 11309-11318. [26] XU H D, ZHANG Y C, LI J J, et al. Heterogeneous activation of peroxymonosulfate by a biochar-supported Co3O4 composite for efficient degradation of chloramphenicols[J]. Environmental Pollution, 2020, 257: 113610. doi: 10.1016/j.envpol.2019.113610 [27] PENG Y F, XUE C J, LUO J Y, et al. Lanthanum-doped magnetic biochar activating persulfate in the degradation of florfenicol[J]. Science of The Total Environment, 2024, 916: 170312. doi: 10.1016/j.scitotenv.2024.170312 [28] ZHAO Y, LI B, LI Y, et al. Synergistic activation of peroxymonosulfate between Co and MnO for bisphenol A degradation with enhanced activity and stability[J]. Journal of Colloid and Interface Science, 2022, 623: 775-786. doi: 10.1016/j.jcis.2022.05.105 [29] CHEN J S, LUO H Y, LUO D Y, et al. New insights into the degradation of nitrobenzene by activated persulfate with sulfidated nanoscale zero-valent iron: Synergistic effects of reduction and reactive oxygen species oxidation[J]. Separation and Purification Technology, 2023, 322: 124252. doi: 10.1016/j.seppur.2023.124252 [30] XU A L, WU D H, ZHANG R, et al. Bio-synthesis of Co-doped FeMnOx and its efficient activation of peroxymonosulfate for the degradation of moxifloxacin[J]. Chemical Engineering Journal, 2022, 435: 134695. doi: 10.1016/j.cej.2022.134695 [31] CHEN M J , YANG T X, ZHAO L Y, et al. Manganese oxide on activated carbon with peroxymonosulfate activation for enhanced ciprofloxacin degradation: Activation mechanism and degradation pathway[J]. Applied Surface Science, 2024, 645: 158835. [32] ZHANG Y, LI J H, ZHOU L, et al. Aqueous photodegradation of antibiotic florfenicol: kinetics and degradation pathway studies[J]. Environmental Science and Pollution Research International, 2016, 23(7): 6982-6989. doi: 10.1007/s11356-015-5897-1 [33] WANG X Y, LUO X Y, LI R, et al. Boosting peroxymonosulfate activation over partial Zn-substituted Co3O4 for florfenicol degradation: Insights into catalytic performance, degradation mechanism and routes[J]. Chemical Engineering Journal, 2024, 491: 152197. doi: 10.1016/j.cej.2024.152197 [34] TANG Z, KONG Y F, QIN Y, et al. Performance and degradation pathway of florfenicol antibiotic by nitrogen-doped biochar supported zero-valent iron and zero-valent copper: A combined experimental and DFT study[J]. Journal of Hazardous Materials, 2023, 459: 132172. doi: 10.1016/j.jhazmat.2023.132172 [35] CHEN Z H, CHEN J D, TAN S D, et al. Dechlorination Helps Defluorination: Insights into the Defluorination Mechanism of Florfenicol by S-nZVI and DFT Calculations on the Reaction Pathways[J]. Environmental Science & Technology, 2024, 58(5): 2542-2553. -




 下载:
下载: