-
腐殖酸是一类广泛存在于多种水体中难生物降解的高分子有机物,浓度范围为0.1~200 mg·L−1[1-3]。其结构复杂、组成多变,常与有机物、重金属等发生络合反应造成复合污染[4],为人类的生产生活带来了诸多问题。一方面,腐殖酸在给水处理消毒过程中可与氯反应生成卤乙酸等致畸致癌副产物,同时在管网输送过程中腐蚀管道、增加微生物繁殖概率[5]。另一方面,腐殖酸能通过影响人体对无机元素的吸收代谢平衡诱发大骨病[6]。此外,垃圾渗滤液中含有的腐殖酸会导致后续渗滤液膜处理系统的污染与堵塞[7]、增大处理难度[8]。因此去除多种水体中的腐殖酸是亟待解决的问题。
目前腐殖酸主要使用混凝法、吸附法等方法去除[9],但受限于其结构复杂性和难生物降解性,各种方法均有一定不足,例如混凝法去除不彻底且大大增加污泥产量[10]。近年来,光催化是一种安全高效、环境友好的处理技术,可以利用阳光产生活性氧物种,将大分子有机污染物转化为无毒无害的产物[11]。RAJCA和BODZEK[12]研究了二氧化钛光催化剂降解腐殖酸的反应过程与特征规律,证明了二氧化钛光催化降解腐殖酸的可行性,但二氧化钛光催化剂存在低太阳能利用率 (<4%) 和高光生载流子复合率等问题[13]。
针对上述问题,目前可通过掺杂、复合等方式来提高光催化活性[14],其中碳量子点 (CDs) 具有良好的光致发光性能和上转换发光特性,可以将光响应范围扩大到可见光和近红外光区域,有效抑制电子-空穴对的复合,因此碳点及其复合光催化剂在水环境治理方面去除有机物受到持续关注[15-16]。LI等[17]利用水热法制备了CDs-TiO2纳米片光催化剂 (CDs-TNs) ,在Ti-O-C键的作用下CDs均匀地分散在TiO2纳米片上,改善了TiO2对四价Cr的光催化还原性能。SHEN等[18]制备的CQDs/TiO2光催化剂较TiO2在降解刚果红、罗丹明B和四环素时均表现出优异的光催化活性。目前碳点复合光催化剂降解腐殖酸的降解效果未知、机理研究不清,因此本研究采用水热法制备了碳点复合光催化剂 (CDs/P25) ,将其应用在腐殖酸处理过程中,探究合成条件对复合材料降解腐殖酸性能的影响,择优对其物化性质进行表征,并进一步阐明该催化反应的作用机理。
-
一水柠檬酸 (C6H8O7·H2O) 、氨水 (NH3·H2O) 为优级纯,氢氧化钠 (NaOH) 、二氧化钛 (TiO2,P25) 为分析纯,腐殖酸为生物试剂,实验用水为超纯水。配制200 mg·L−1的腐殖酸标准溶液方法为:称取0.20 g的腐殖酸,溶于1 000 mL浓度为0.1 mol·L−1的NaOH溶液,超声搅拌后放置24 h,将上述溶液用0.45 μm滤膜抽滤,密封保存待用。
-
本研究采用水热法制备复合材料CDs/P25。将不同质量 (2.52、5.04 g) 的一水柠檬酸溶解于60 mL去离子水中,通过滴加浓氨水调节 pH至一定值 (6、8) 。称取0.96 g 二氧化钛加入到上述混合液中,磁力搅拌、超声30 min使其分散均匀。将此混合液转移至100 mL反应釜中,在不同温度下 (160、200 °C) 恒温反应一定时间 (4、6 h) 后,自然冷却到室温。将得到的棕色固体自然冷却至室温后进行离心,经无水乙醇及超纯水洗涤3次,置于60 °C真空干燥箱烘干12 h,研磨得到粉末备用[17]。
-
本研究采用场发射透射电子显微镜 (Talos F200S G2 S/TEM,赛默飞科技有限公司) 对催化剂进行形貌分析,加速电压200 kV,点分辨率0.25 nm;材料进行镀金处理后采用能谱仪 (Model 550i,美国IXRF公司) 对催化剂进行元素组成分析;采用比表面积分析仪 (ASAP 2020 PLUS HD88,美国麦克默瑞提克公司) 在氮气吸附下对催化剂进行吸附性能分析;采用Zeta电位测试仪 (Nano-ZS90,英国马尔文仪器有限公司) 测定催化剂Zeta值;采用X射线光电子能谱仪 (K-Alpha,赛默飞科技有限公司) 和傅里叶变换红外光谱仪 (IRTracer-100,日本岛津仪器公司) 对催化剂进行化学成键分析,其中红外扫描范围
4000 cm−1~400 cm−1,扫描次数32,分辨率4 cm−1;采用电化学工作站 (Zennium C-IMPS,德国札纳电化学公司) 0.8 V测试电压光照条件下,对催化剂进行阻抗性能分析;采用荧光分光光度计 (LS 55,珀金埃尔默股份有限公司) 对催化剂进行光致发光光谱测试;采用紫外分光光度计 (lambda1050 ,珀金埃尔默股份有限公司) 对催化剂进行紫外可见漫反射光谱测试。 -
本研究采用双层夹套烧杯进行光催化降解实验。光源由氙灯 (CEL-HXF300,北京中教金源科技有限公司) 提供。首先称取0.075 g的催化剂加入到150 mL腐殖酸溶液中,进行持续磁力搅拌。在黑暗处60 min达到吸附-解吸平衡后,进行光照反应240 min。每隔30 min取5 mL反应样品,采用12 000 r·min−1 离心处理15 min,取上清液使用0.22 μm水系针式过滤器进行过滤后,用紫外可见分光光度计 (UV-
1800 ,日本岛津仪器公司) 测定溶液中腐殖酸含量变化情况。其中在254 nm波长下的吸光度 (UV254) 代表腐殖酸中C=C双键和C=O双键的芳香基团的含量[19-20],在400 nm波长下的吸光度 (VIS400) 代表腐殖酸中的发色基团含量[21]。采用电子顺磁共振波谱仪 (A300,德国布鲁克公司) 测试催化过程自由基信号;采用高分辨率液质联用仪 (Q Exactive Focus,赛默飞科技有限公司) 分析光催化过程中间产物和降解路径。具体分析条件为:色谱柱 (2.1 mm×100 mm,HILIC,美国沃特世科技有限公司) ,流速0.28 mL·min−1,进样体积3 μL,流动相A为水溶液 (0.1%甲酸+10 mmol·L−1乙酸铵) ,流动相B为乙腈+10 mmol·L−1乙酸铵,采用梯度洗脱程序。质谱采用电喷雾离子源,以负离子模式采集数据,扫描范围为50~750 m·z−1,通过Compound Discoverer软件包 (v3.3.0.550) 进行数据提取和分析。 -
本研究首先考察了碳点负载量、水热反应pH、水热温度、水热时间共四个因素对复合材料性能的影响。表1为各材料合成具体条件,CDs/P25-A的碳点负载量为0.2 mol·L−1,滴加氨水调节反应溶液pH为6,在水热温度为160 ℃的条件下恒温反应4 h。CDs/P25-B与CDs/P25-C均在CDs/P25-A的合成条件下进行调控,其中CDs/P25-B合成pH增大至8,水热温度升高为200 ℃,水热时间增加至6 h;CDs/P25-C调整碳点负载量为0.4 mol·L−1,水热温度与水热时间与CDs/P25-B相同,以此实现对催化剂的优化探究。
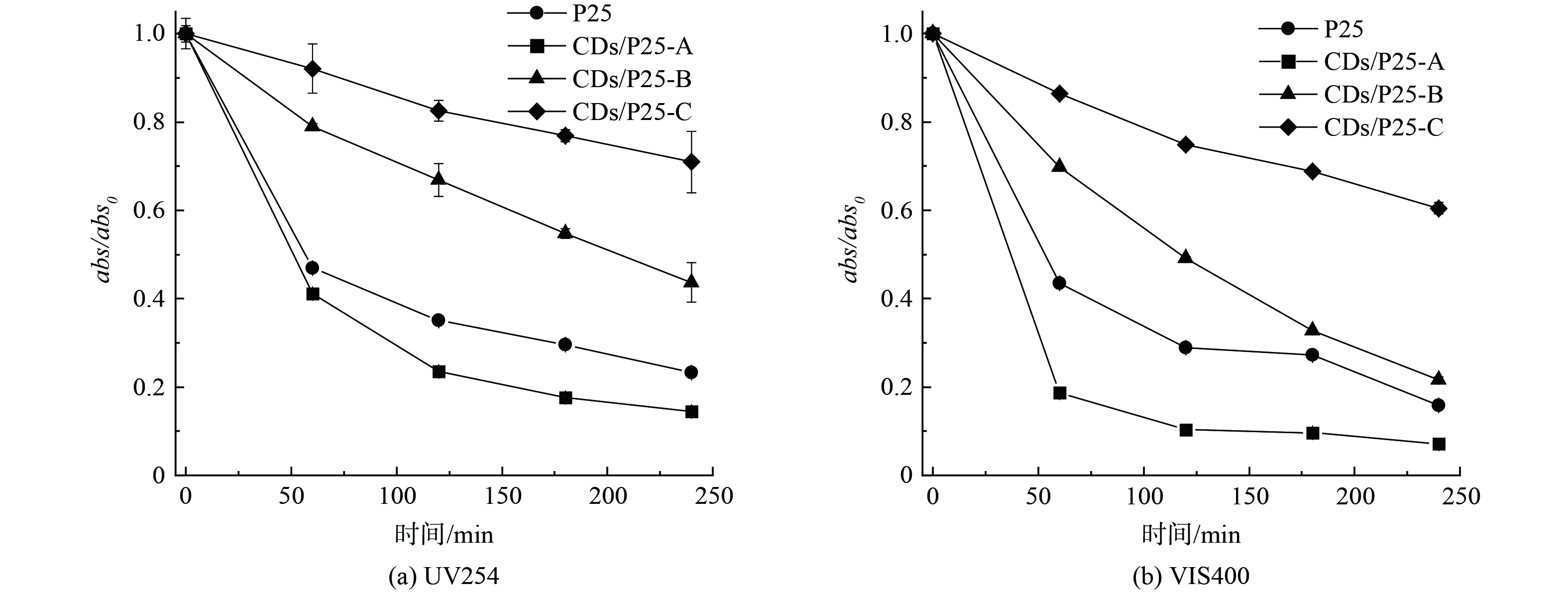
为研究各材料的光催化活性,将其投加到浓度为50 mg·L−1的腐殖酸溶液中,光催化时长为240 min。图1是3种复合材料的光催化性能。CDs/P25-A、CDs/P25-B、CDs/P25-C催化剂UV254去除率依次是71.2%、56.3%和29.0%;VIS400去除率为94.3%、78.4%和39.6%。3者中CDs/P25-A表现出稳定最优的光催化性能。综上所述,本实验选择CDs/P25-A作为后续表征和机理研究对象。
-
采用透射电子显微镜 (TEM) 放大105万倍对催化剂进行形貌分析。图2显示了CDs/P25的TEM图像。通过Digital Micrograph对图像进行处理分析,可以看到样品显示出很好的晶格条纹。0.313 nm的晶格条纹间距为对应于锐钛矿的 (211) 晶面 (JCPDS card no. 99-0008) ;而0.350 nm的晶格条纹对应于金红石的 (221) 晶面 (JCPDS card no. 21-
1276 ) ;此外还有石墨的 (100) 晶面 (JCPDS card no. 41-1487 ) [22]。进一步采用能谱仪 (EDS) 放大800倍进行元素面扫,结果表明CDs/P25中Ti (粉色) 、O (蓝色) 、C (黄色) 、N (绿色) 4种元素均匀的分布于材料中,其中C 和N元素分别来自于碳点水热合成过程中碳源一水柠檬酸和氮源氨水。综上所述,碳点已成功复合到二氧化钛表面中 [23-24]。通过测定Zeta电位来对比CDs/P25体系的稳定性。结果显示,CDs/P25在纯水中Zeta电位为−38.43 mV,在腐殖酸溶液中为−30.10 mV,这表明CDs/P25体系颗粒之间吸引力小于斥力,稳定性较好[25]。P25和CDs/P25的基本性质如表2所示。其中CDs/P25总孔容为0.31 cm3·g−1,平均孔径为0.72 nm,说明CDs/P25复合材料是以介孔孔道结构为主。从表2可以得出CDs/P25的比表面积 (BET) 为91.02 m2·g−1,而P25的比表面积为89.07 m2·g−1,XUE等[26]发现较大的比表面积有利于腐殖酸吸附于光催化剂表面,增加光催化反应速率[27]。结合图1的光催化性能,CDs/P25的光催化性能优于P25,因此CDs/P25略有增加的比表面积可能与光催化活性提高之间有关系。
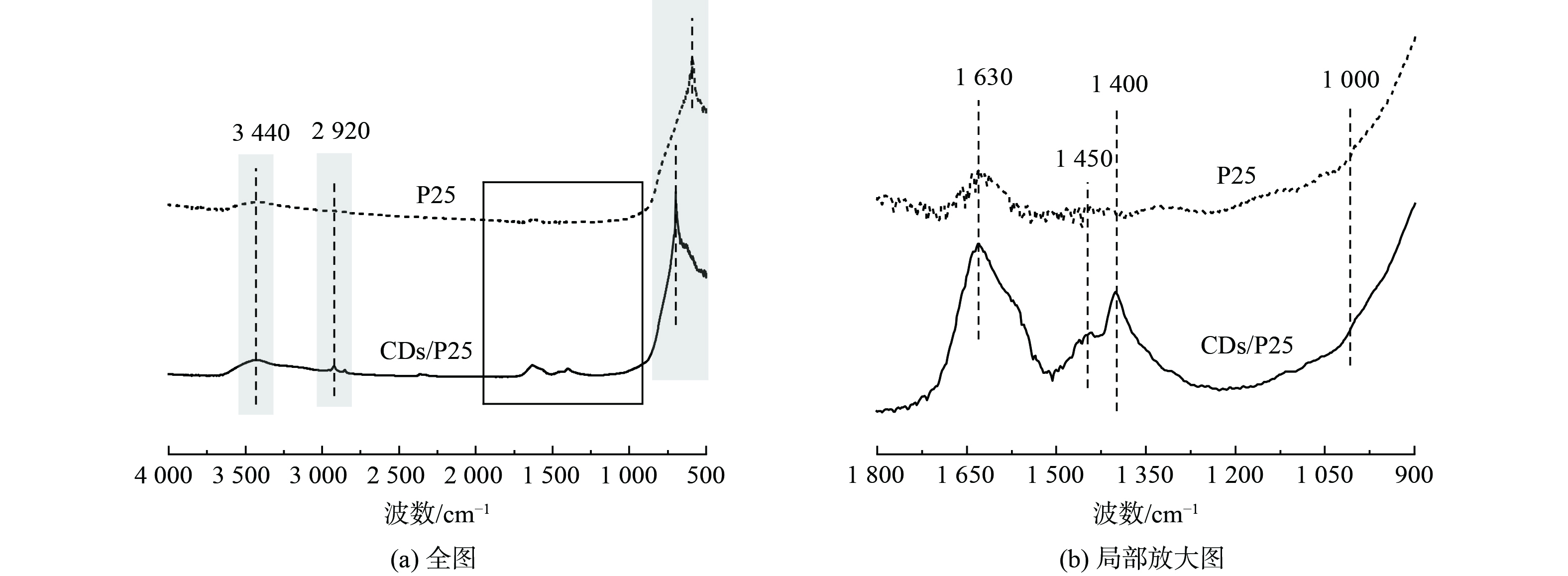
2种催化剂的红外 (FTIR) 分析结果如图3所示。在3 440 cm−1处观察到的吸收峰对应于表面吸附水,而CDs/P25中2 920 cm−1处的峰对应于C-H伸缩震动。进一步对比CDs/P25复合材料与P25的谱图发现,在复合材料中均可以观察到与P25相似的特征吸收峰,说明P25性质稳定,在复合材料中没有发生明显的结构变化。进一步放大900~1 800 cm−1段的红外光谱图,从放大图可以看到1 450、1 440 cm−1处的峰是CDs/P25中C-N=和C-O-C的伸缩振动[17],而1 637 cm−1处吸收峰是催化剂中游离水H-O-H键的弯曲振动。CDs/P25复合材料的红外谱图中可同时观察到属于CDs和TiO2的特征吸收峰,表明经水热处理后2者间成功复合[22],形成的化学键便于界面电子的转移。
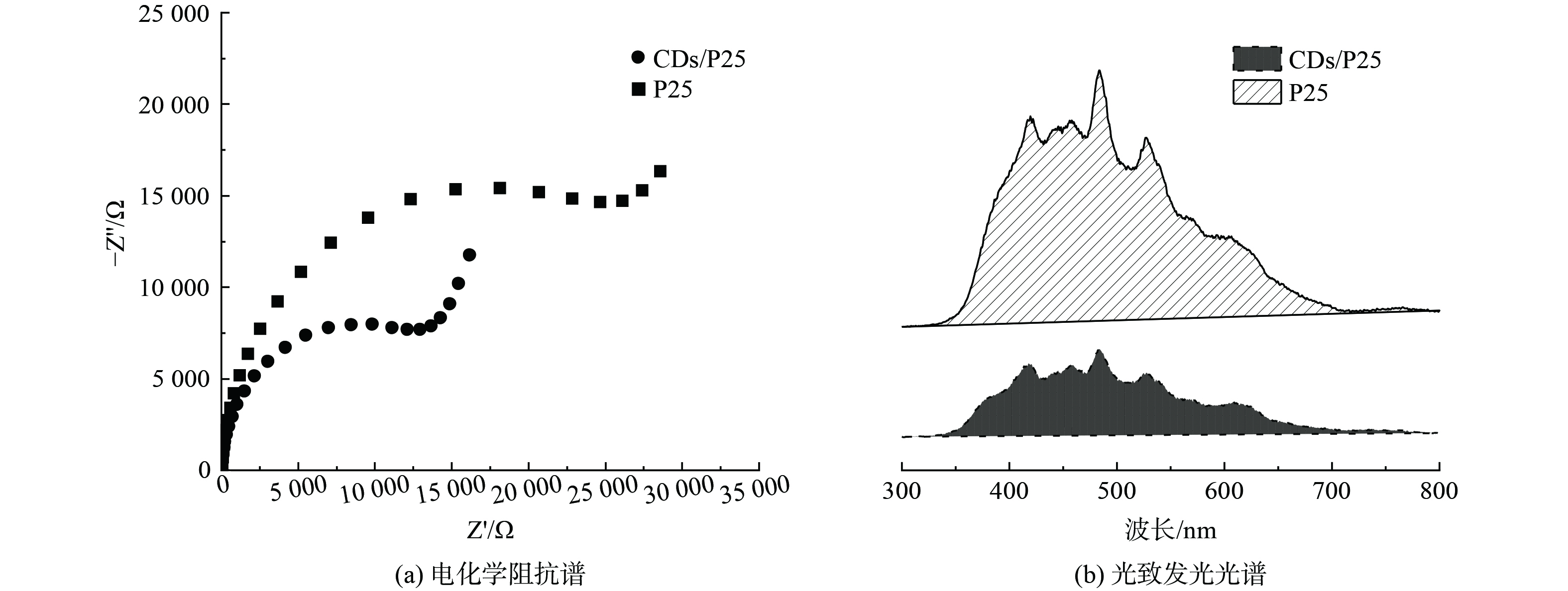
通过电化学阻抗谱 (EIS) 分析,测试催化剂电荷转移的特性。从图4奈奎斯特图中可以看出,CDs/P25复合材料的圆弧半径小于P25,表明其具有更低的电荷转移电阻,可以导致更快的电荷转移速率。通过光致发光光谱可得,CDs/P25复合材料的荧光光谱峰值强度明显低于P25,这表明CDs的引入促进了P25电荷分离增强、复合降低[28]。综上,电化学阻抗谱与光致发光光谱的测试结果一致说明碳点复合材料电荷转移能力增强,利于促进光催化反应的进行[29]。
-
CDs/P25复合材料降解不同浓度腐殖酸的结果表明,随着腐殖酸浓度的增加,去除率呈现先增大后减小的趋势 (图5(a)) 。UV254去除率在腐殖酸低浓度25 mg·L−1和高浓度200 mg·L−1时较低不足19%,中间浓度50、100和150 mg·L−1去除率分别提高为71.2%、81.6%和76.3%。而在VIS400中,当腐殖酸浓度由25 mg·L−1增至50 mg·L−1时,腐殖酸的去除率从41.1%增加至94.3%。而当腐殖酸浓度由50 mg·L−1进一步增加到150 mg·L−1时,去除率提高有限为97.2%。当腐殖酸浓度提高到200 mg·L−1时,降解效果衰减至66.4%。
为了进一步评估复合材料降解性能,利用一级动力学模型拟合光催化反应过程,得到不同浓度条件下的速率常数k。动力学方程如式(1)所示。
式中:abs和abs0分别代表腐殖酸溶液UV254和VIS400任意时刻的吸光度和初始时刻的吸光度;k为反应的一级速率常数,min−1;t为光催化反应时间,min。由图5(b)可知降解反应遵循一级反应动力学方程,满足线性关系,反应速率常数随初始浓度的增加呈现先增后减的趋势。CDs/P25在腐殖酸浓度为100 mg·L−1时,光催化反应VIS400的速率常数为1.53×10−2 min−1,是25 mg·L−1和200 mg·L−1的5.6倍和3.1倍。
导致这种现象的主要原因是低浓度时催化剂吸附的腐殖酸有限,光催化产生的活性氧与腐殖酸发生反应的概率低,不利于腐殖酸的降解 [30]。随着腐殖酸浓度增加催化剂活性位点利用率提高,逐渐表现出更优的光催化活性;而高浓度下已吸附的腐殖酸会与溶液中的腐殖酸以及中间产物互相排斥竞争吸附位点[31],腐殖酸浓度越高中间产物的浓度也越高,阻碍了腐殖酸向催化剂表面的传质[32];同时产生活性氧的数目有限,腐殖酸与之碰撞发生反应的概率减小[33-34],使得CDs/P25吸附作用减弱去除率下降。此外随着腐殖酸浓度的进一步增加,溶液色度不断升高,对光线的吸收也会增大,对反应体系的透光率造成影响,遮挡了光源对溶液内部的照射,阻碍光生载流子的激发,从而导致其降解腐殖酸效果下降 [35-36]。
-
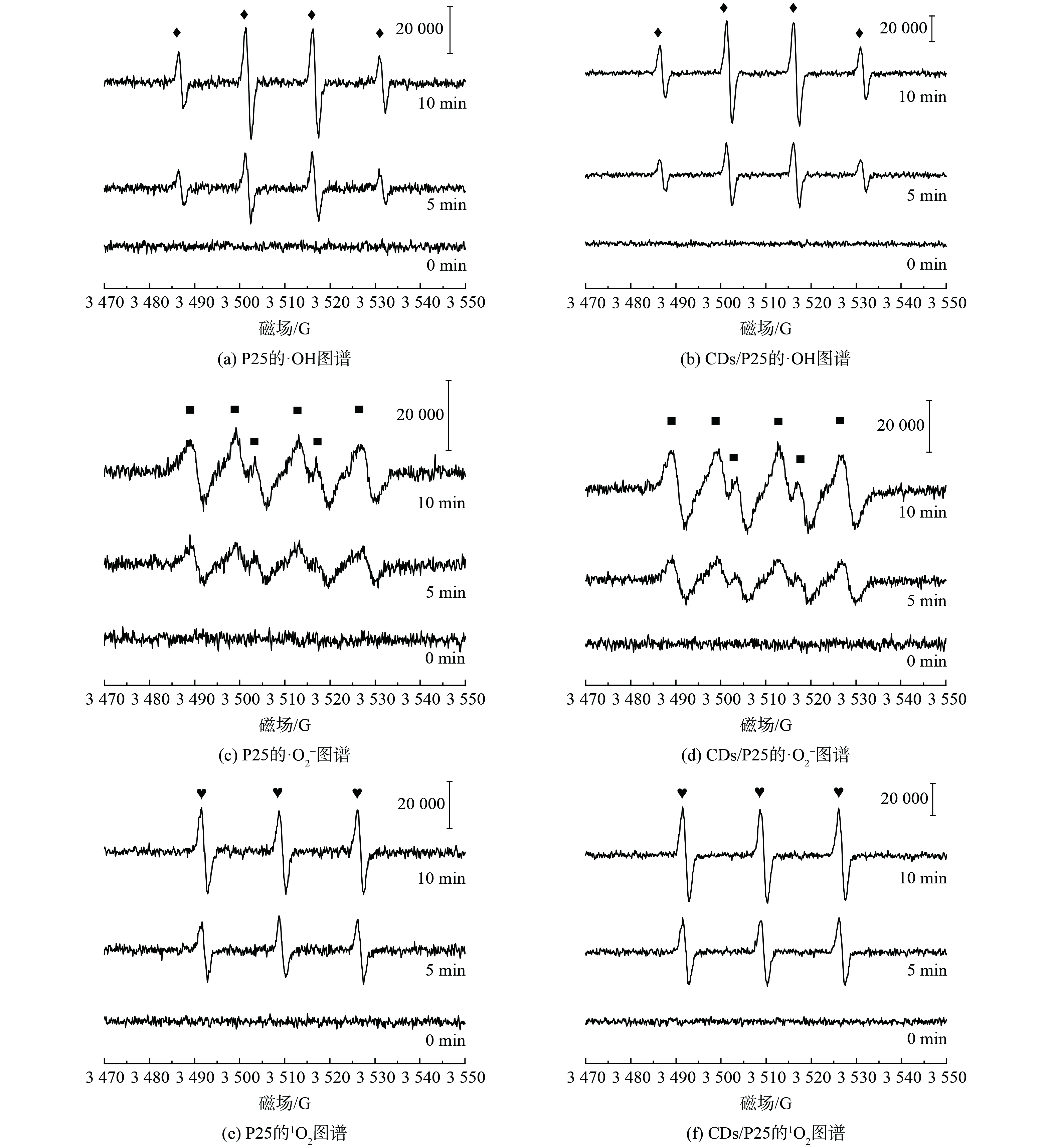
为了评估活性氧对腐殖酸降解的贡献,将CDs/P25与P25分别投加到50 mg/L的腐殖酸溶液中,使用TEMP和DMPO分别在黑暗、光照5 min和光照10 min进行光催化过程活性物种检测[37],结果如图6所示。暗反应过程中两种催化剂均无特征峰出现,说明在无光的情况下催化剂不会产生活性氧。而光照5 min后,出现·OH的1∶2:2∶1的特征峰、·O2−的六重峰以及1O2的1∶1∶1的等高峰,且随着反应时间延长活性氧信号强度均有增加,说明催化剂在光的激发下持续不断产生活性物种。CDs/P25的活性氧强度在光催化初期5~10 min时始终高于P25。综上可知,·OH、·O2−和1O2在腐殖酸降解催化反应中起关键作用,是CDs/P25光催化活性的主要来源[38]。
为了研究腐殖酸光催化降解的途径,通过LC-MS分析确定反应中间体和产物,结果如图7所示。腐殖酸是一种主要以酚羟基、羧基、酮基等含氧基团,氨基等含氮基团为苯环取代基的复杂有机物,分析结果表明P25暗反应60 min中生成壬酸、棕榈酸、硬脂酸等物质,而CDs/P25在上述产物基础上还能生成己二酸。开始光催化后中间产物在活性氧物种开环断键作用下继续降解[39],光反应120 min时CDs/P25产物主要为己内酰胺、辛酸等,P25需要光反应240 min才生成己内酰胺。光催化4 h后腐殖酸降解为甜菜碱、磷酸乙酯和二异丙基乙胺等物质[40]。
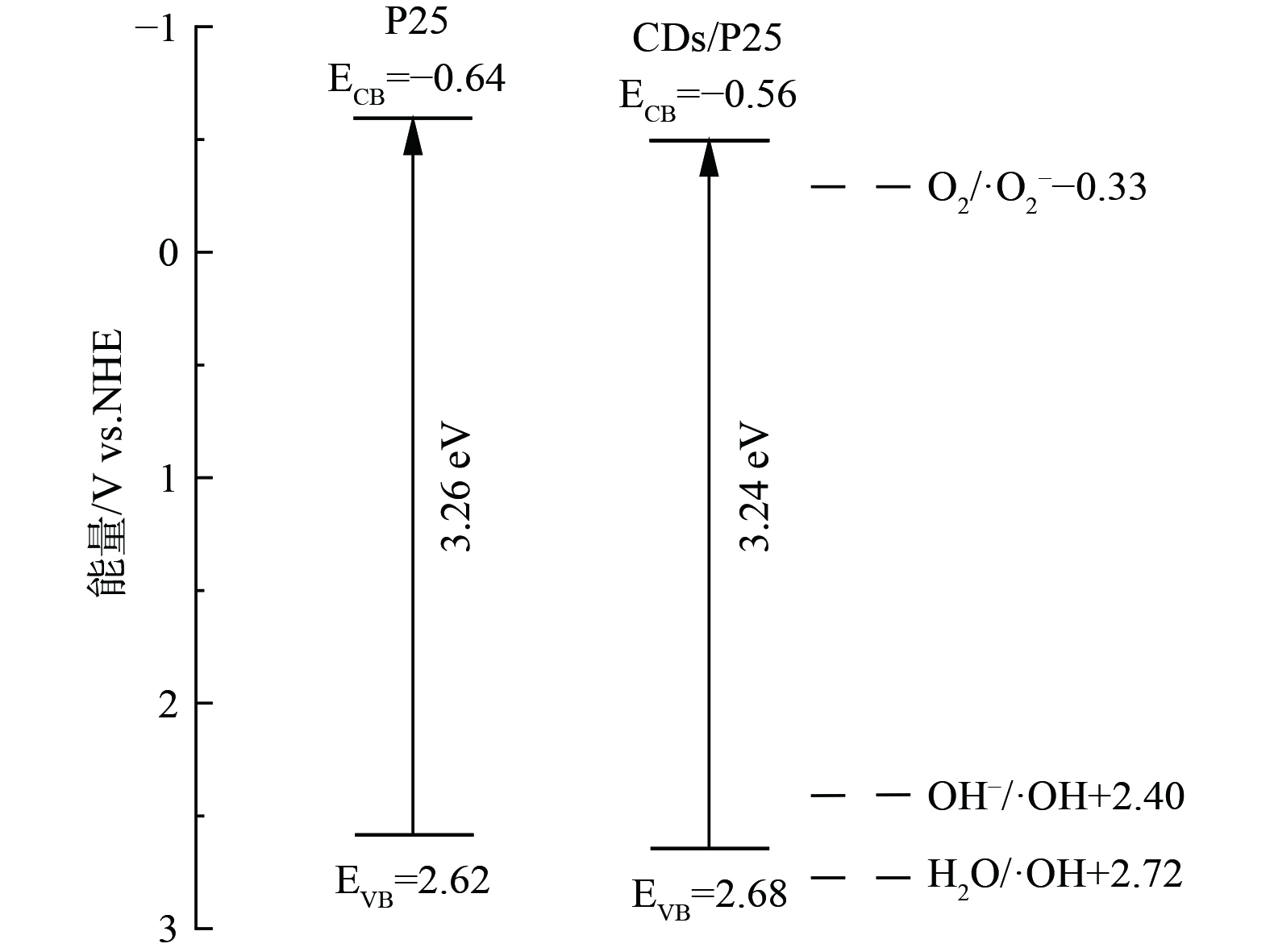
基于以上分析,图8呈现了CDs/P25复合材料提高光催化降解腐殖酸活性的机制。相比于P25 (Eg=3.26 eV) ,CDs/P25的禁带宽度 (Eg=3.24 eV) 变窄,表明CDs/P25增强了光吸收范围,更容易受光激发。同时CDs/P25的价带 (EVB=2.68 eV) 比P25的价带 (EVB=2.62 eV) 能级高,表明CDs/P25复合材料的氧化能力越强。在可见光照射下,CDs/P25材料后,P25价带上的电子被激发跃迁到导带上,在价带上留下光生空穴。由于碳点优良的电子转移能力,P25导带电子可以自发移动到碳点的导带上,使得电子空穴对有效分离避免复合。随后,光生电子迁移到催化剂表面捕捉水中的氧产生超氧自由基;价带空穴会与水生成羟基自由基,与超氧自由基反应生成单线态氧,在这些自由基的氧化还原作用下可以有效降解腐殖酸。由此可见,碳点作为电子的传输通道[41-42],极大地提高了复合材料的光催化降解性能。
腐殖酸各浓度的降解情况如图9所示,可以得到腐殖酸降解率、降解量与浓度的关系均表现为先上升后下降。UV254中腐殖酸浓度为25、200 mg·L−1时,降解率仅为17.4%和18.2%,当腐殖酸初始浓度从25 mg·L−1提高到50 mg·L−1时降解率显著提高,而初始浓度从50 mg·L−1提高到100 mg·L−1时,降解率增长减缓,继续增加腐殖酸初始浓度为150 mg·L−1,降解率略有降低,当浓度为200 mg·L−1时,降解率急剧下降。VIS400中随着初始浓度的升高,腐殖酸降解量呈现不断增大趋势,在初始浓度为为150 mg·L−1时降解量达到146 mg·L−1;而初始浓度为200 mg·L−1时,降解量仅为133 mg·L−1。这是因为腐殖酸浓度过高阻挡入射光的透射能力,影响催化剂对光的吸收能力,加之产生光生载流子的数量有限的不足以降解腐殖酸[24],进而限制光催化效率。比较UV254与VIS400,后者在降解率与降解量均高于前者,表明腐殖酸发色基团更容易去除。
-
1) 通过水热法合成碳点复合材料,当催化剂用量0.5 g·L−1,腐殖酸浓度为50 mg·L−1,CDs/P25比未改性的P25可见光下光催化性能提高1.6倍。原因是碳点的复合导致P25电子能量结构发生了显著变化,表现为带隙变窄,拓宽可见光吸收范围,改善电子空穴分离,增强界面电荷分离转移。未来可进一步优化复合材料合成条件。
2) CDs/P25复合材料的降解效果随着腐殖酸浓度升高而变化,其中腐殖酸的初始浓度为50~100 mg·L−1时,复合材料活性逐渐达到98%;100~200 mg·L−1有下降趋势。ln(abs/abs0)与降解时间t的拟合曲线为直线,且线性关系较好,在初始浓度为100 mg·L−1一级速率常数为1.53×10−2 min−1。
3) CDs/P25复合材料协同降解体系可以产生多个活性物种 (·OH、·O2−和1O2) 共同参与腐殖酸的降解,通过暗反应和光反应两个阶段对腐殖酸进行开环断键,较改性前的P25更快生成己内酰胺等小分子物质,最终主要产物为甜菜碱、磷酸乙酯、二异丙基乙胺等。
碳点复合材料光催化降解腐殖酸的机制
Mechanism of photocatalytic degradation of humic acid by carbon dots composite materials
-
摘要: 腐殖酸分子结构复杂、活性基团丰富,可通过离子交换或络合引发环境安全隐患。针对腐殖酸难以有效彻底去除的问题,采用碳点复合材料 (CDs/P25) 光催化技术实现了高效降解。通过模拟太阳光光催化实验研究了水热合成条件、腐殖酸浓度对复合材料降解腐殖酸性能的影响。实验结果表明,当碳点负载量为0.2 mol·L−1、pH为6,水热合成温度160 ℃、水热合成4 h时,复合材料光催化活性较好。通过红外光谱和能谱分析,验证碳点已成功负载于二氧化钛表面。光电化学测试结果表明,引入碳点后可提升二氧化钛光生载流子转移能力。同时探究了不同腐殖酸浓度下复合材料的光催化活性,在碳点复合材料投加量为0.5 g·L−1时、浓度为100 mg·L−1时腐殖酸去除率可达97%;机理分析表明碳点复合材料通过生成·OH、·O2−及1O2活性氧物种,将腐殖酸以开环断键的方式比二氧化钛更快生成己内酰胺等更多的小分子物质。该研究结果可为新型高效光催化体系的开发及其在环境污染控制领域的应用提供参考。Abstract: Humic acids contain complex molecular structures and abundant active groups, which can cause environmental safety hazards through ion exchange or complexation. To solve the problem that humic acid is difficult to effectively and ultimately remove, carbon dots composite material (CDs/P25) photocatalytic technology was used to achieve efficient degradation. The effects of hydrothermal synthesis conditions and humic acid concentration on the degradation of humic acid in composites were studied by simulated solar photocatalytic experiments. The experimental results showed that when the carbon dot loading was 0.2 mol·L−1, pH was 6, hydrothermal synthesis temperature was 160 ℃, and hydrothermal synthesis time was 4 hours, the composite material had better photocatalytic activity. The infrared spectroscopy results showed that carbon dots have been loaded onto the surface of TiO2. The photoelectrochemical test results indicated that decorating carbon dots can enhance the separation ability of photogenerated carriers in TiO2 and accelerate the transfer of electron-hole pairs. Moreover, the photocatalytic activity of CDs/P25 was compared under different humic acid concentrations. The results showed that 97% humic acid was removed under 4 hours of visible light irradiation, with 0.5 g·L−1 of CDs/P25 dosage and an initial humic acid concentration of 100 mg·L−1. The main active species in the CDs/P25 photocatalytic reaction system are ·OH, ·O2−, and 1O2. Humic acids were degraded mostly by opening-ring reactions and chemical bond-breaking reactions. The analysis of LC-MS revealed that CDs/P25 faster degraded humic acids to small molecule substances (i.e., caprolactam) compared to the TiO2. This study can help develop new and efficient photocatalytic systems for humic acids, facilitating applications in environmental pollution control.
-
Key words:
- carbon dots /
- photocatalysis /
- humic acid /
- titanium dioxide /
- active oxygen species
-

-
表 1 CDs/P25合成条件
Table 1. Synthesis conditions of different CDs/P25
样品 碳点负载量/
(mol·L−1)pH 水热温度/
°C水热时间/
hCDs/P25-A 0.2 6 160 4 CDs/P25-B 0.2 8 200 6 CDs/P25-C 0.4 6 200 6 表 2 P25和CDs/P25的物理性质
Table 2. Physical characteristics of P25 and CDs/P25
样品 比表面积/
(m2·g−1)Langmuir
表面积/(m2·g−1)总孔容/
(cm3·g−1)平均
孔径/nm平均
粒径/nmP25 89.07 571.59 0.33 0.63 20.00 CDs/P25 91.02 552.53 0.31 0.72 19.69 -
[1] ALI M, AWAN F U R, ALI M, et al. Effect of humic acid on CO2-wettability in sandstone formation[J]. Journal of Colloid and Interface Science, 2021, 588: 315-325. doi: 10.1016/j.jcis.2020.12.058 [2] SUDOH R, ISLAM M S, SAZAWA K, et al. Removal of dissolved humic acid from water by coagulation method using polyaluminum chloride (PAC) with calcium carbonate as neutralizer and coagulant aid[J]. Journal of Environmental Chemical Engineering, 2015, 3(2): 770-774. doi: 10.1016/j.jece.2015.04.007 [3] ŠíR M, PODHOLA M, PATOČKA T, et al. The effect of humic acids on the reverse osmosis treatment of hazardous landfill leachate[J]. Journal of Hazardous Materials, 2012, 207-208: 86-90. doi: 10.1016/j.jhazmat.2011.08.079 [4] 赵凯, 杨春风, 孙境求, 等. 电絮凝─超滤协同去除水中的腐殖酸[J]. 环境工程学报, 2017, 11(7): 3965-3970. doi: 10.12030/j.cjee.201605058 [5] 王文东, 张轲, 范庆海, 等. 紫外辐射对腐殖酸溶液理化性质及其混凝性能的影响[J]. 环境科学, 2016, 37(3): 994-999. [6] WANG J, LI H R, LI Y H, et al. Speciation, distribution, and bioavailability of soil selenium in the Tibetan Plateau Kashin–Beck disease area—a case study in Songpan County, Sichuan Province, China[J]. Biological Trace Element Research, 2013, 156(1-3): 367-375. doi: 10.1007/s12011-013-9822-5 [7] ZHU R C, DIAZ A J, SHEN Y, et al. Mechanism of humic acid fouling in a photocatalytic membrane system[J]. Journal of Membrane Science, 2018, 563: 531-540. doi: 10.1016/j.memsci.2018.06.017 [8] LI S, YANG Y L, ZHENG H S, et al. Advanced oxidation process based on hydroxyl and sulfate radicals to degrade refractory organic pollutants in landfill leachate[J]. Chemosphere, 2022, 297: 134214. doi: 10.1016/j.chemosphere.2022.134214 [9] OSKOEI V, DEHGHANI M H, NAZMARA S, et al. Removal of humic acid from aqueous solution using UV/ZnO nano-photocatalysis and adsorption[J]. Journal of Molecular Liquids, 2016, 213: 374-380. doi: 10.1016/j.molliq.2015.07.052 [10] YE W Y, LIU H W, JIANG M, et al. Sustainable management of landfill leachate concentrate through recovering humic substance as liquid fertilizer by loose nanofiltration[J]. Water Research, 2019, 157: 555-563. doi: 10.1016/j.watres.2019.02.060 [11] BYRNE C, SUBRAMANIAN G, PILLAI S C. Recent advances in photocatalysis for environmental applications[J]. Journal of Environmental Chemical Engineering, 2018, 6(3): 3531-3555. doi: 10.1016/j.jece.2017.07.080 [12] RAJCA M, BODZEK M. Kinetics of fulvic and humic acids photodegradation in water solutions[J]. Separation and Purification Technology, 2013, 120: 35-42. doi: 10.1016/j.seppur.2013.09.019 [13] WANG J Q, WANG Z H, WANG W, et al. Synthesis, modification and application of titanium dioxide nanoparticles: a review[J]. Nanoscale, 2022, 14(18): 6709-6734. doi: 10.1039/D1NR08349J [14] YANG H Y, ZHOU J Y, DUAN Z J, et al. Amorphous TiO2 beats P25 in visible light photo-catalytic performance due to both total-internal-reflection boosted solar photothermal conversion and negative temperature coefficient of the forbidden bandwidth[J]. Applied Catalysis B: Environmental, 2022, 310: 121299. doi: 10.1016/j.apcatb.2022.121299 [15] TIAN J, LENG Y H, ZHAO Z H, et al. Carbon quantum dots/hydrogenated TiO2 nanobelt heterostructures and their broad spectrum photocatalytic properties under UV, visible, and near-infrared irradiation[J]. Nano Energy, 2015, 11: 419-427. doi: 10.1016/j.nanoen.2014.10.025 [16] ZHAO Z, REISCHAUER S, PIEBER B, et al. Carbon dot/TiO2 nanocomposites as photocatalysts for metallaphotocatalytic carbon–heteroatom cross-couplings[J]. Green Chemistry, 2021, 23(12): 4524-4530. doi: 10.1039/D1GC01284C [17] LI Y R, LIU Z M, WU Y C, et al. Carbon dots-TiO2 nanosheets composites for photoreduction of Cr(VI) under sunlight illumination: Favorable role of carbon dots[J]. Applied Catalysis B: Environmental, 2018, 224: 508-517. doi: 10.1016/j.apcatb.2017.10.023 [18] SHEN S, CHEN K L, WANG H B, et al. Construction of carbon dots-deposited TiO2 Photocatalysts with visible-light-induced photocatalytic activity for the elimination of pollutants[J]. Diamond and Related Materials, 2022, 124: 108896. doi: 10.1016/j.diamond.2022.108896 [19] ALTMANN J, MASSA L, SPERLICH A, et al. UV254 absorbance as real-time monitoring and control parameter for micropollutant removal in advanced wastewater treatment with powdered activated carbon[J]. Water Research, 2016, 94: 240-245. doi: 10.1016/j.watres.2016.03.001 [20] CHEN W M, LI Q B. Elimination of UV-quenching substances from MBR- and SAARB-treated mature landfill leachates in an ozonation process: A comparative study[J]. Chemosphere, 2020, 242: 125256. doi: 10.1016/j.chemosphere.2019.125256 [21] KATSUMATA H, SADA M, KANECO S, et al. Humic acid degradation in aqueous solution by the photo-Fenton process[J]. Chemical Engineering Journal, 2008, 137(2): 225-230. doi: 10.1016/j.cej.2007.04.019 [22] ZHOU T S, LI L, LI J H, et al. Electrochemically reduced TiO2 photoanode coupled with oxygen vacancy-rich carbon quantum dots for synergistically improving photoelectrochemical performance[J]. Chemical Engineering Journal, 2021, 425: 131770. doi: 10.1016/j.cej.2021.131770 [23] SHEN S, WANG H B, FU J J. A nanoporous Three-dimensional graphene aerogel doped with a carbon quantum Dot-TiO2 composite that exhibits superior activity for the catalytic photodegradation of organic pollutants[J]. Applied Surface Science, 2021, 569. [24] XU L, BAI X, GUO L K, et al. Facial fabrication of carbon quantum dots (CDs)-modified N-TiO2-x nanocomposite for the efficient photoreduction of Cr(VI) under visible light[J]. Chemical Engineering Journal, 2019, 357: 473-486. doi: 10.1016/j.cej.2018.09.172 [25] AMINI TAPOUK F, PADERVAND S, YAGHMAEIAN K, et al. Synthesis of PAC-LaFeO3-Cu nanocomposites via sol-gel method for the photo catalytic degradation of humic acids under visible light irradiation[J]. Journal of Environmental Chemical Engineering, 2021, 9(4): 105557. doi: 10.1016/j.jece.2021.105557 [26] XUE G, LIU H, CHEN Q, et al. Synergy between surface adsorption and photocatalysis during degradation of humic acid on TiO2/activated carbon composites[J]. Journal of Hazardous Materials, 2011, 186(1): 765-772. doi: 10.1016/j.jhazmat.2010.11.063 [27] ZHANG H, LV X J, LI Y M, et al. P25-Graphene Composite as a High Performance Photocatalyst[J]. ACS Nano, 2010, 4(1): 380-386. doi: 10.1021/nn901221k [28] NI L F, WANG T, WANG H, et al. An anaerobic-applicable Bi2MoO6/CuS heterojunction modified photocatalytic membrane for biofouling control in anammox MBRs: generation and contribution of reactive species[J]. Chemical Engineering Journal, 2022, 429: 132457. doi: 10.1016/j.cej.2021.132457 [29] ZHANG J J, LIU Q R, WANG J H, et al. Facile preparation of carbon quantum dots/TiO2 composites at room temperature with improved visible-light photocatalytic activity[J]. Journal of Alloys and Compounds, 2021, 869: 159389. doi: 10.1016/j.jallcom.2021.159389 [30] MEHRABANPOUR N, NEZAMZADEH-EJHIEH A, GHATTAVI S, et al. A magnetically separable clinoptilolite supported CdS-PbS photocatalyst: Characterization and photocatalytic activity toward cefotaxime[J]. Applied Surface Science, 2023, 614: 156252. doi: 10.1016/j.apsusc.2022.156252 [31] PENG P, CHEN Z, LI X M, et al. Biomass-derived carbon quantum dots modified Bi2MoO6/Bi2S3 heterojunction for efficient photocatalytic removal of organic pollutants and Cr(VI)[J]. Separation and Purification Technology, 2022, 291: 120901. doi: 10.1016/j.seppur.2022.120901 [32] 马双念, 宋卫锋, 杨佐毅, 等. LaCoO3催化过一硫酸盐高效降解阿特拉津的性能及机理[J]. 环境工程学报, 2022, 16(10): 3266-3280. doi: 10.12030/j.cjee.202205045 [33] KHATAEE A, SADEGHI RAD T, NIKZAT S, et al. Fabrication of NiFe layered double hydroxide/reduced graphene oxide (NiFe-LDH/rGO) nanocomposite with enhanced sonophotocatalytic activity for the degradation of moxifloxacin[J]. Chemical Engineering Journal, 2019, 375: 122102. doi: 10.1016/j.cej.2019.122102 [34] 付权超, 许路, 刘沛华, 等. FeTiO2-x可见光活化过硫酸盐降解双酚A的作用机制[J]. 中国环境科学, 2023, 43(6): 2841-2852. doi: 10.3969/j.issn.1000-6923.2023.06.018 [35] 王菲凤. N掺杂TiO2纳米材料可见光催化性能及其降解水中腐殖酸[J]. 环境工程, 2017, 35(1): 6-10+58. [36] 冯宝瑞, 刘海成, 李阳, 等. Fe3O4@SiO2@TiO2-AC光催化降解水源水中腐殖酸[J]. 工业水处理, 2020, 40(8): 55-59+74. [37] CHEN P, WANG F, CHEN Z-F, et al. Study on the photocatalytic mechanism and detoxicity of gemfibrozil by a sunlight-driven TiO2/carbon dots photocatalyst: The significant roles of reactive oxygen species[J]. Applied Catalysis B: Environmental, 2017, 204: 250-259. doi: 10.1016/j.apcatb.2016.11.040 [38] HAMILTON J W J, BYRNE J A, DUNLOP P S M, et al. Evaluating the mechanism of visible light activity for N, F-TiO2 using photoelectrochemistry[J]. The Journal of Physical Chemistry C, 2014, 118(23): 12206-12215. doi: 10.1021/jp4120964 [39] CAI J B, LI H, FENG K, et al. Low-temperature degradation of humic acid via titanium zirconium oxide@copper single-atom activating oxygen: Mechanism and pathways[J]. Chemical Engineering Journal, 2022, 450: 138239. doi: 10.1016/j.cej.2022.138239 [40] WANG Q, WANG T, LAILA N, et al. Carbon dots/TiO2 enhanced visible light-assisted photocatalytic of leachate: Simultaneous effects and Mechanism insights[J]. Water Research, 2023, 245: 120659. doi: 10.1016/j.watres.2023.120659 [41] YU H J, ZHAO Y F, ZHOU C, et al. Carbon quantum dots/TiO2 composites for efficient photocatalytic hydrogen evolution[J]. Journal of Materials Chemistry A, 2014, 2(10): 3344. doi: 10.1039/c3ta14108j [42] SUI Y L, WU L, ZHONG S K, et al. Carbon quantum dots/TiO2 nanosheets with dominant (001) facets for enhanced photocatalytic hydrogen evolution[J]. Applied Surface Science, 2019, 480: 810-816. doi: 10.1016/j.apsusc.2019.03.028 -



 下载:
下载: