-
我国土壤和地下水六价铬(Cr(Ⅵ))污染问题突出。在地下水环境中,Cr主要以六价和三价(Cr(Ⅲ))形式存在,其中Cr(Ⅵ)通常以Cr2O72-、CrO42-和HCrO4−等含氧阴离子形式存在,迁移性强,毒性大[1-2];而Cr(Ⅲ)则主要以Cr3+、Cr(OH)2+、Cr(OH)2+和Cr(OH)3等阳离子或胶体沉淀形式存在,迁移性弱,毒性小。因此,地下水中Cr(Ⅵ)在含水介质上的吸附,或被还原为Cr(Ⅲ),均为Cr(Ⅵ)环境风险削减的重要天然途径。
在地下环境中,存在着大量金属氢氧化物(氧化物)和天然有机质,如无定形Al(OH)3和胡敏酸(HA)等,它们分别对Cr(Ⅵ)具有较强的吸附和还原能力。一方面,无定形Al(OH)3可通过静电引力、配体交换和颗粒内扩散等方式吸附Cr(Ⅵ)[3-4]。另一方面,HA表面的羧基能将通过吸附形成的离子交换态Cr(Ⅵ)络合,形成络合态Cr(Ⅵ),进而通过相邻的酚羟基和醇羟基等官能团将其还原为Cr(Ⅲ)[5]。但土壤和含水介质中的金属氢氧化物(氧化物)和天然有机质很少单独存在,在某些Eh或pH交替频繁的环境中(如水稻田、沼泽和泥炭地等)[6],常通过共沉淀作用形成有机矿质复合体,如HA-Al(Ⅲ)共沉物等[7-8]。Al(OH)3为无定形氢氧化物,易脱水形成三水铝石等晶质矿物[9],同时伴随比表面积和孔容的减小,进而影响水中污染物的界面反应过程。HA与Al(OH)3的结合会抑制复合体中的矿相转化过程,这势必会对Cr(Ⅵ)的吸附还原造成影响,但目前对其影响机理尚不明确。
在共沉淀过程中,有机碳与金属原子的摩尔比值(C/M比)是决定共沉物结构、理化性质和转化特征的决定性参数[6,10]。目前针对Al(Ⅲ)矿物的相关研究较少,但有关HA-Fe(Ⅲ)复合体方面的研究已有报道。相关研究表明,当C/M比<3时,Fe(Ⅲ)主要以水铁矿形式存在;当C/Fe比>3时,产物中矿物表面位点和孔隙几乎被完全堵塞,导致晶体结构的缺失,使得Fe(Ⅲ)主要以阳离子桥形式存在,此时零点电荷pH值(pHpzc)显著降低,这增强了复合体与Cr(Ⅵ)之间的静电斥力,不利于Cr(Ⅵ)的吸附[10]。又有研究表明,当C/M比≤1.9时,共沉淀态复合体呈现出典型的“核壳结构”,其核心为弱晶质的二线型水铁矿,壳层为有机质;当2.4≤C/M比≤8.1时,形成共边和共角的铁氧八面体,同时有Fe—C键形成;当C/M比≥11.5时,共边铁氧八面体消失,只形成共角铁氧八面体以及Fe—C键,此时Fe(Ⅲ)以单晶形式存在[11]。同时,前人通过HA-Fe(Ⅲ)共沉物的制备与光谱表征也发现了从“类矿物”到“类有机质”的结构转变,识别出共沉物发生结构突变的临界C/M比值约为3,即当Fe(Ⅲ)-HA共沉物C/M比<3时,Fe(Ⅲ)主要以水铁矿形式存在,呈现出“类矿物”特征;而当Fe(Ⅲ)-HA共沉物C/M>3时,Fe(Ⅲ)主要以阳离子桥或单晶形式存在,呈现出“类有机质”特征[12]。Al(Ⅲ)与Fe(Ⅲ)都是土壤和地下水中主要的金属离子,故推测Al(Ⅲ)-HA共沉淀过程中可能也具有与Fe(Ⅲ)类似的共沉淀特征,这导致在吸附还原Cr(Ⅵ)时,Al(Ⅲ)可能具有与Fe(Ⅲ)相似的影响,但由于二者理化性质不同,仍可能存在一定差异。目前对不同结构特征(C/M比)的HA-Al(OH)3共沉物的转化特征,及其对Cr(Ⅵ)吸附还原的影响机理尚不清楚,有待开展进一步研究。
本研究旨在探究不同C/M比HA-Al(Ⅲ)共沉物的转化产物对Cr(Ⅵ)的吸附还原机理,通过制备C/M比为1和15的HA-Al(Ⅲ)共沉物,分别模拟土壤和含水介质中的“类矿物”和“类有机质”结构的共沉物;以无定形Al(OH)3单体为对照,通过75℃水浴加热的方式得到具有不同转化进度的共沉物和Al(OH)3单体,以模拟不同地质历史时期形成的、具有不同转化进度的共沉物,并对各转化产物进行表征;进行上述Al(OH)3单体、共沉物及其转化产物对Cr(Ⅵ)的吸附还原实验,并探究不同转化进度共沉物对Cr(Ⅵ)的表面络合、颗粒内扩散吸附及还原特征;在此基础之上,分析转化前后不同C/M比共沉物的结构参数和Cr(Ⅵ)的吸附还原特征之间的相关关系,揭示共沉物转化进度对不同C/M比共沉物吸附还原Cr(Ⅵ)的影响及其主控机制。本研究有助于深入认识Cr(Ⅵ)在富铝和有机质的土壤及含水层中的迁移转化规律,也可为土壤地下水Cr(Ⅵ)污染控制修复材料的研发提供理论依据。
-
为了探究结构特征对于共沉物转化过程的影响,开展了预实验研究,设置了C/M比为1、2、5、10、15和20的HA-Al(Ⅲ)共沉物并进行表征,发现以C/M比等于5为界,HA-Al(Ⅲ)共沉物分别呈现出“类矿物”和“类有机质”结构特征。因此,本研究以C/M比分别为1和15的两种不同结构特征的共沉物作为代表,以无定形Al(OH)3单体作为对照,进行不同结构特征共沉物转化进度对Cr(Ⅵ)吸附还原的影响机理研究,具体实验方案如下。
-
本实验采用的氯化钙(CaCl2)、氢氧化钠(NaOH)、盐酸(HCl)、硫酸(H2SO4)、磷酸(H3PO4)、磷酸二氢钾(KH2PO4)、磷酸氢二钾(K2HPO4)、碳酸钠(Na2CO3)均购自北京化工厂,九水合硝酸铝(Al(NO3)3·9H2O)购自阿拉丁试剂有限公司,重铬酸钾(K2Cr2O7)购自天津市光复科技发展有限公司,二苯碳酰二肼购自天津市福晨化学试剂厂,上述试剂均为分析纯。丙酮为色谱纯,购自Honeywell公司。HA购自Sigma-Aldrich公司。
通过改变Al(Ⅲ)的浓度使得共沉物制备体系中液相HA的浓度始终维持为50 mg·L−1 C,使得实验浓度不超出地下水中天然有机质的实际浓度范围[12];共沉物体系pH值设置为6.0±0.1,以模拟有机质丰富的土壤和地下水的弱酸性环境[13]。具体的操作步骤如下[14]:先称取一定量的HA溶解于0.1 mol·L−1 NaOH溶液中,在磁力搅拌器上避光搅拌24 h,确保HA完全溶解,再逐滴滴加1 mol·L−1 HCl,将溶液pH值回调至7.0左右,得到HA储备液;利用总有机碳分析仪(PE 2400 Series II,PerkinElmer)测定HA储备液TOC浓度,再稀释指定倍数,得到50 mg·L−1 C HA使用液。在此基础之上,分别称取112.32 mg·L−1和5.62 mg·L−1的Al(NO3)3·9H2O溶解于1 L去离子水中,得到2种不同浓度的Al(Ⅲ)溶液,将Al(Ⅲ)溶液缓慢加入盛有HA溶液的烧杯中。待Al(Ⅲ)和HA溶液充分混合之后,使用0.1 mol·L−1 NaOH或HCl溶液将pH值调节至6.0±0.1,并在老化过程中每隔1 d测定一次pH值,并通过滴加0.1 mol·L−1 NaOH或HCl将溶液pH值回调至6.0±0.1,以保持反应条件稳定。由于在天然环境中Al(Ⅲ)矿物及其复合体的转化速率十分缓慢,因此本实验采用以往文献所报道的方法[15-17],将溶液通过水浴方式加热至75°C,从而加速其转化速率。
分别将经历了0、2、7、15、26 d转化后得到的实验组悬浊液移入离心瓶中,在3500 r·min−1条件下离心5 min,弃去上清液,并加入等量去离子水,用玻璃棒充分搅拌,洗去固体表面残留的NO3−等杂质离子,再次离心。重复3次上述水洗过程后,将得到的固体沉淀进行冷冻干燥和研磨,并过100目筛,即可得到不同转化进度的HA-Al(Ⅲ)共沉物。不同转化进度的共沉物记作RaDb(a为共沉物的C/M比,b为转化天数)。无定形Al(OH)3对照组样品制备方法同上,只是在制备过程中不添加HA。
本实验对不同C/M比HA-Al(Ⅲ)共沉物的理化性质和结构特征进行了表征,具体如下:采用ICP-OES(BLUE,德国斯派克公司)测定Al含量;采用元素分析仪(PE 2400 Series II,PerkinElmer)测定C含量;采用全自动比表面积、微孔孔隙和化学吸附仪(ASAP 2020M+C,美国Micromeritic公司)测定比表面积和孔容;采用X-射线衍射仪(D/max-rB,日本理学公司)测定矿物晶型和结晶程度;采用傅里叶变换红外光谱仪(Lumos,德国布鲁克公司)测定官能团类型。
-
Cr(Ⅵ)的平衡吸附还原实验条件如下:本实验设置4组平行样,初始Cr(Ⅵ)浓度为1 mmol·L−1,背景电解质为0.01 mol·L−1 CaCl2,平衡pH=5.0±0.1,固液比为1∶1000,反应温度为25 ℃,反应平衡时间为20 d。具体操作步骤[16]如下:称取20 mg不同C/M比HA-Al(Ⅲ)共沉物于20 mL棕色玻璃瓶中(排除光照影响),同时加入20 mL初始浓度为1 mmol·L−1的Cr(Ⅵ)溶液(含0.01 mol·L−1 CaCl2作为背景电解质)。共沉物中HA和无定形Al(OH)3均具有一定的pH值缓冲能力,故通过预实验确定反应体系中不同初始pH值和平衡pH值的对应关系,据此设置反应体系的初始pH值,以确保反应体系平衡pH值为5.0±0.1。将反应玻璃瓶置于25℃、175 r·min−1转速条件的水平恒温摇床(QYC-2102C,上海福玛实验设备有限公司)进行吸附实验,每隔一定反应时间后,将反应瓶取出,于3000 r·min−1条件下离心5 min,准确移取10 mL上清液,过0.45 μm聚醚砜滤膜[18-19],并采用二苯碳酰二肼分光光度法(DR6000,美国哈希公司)测定溶液中的Cr(Ⅵ)浓度(C1)。取其中1个平行样,离心分离出固体样品,并进行冷冻干燥,以备后续表征使用。
为了测定吸附在共沉物上Cr(Ⅵ)的形态,本实验采用了“分步解吸法”,具体原理如下:利用磷酸根对Cr(Ⅵ)阴离子的置换作用,确定表面络合态Cr(Ⅵ)的含量,利用高浓度NaOH和Na2CO3混合溶液对HA和Al(OH)3的溶解作用,确定颗粒内扩散态Cr(Ⅵ)的含量[17]。上述分步解吸体系依次为0.05 mol·L−1 K2HPO4+0.05 mol·L−1 KH2PO4和1 mol·L−1 NaOH+0.5 mol·L−1 Na2CO3溶液,解吸时间均为1 d。具体操作步骤如下:首先,向剩余三组平行样中加入10 mL 0.1 mol·L−1 K2HPO4+0.1 mol·L−1 KH2PO4溶液,置于摇床中于相同条件下进行首次解吸,1 d后取出样品,3000 r·min−1转速条件下离心5 min后,再次移取10 mL上清液,过0.45 μm聚醚砜滤膜后测定Cr(Ⅵ)浓度(C2);继而,向3个样品中加入10 mL 2 mol·L−1 NaOH+1 mol·L−1 Na2CO3溶液(CO32-用于络合背景溶液中Ca2+,从而消除其阳离子桥作用的影响[20])进行二次解吸,反应1 d后再次取出样品,过滤并测定Cr(Ⅵ)浓度(C3)。
-
基于本实验条件中Cr(Ⅵ)与共沉物之间的吸附和解吸动力学实验,不同反应时刻Cr(Ⅵ)的总去除量QT、总吸附量Qa(包括表面络合Qc和颗粒内扩散Qd)和总还原量Qr的单位均为mmol·g−1,具体计算公式如下:
其中,C0、C1、C2、C3分别表示液相中Cr(Ⅵ)的初始浓度、吸附反应后液相剩余的Cr(Ⅵ)浓度、磷酸盐体系解吸后液相中的Cr(Ⅵ)浓度、NaOH体系二次解吸后液相中的Cr(Ⅵ)浓度,单位均为mmol·L−1;V表示反应体系体积(0.02 L);m表示样品质量(0.02 g)。
-
“类矿物”(C/M比为1)和“类有机质”(C/M比为15)共沉物随转化时间的增加,转化进度不断提高,产物中的元素组成如表1所示。由表1可得,当转化时间从0 d增加到26 d时,“类矿物”共沉物中Al含量和C含量均随转化进度提高而逐渐上升,这可能是由于共沉物中无定形Al(OH)3逐渐脱水结晶,导致其中Al和C元素占比提高[11,21]。相较于无定形Al(OH)3单体,“类矿物”共沉物中Al含量的变化趋势与无定形Al(OH)3一致,但是变化幅度相对较小,推测是由于HA的存在阻碍了晶胞之间的结合,导致晶胞难以通过脱水方式结合形成大规模Al矿物晶体。而“类有机质”共沉物(C/M比为15)在转化过程中,Al含量和C含量均未发生显著变化,这可能是由于Al(Ⅲ)主要以阳离子桥或单晶形式存在,不具备发生晶型转化的条件。
-
不同结构共沉物26 d转化前后的比表面积与孔径分布如表2所示。转化前,C/M比为1(R1D0)的共沉物的比表面积和孔容与无定形Al(OH)3(R0D0)接近,具有“类矿物”共沉物特征;C/M比为15(R15D0)的共沉物的比表面积和孔容远小于无定形Al(OH)3(R0D0),具有“类有机物”共沉物特征。相较于无定形Al(OH)3单体,“类矿物”共沉物(C/M比为1)经转化后,比表面积和孔容均发生了显著衰减,它们的变化趋势与无定形Al(OH)3一致,但是变化幅度相对降小,再次说明HA抑制了“类矿物”共沉物中无定形Al(OH)3的转化速率。而“类有机质”共沉物转化前后的比表面积和孔容均未发生显著变化,可能是由于“类有机质”共沉物中HA含量较高,堵塞了大部分孔隙,使其初始比表面积和孔容很小,因此转化前后变化不明显。
-
转化前后不同结构HA-Al(Ⅲ)共沉物中矿物晶型与结晶程度的变化情况如图1所示。通过将转化前不同C/M比的HA-Al(Ⅲ)共沉物(R0D0、R0D0、R15D0)的XRD图与HA和无定形Al(OH)3的XRD光谱图进行对比,发现R1D0出现了R0D0(无定形Al(OH)3)的特征峰,且缺少HA光谱图的特征峰,具有“类矿物”共沉物特征;而R15D0与HA光谱图有相似的的特征峰,具有“类有机质”共沉物特征。
转化前无定形Al(OH)3单体的XRD光谱图(R0D0)中存在4个典型衍射峰,但强度整体偏低,峰宽较大,是无定型Al(OH)3的典型衍射峰,在图中用字母“A”进行标注[20]。转化26 d后,XRD光谱图(R0D26)中衍射峰的数量、位置、强度和峰宽均发生了改变,整体上可划分为两类衍射峰:一类峰宽较大,是拟薄水铝石的典型衍射峰[22](图1(e)),在图中用字母“B”进行标注;另一类峰宽较小,是三水铝石的典型衍射峰[22](图1(f)),在图中用字母“G”进行标注。这说明无定形Al(OH)3经转化后同时形成了拟薄水铝石和三水铝石矿物晶体。
与无定形Al(OH)3单体不同,共沉物转化产物类型受其结构特征影响。对于“类矿物”共沉物来说,转化26 d后样品的XRD光谱图(R1D26)仅呈现出了拟薄水铝石的典型特征,但并未检测到三水铝石特征峰的存在。从R0D26的XRD光谱图可以看到,拟薄水铝石的峰宽明显大于三水铝石,说明拟薄水铝石比三水铝石结晶程度差,这也是“类矿物”共沉物中仅转化形成了拟薄水铝石的原因,即共沉物中HA抑制了结晶程度更高的三水铝石的形成。而对于“类有机质”共沉物来说,转化前后样品的XRD光谱图均与HA谱图(图1(d))的特征峰峰形相似,并未发生明显变化,始终未检测到无定形Al(OH)3(R0D0)、拟薄水铝石(图1(e))和三水铝石(图1(f))等矿物的存在,因此推断“类有机质”共沉物中Al并不以无定形Al(OH)3形式存在,可能以阳离子桥或单晶形式存在,且未发生明显的矿物晶型转化。
-
转化前后不同结构HA-Al(Ⅲ)共沉物的FTIR光谱图如图2所示。与XRD光谱图相同,FTIR光谱图在转化前,R1D0多个特征峰与无定形Al(OH)3(R0D0)吻合,具有“类矿物”共沉物特征,而R15D0与HA谱图有相似的峰形,具有“类有机质”共沉物特征。无定形Al(OH)3的FTIR光谱图存在4个显著的吸收峰,分别位于1633、1386、1026、573 cm−1处,为无定形Al(OH)3的特征峰;而在转化26 d后,样品中FTIR光谱的吸收峰数量显著增加,其中3621、3526、3460 cm−1处的吸收峰与三水铝石的特征吸收峰吻合[23],进一步说明无定形Al(OH)3单体转化产物中含有三水铝石组分,这与XRD表征结果一致。
“类矿物”共沉物在转化前也具有无定形Al(OH)3的FTIR光谱特征吸收峰,但其转化产物中并未观察到位于3460—3621 cm−1处三水铝石的特征吸收峰,且573 cm−1处的Al—O伸缩振动峰蓝移至741 cm−1,指示了AlO4的形成,为拟薄水铝石的特征吸收峰[24-25],说明“类矿物”共沉物的转化产物未形成三水铝石,而是形成了拟薄水铝石,这一发现与XRD表征结果一致。而对于“类有机质”共沉物来说,转化前后共沉物样品的FTIR光谱图的峰形与HA相似,未观察到明显形态上的变化,说明该类共沉物转化进度较低,与XRD表征结果一致。此外,HA光谱图的特征峰主要位于1706 cm−1(自由羧基的C=O伸缩振动)、1594 cm−1(羰基中C=O键的伸缩振动)、1386 cm−1(CH3的变形振动)、1262 cm−1(酚类物质的C—O伸缩振动)、1095 cm−1和1033 cm−1(醇羟基的伸缩振动)处,而“类有机质”共沉物转化前后位于1706 cm−1处和1262 cm−1处的特征峰强度均显著降低,这可能是由于络合能力较强的羧基和醇羟基与Al(Ⅲ)形成了络合物所导致的,这进一步支撑了在“类有机质”复合体中Al(Ⅲ)可能主要以阳离子桥或单晶的形式存在的推断。
综上,不同结构HA-Al(Ⅲ)共沉物具有截然不同的转化特征,“类矿物”共沉物(C/M比为1)由于无定形Al(OH)3组分的存在,具有较强的不稳定性,在本研究实验条件下发生了显著转化,但相较于无定形Al(OH)3单体而言,HA的存在降低了共沉物中无定形Al(OH)3的转化速率,同时也改变了转化产物的矿物类型;而“类有机质”共沉物(C/M比为15)由于Al(Ⅲ)主要以阳离子桥或单晶形式存在,性质相对稳定,在本实验条件下几乎未发生矿物晶型转化。
-
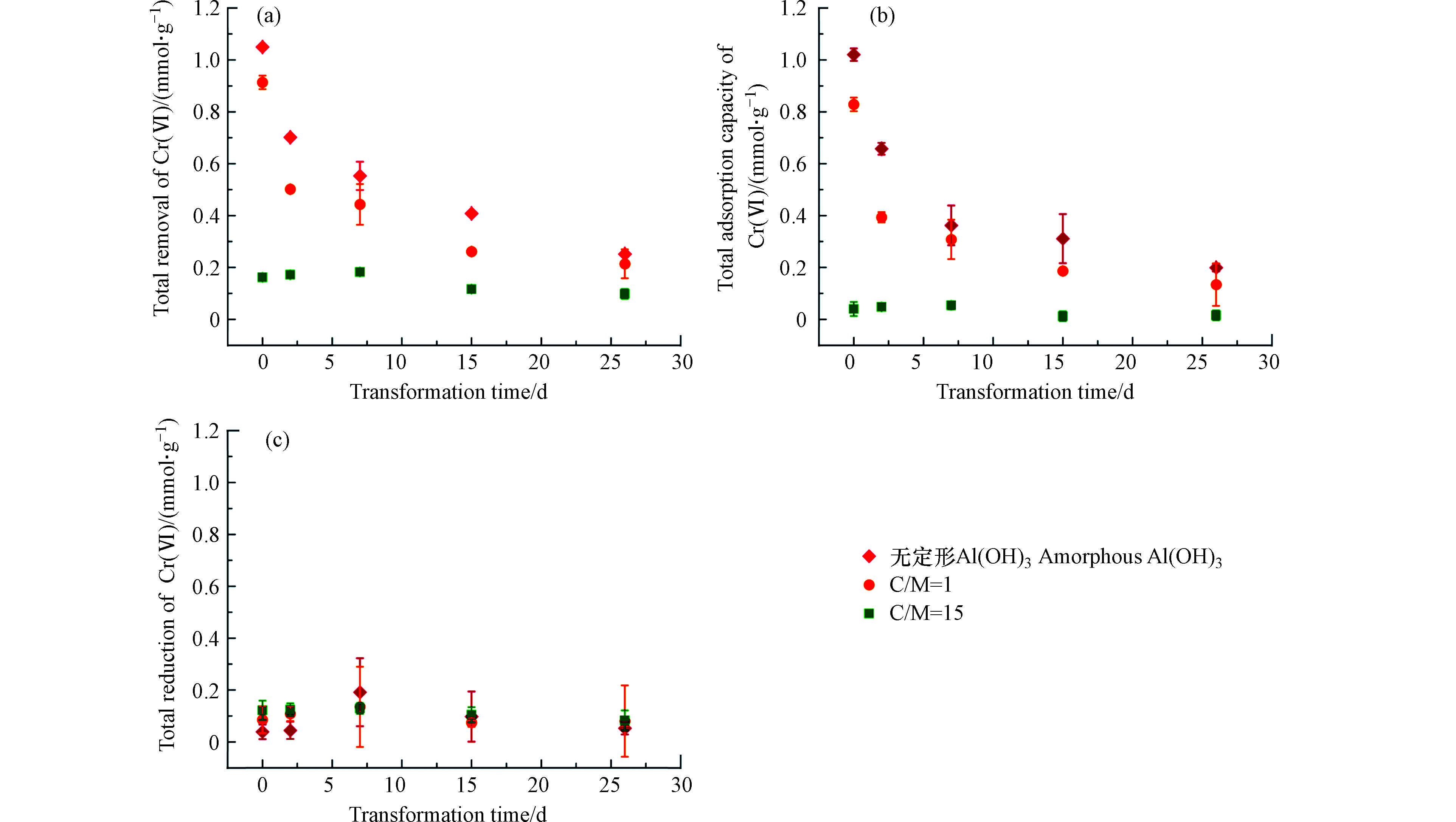
为了探究不同结构共沉物转化进度对Cr(Ⅵ)吸附还原的影响,采用不同结构和不同转化进度的共沉物样品,进行了Cr(Ⅵ)的平衡吸附还原实验,结果如图3所示。在转化时间从0 d增长至26 d的过程中,“类矿物”共沉物中Cr(Ⅵ)的总去除量从0.91 mmol·g−1降至0.21 mmol·g−1,总吸附量从0.82 mmol·g−1降至0.13 mmol·g−1,但总还原量始终维持在0.10 mmol·g−1左右,说明HA中作为电子供体的官能团几乎未受到转化过程的影响,但矿相转化却显著抑制了“类矿物”共沉物对Cr(Ⅵ)的吸附[26]。对于“类有机质”共沉物来说,不同转化产物对Cr(Ⅵ)的去除也包括吸附和还原两种途径,但以还原作用为主。此外,“类有机质”共沉物中HA完全抑制了Al(Ⅲ)的晶型转化,因此Cr(Ⅵ)的总吸附量和总还原量几乎不受转化进度的影响,始终保持在0.05 mmol·g−1和0.12 mmol·g−1左右。
-
为了进一步探明共沉物转化进度对Cr(Ⅵ)吸附机制的影响,本研究采用“分步解吸法”实现了对共沉物中表面络合态和颗粒内扩散态Cr(Ⅵ)的定量检测,结果如图4所示。由于共沉物中的无定形Al(OH)3具有多羟基和多孔的特征,在未发生转化的“类矿物”共沉物中,被吸附的Cr(Ⅵ)同时以表面络合态和颗粒内扩散态形式存在,且以表面络合态为主。
“类矿物”共沉物的转化产物上表面络合态和颗粒内扩散态Cr(Ⅵ)含量均发生了显著衰减,且颗粒内扩散态Cr(Ⅵ)含量的衰减速度更快,在经历2 d转化后,已检测不到颗粒内扩散态Cr(Ⅵ)的存在。随着转化进度进一步提高,“类矿物”共沉物只能通过表面络合作用吸附Cr(Ⅵ),且表面络合量随转化时间的延长逐渐减少。然而“类有机质”共沉物在转化前后,均只检测到少量的表面络合态Cr(Ⅵ),且表面络合量并未随转化时间的增加而发生显著衰减,说明Cr(Ⅵ)只能通过表面络合方式吸附在“类有机质”共沉物表面,且转化过程不影响其表面络合吸附量[27]。
-
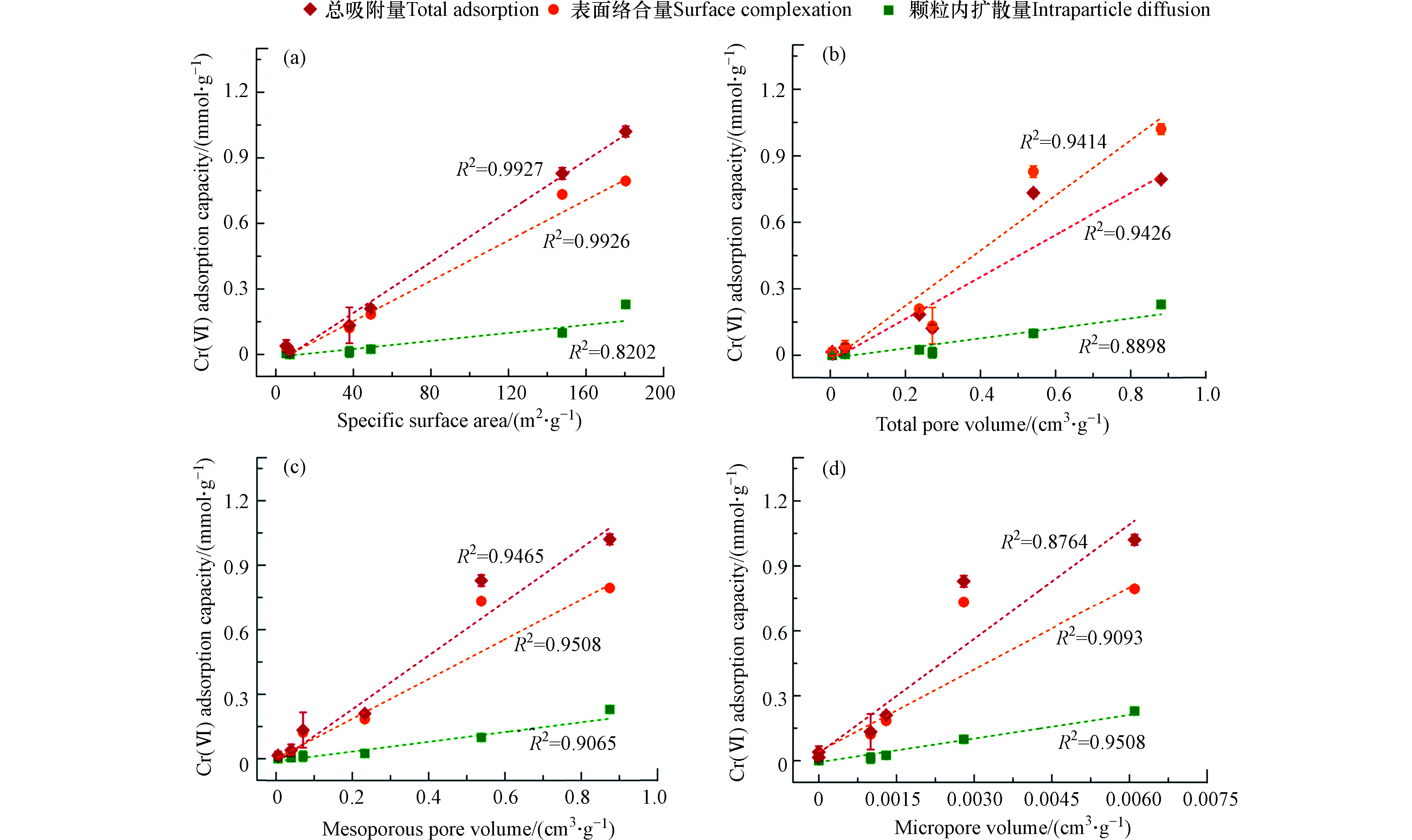
为了揭示共沉物转化进度对共沉物吸附还原Cr(Ⅵ)过程的主控机制,分析了不同C/M比共沉物和无定形Al(OH)3单体对Cr(Ⅵ)的吸附量与其比表面积和孔容之间的相关关系,结果如图5所示。Cr(Ⅵ)的总吸附量与比表面积呈强正相关关系(R2=0.9927),但与总孔容、介孔孔容之间的相关性相对较弱,R2介于0.8764至0.9465之间。按吸附机制区分,表面络合态Cr(Ⅵ)含量与共沉物比表面积呈强正相关关系(R2=0.9926)。相反,对于颗粒内扩散过程来说,颗粒内扩散量与比表面积之间的相关性相对较差(R2=0.8202),但与微孔孔容(R2=0.9488)和介孔孔容(R2=0.9065)之间均具有显著的正相关性。考虑到共沉物微孔孔容极低(<0.0061 cm3·g−1),仅占总孔容的0.69%,可知Cr(Ⅵ)颗粒内扩散过程主要受介孔孔容控制,而非比表面积。
综上,将不同C/M比共沉物转化进度对Cr(Ⅵ)吸附还原的影响机理归纳如下(见图6)。“类矿物”共沉物(C/M比为1)具有类似于无定形Al(OH)3的结构特征,其表面含有大量的羟基官能团,可以通过表面络合方式吸附Cr(Ⅵ);同时,其孔隙结构发育,可以通过颗粒内扩散方式吸附Cr(Ⅵ)。但是,随着转化进度的提高,“类矿物”共沉物中无定形Al(OH)3组分逐渐转化为结晶程度更高的拟薄水铝石,比表面积减小,表面络合位点数量随之减少,使得其对Cr(Ⅵ)的表面络合作用随之减弱;同时,孔容衰减至较低水平,使得转化产物无法再通过颗粒内扩散作用吸附Cr(Ⅵ)。而对于“类有机质”共沉物(C/M比为15)来说,由于高浓度HA抑制了Al3+的水解和结晶过程,使得Al(Ⅲ)主要以阳离子桥或单晶形式存在,共沉物不具有多孔结构,因此只能通过HA表面有机官能团微弱的表面络合作用吸附Cr(Ⅵ)。“类有机质”共沉物不含弱晶质Al(OH)3,结构较稳定,几乎不发生矿物晶型的转化。此外,共沉物的转化过程只与其中的Al(OH)3组分有关,HA组分作为反应体系中的唯一电子供体,在转化过程中几乎不受影响[5],这也是Cr(Ⅵ)还原量不受共沉物转化进度影响的原因所在。
-
本研究以C/M比等于1和15的两类具有不同结构特征的HA-Al(Ⅲ)共沉物为代表,对其转化产物进行了制备和表征,并开展了其对Cr(Ⅵ)的平衡吸附还原实验,主要得出以下结论与认识:
(1)“类矿物”共沉物(C/M比为1)易发生转化,比表面积和孔容均随转化进度的升高而不断减小,同时产物更倾向转化为拟薄水铝石;而“类有机质”共沉物(C/M比为15)中Al(Ⅲ)主要以阳离子桥或单晶形式存在,因此几乎不发生晶型转化。
(2)“类矿物”共沉物对Cr(Ⅵ)的去除主要通过吸附作用实现,其总吸附量随着转化进度的提高逐渐衰减,总还原量基本不受影响;“类有机质”共沉物对Cr(Ⅵ)的去除主要通过还原作用实现,总吸附量和总还原量几乎不受转化进度的影响。
(3)吸附过程中,“类矿物”共沉物上表面络合态和颗粒内扩散态Cr(Ⅵ)的量均随转化进度的提高而减少,且颗粒内扩散态Cr(Ⅵ)的量快速衰减至0。
(4)在共沉物及转化产物上的表面络合态Cr(Ⅵ)含量受比表面积控制;Cr(Ⅵ)在共沉物及转化产物上的颗粒内扩散过程与孔容有关,且主要受介孔孔容控制。
(5)由于晶型转化导致“类矿物”共沉物比表面积下降,孔容骤减,造成其对Cr(Ⅵ)的表面络合能力降低,且Cr(Ⅵ)也无法通过孔隙进入颗粒内部;而“类有机质”共沉物几乎不发生转化,产物结构相对稳定,加之HA组分作为反应体系中还原Cr(Ⅵ)的唯一电子供体,在转化过程中几乎不受影响,因此Cr(Ⅵ)的还原量基本保持不变。
不同C/M比HA-Al(Ⅲ)共沉物转化进度对其吸附还原Cr(Ⅵ)的影响机理
The Influence Mechanism of Transformation Extent of HA-Al(Ⅲ) Co-precipitate with Different C/M Ratio on Cr(Ⅵ) Adsorption and Reduction
-
摘要: HA-Al(Ⅲ)共沉物普遍存在于土壤和含水层中,对地下水中的Cr(Ⅵ)具有较强的吸附和还原能力。共沉物中的无定形Al(OH)3不稳定,易转化为三水铝石等晶质矿物,从而对Cr(Ⅵ)的吸附和还原产生影响,但目前对其影响机理尚不明确。本研究分别制备了两种有机碳与金属原子物质的量比值(C/M比)为1和15的HA-Al(Ⅲ)共沉物,并对它们和Al(OH)3单体同步进行了转化处理和表征;利用不同转化进度的HA-Al(Ⅲ)共沉物和Al(OH)3单体开展了Cr(Ⅵ)吸附还原实验,并分析了共沉物转化进度对Cr(Ⅵ)吸附还原的影响机理。实验结果表明,共沉物的转化进度对Cr(Ⅵ)的还原几乎无影响,但对Cr(Ⅵ)的吸附影响显著;随转化进度提高,“类矿物”共沉物(C/M比为1)对Cr(Ⅵ)的吸附量从0.91 mmol·g−1降低至0.21 mmol·g−1,而“类有机质”共沉物(C/M比为15)对Cr(Ⅵ)的吸附量几乎未受影响;“类矿物”共沉物对Cr(Ⅵ)的吸附受Al(Ⅲ)矿物表面羟基的络合作用主控,其次为颗粒内扩散作用;随转化进度提高,共沉物及转化产物上表面络合态与颗粒内扩散态Cr(Ⅵ)的量分别随矿物比表面积和孔容的减小而降低;“类有机质”共沉物对Cr(Ⅵ)的吸附和还原主要受HA表面有机官能团的络合和还原作用控制,因此几乎不受矿物晶型转化的影响。
-
关键词:
- 铬污染 /
- HA-Al(Ⅲ)共沉物 /
- 吸附还原 /
- 表面络合 /
- 颗粒内扩散
Abstract: HA-Al(Ⅲ) co-precipitates are widespread in soils and aquifers, and have strong adsorption and reduction capabilities for Cr(Ⅵ) in groundwater. The amorphous Al(OH)3 in co-precipitate is unstable and easy to transform into crystalline minerals, such as gibbsite, which will affect the adsorption and reduction of Cr(Ⅵ), but the influence mechanism is still unclear. In this study, two HA-Al(Ⅲ) co-precipitates with atom molar ratios of organic carbon to metal (C/M ratio) of 1 and 15 were prepared, and the transformation and characterization were conducted on both of them synchronously, and taking Al(OH)3 monomer as reference substance. The Cr(Ⅵ) adsorption and reduction experiment was conducted using HA-Al(Ⅲ) co-precipitates and Al(OH)3 monomer with different transformation extent, and the influence mechanism of transformation extent on Cr(Ⅵ) adsorption and reduction was investigated. According to the results, the transformation extent of the co-precipitate had little effect on Cr(Ⅵ) reduction, but had significant effects on Cr(Ⅵ) adsorption. With transformation extent increasing, the adsorption amount of Cr(Ⅵ) by “mineral-like” co-precipitate (C/M ratio was 1) decreased from 0.91 mmol·g−1 to 0.21 mmol·g−1, while the adsorption amount of Cr(Ⅵ) by the “organic matter-like” co-precipitate (C/M ratio was 15) was almost unchanged. The adsorption of Cr(Ⅵ) by “mineral-like” co-precipitates was dominated by the complexation of hydroxyl groups on the surface of Al(Ⅲ) minerals, followed by intraparticle diffusion. With transformation extent increasing, the surface complexed and intraparticle diffused Cr(Ⅵ) on the co-precipitates and their transformation products decreased with the decreasing of specific surface area and pore volume respectively. The adsorption and reduction of Cr(Ⅵ) by the “organic matter-like” co-precipitates were governed by the complexation and reduction associated with organic functional groups on HA surface, so it was hardly affected by the mineral transformation in co-precipitates. -

-
表 1 不同转化进度HA-Al(III)共沉物的元素组成
Table 1. Elemental composition of HA-Al(III) co-precipitate with different transformation extent
样品名称*
Sample nameAl含量/%
Al contentC含量/%
C content理论C/M比
Theoretical C/M ratio实际C/M比
Actual C/M ratioR0D0 26.02 (0.83) — 0 — R0D2 27.72 (2.25) — 0 — R0D7 32.15 (0.21) — 0 — R0D15 32.47 (0.10) — 0 — R0D26 34.69 (0.45) — 0 — R1D0 22.37 (0.01) 9.52 1 0.96(0.00) R1D2 23.07 (0.67) 9.88 1 0.96(0.03) R1D7 25.68 (1.33) 10.80 1 0.94(0.04) R1D15 26.41 (0.62) 10.77 1 0.92(0.02) R1D26 28.38 (0.28) 10.75 1 0.85(0.01) R15D0 6.69 (0.03) 36.20 15 12.18(0.05) R15D2 6.32 (0.04) 34.77 15 12.38(0.08) R15D7 6.59 (0.04) 36.57 15 12.49(0.08) R15D15 5.97 (0.07) 36.80 15 13.86(0.16) R15D26 5.96 (0.36) 36.31 15 13.76(0.83) *不同转化进度的共沉物记作RaDb(a为共沉物的C/M比,b为转化天数).
*Cop-precipitates with different transformation extent are abbreviated as RaDb (a represents C/M ratio, and b represents transformation days).表 2 不同结构HA-Al(Ⅲ)共沉物转化产物的比表面积及孔径分布
Table 2. specific surface area and pore size distribution of conversion products of HA-Al(Ⅲ) co-precipitation with different structures
样品名称*
Sample name比表面积/(m2·g−1)
Specific surface area总孔容/(cm3·g−1)
Total pore volume介孔孔容/(cm3·g−1)
Mesoporous pore volume微孔孔容/(cm3·g−1)
Micropore volumeR0D0 180.50 0.8809 0.8748 0.0061 R0D26 48.98 0.2371 0.2327 0.0013 R1D0 132.02 0.5408 0.5380 0.0028 R1D26 37.93 0.2719 0.2709 0.0010 R15D0 2.49 0.0063 0.0063 0.0000 R15D26 3.28 0.0052 0.0052 0.0000 *不同转化进度的共沉物记作RaDb(a为共沉物的C/M比,b为转化天数).
*Cop-precipitates with different transformation extent are abbreviated as RaDb (a represents C/M ratio, and b represents transformation days). -
[1] XIE J Y, GU X Y, TONG F, et al. Surface complexation modeling of Cr(Ⅵ) adsorption at the goethite-water interface [J]. Journal of Colloid and Interface Science, 2015, 455: 55-62. doi: 10.1016/j.jcis.2015.05.041 [2] RAKHUNDE R, DESHPANDE L, JUNEJA H D. Chemical speciation of chromium in water: A review [J]. Critical Reviews in Environmental Science and Technology, 2012, 42(7): 776-810. doi: 10.1080/10643389.2010.534029 [3] LADEIRA A C Q, CIMINELLI V S T, DUARTE H A, et al. Mechanism of anion retention from EXAFS and density functional calculations: Arsenic (Ⅴ) adsorbed on gibbsite [J]. Geochimica et Cosmochimica Acta, 2001, 65(8): 1211-1217. doi: 10.1016/S0016-7037(00)00581-0 [4] MCGECHAN M B, LEWIS D R. SW—soil and water: Sorption of phosphorus by soil, part 1: Principles, equations and models [J]. Biosystems Engineering, 2002, 82(1): 1-24. doi: 10.1006/bioe.2002.0054 [5] ZHANG J, CHEN L P, YIN H L, et al. Mechanism study of humic acid functional groups for Cr(Ⅵ) retention: Two-dimensional FTIR and 13C CP/MAS NMR correlation spectroscopic analysis [J]. Environmental Pollution, 2017, 225: 86-92. doi: 10.1016/j.envpol.2017.03.047 [6] SCHEEL T, DÖRFLER C, KALBITZ K. Precipitation of dissolved organic matter by aluminum stabilizes carbon in acidic forest soils [J]. Soil Science Society of America Journal, 2007, 71(1): 64-74. doi: 10.2136/sssaj2006.0111 [7] MIKUTTA R, KLEBER M, TORN M S, et al. Stabilization of soil organic matter: Association with minerals or chemical recalcitrance? [J]. Biogeochemistry, 2006, 77(1): 25-56. doi: 10.1007/s10533-005-0712-6 [8] KLEBER M, EUSTERHUES K, KEILUWEIT M, et al. Mineral-organic associations: Formation, properties, and relevance in soil environments [J]. Advances in Agronomy, 2015, 130: 1-140. [9] BERKOWITZ J, ANDERSON M A, GRAHAM R C. Laboratory investigation of aluminum solubility and solid-phase properties following alum treatment of lake waters [J]. Water Research, 2005, 39(16): 3918-3928. doi: 10.1016/j.watres.2005.06.025 [10] CHEN C M, DYNES J J, WANG J, et al. Properties of Fe-organic matter associations via coprecipitation versus adsorption [J]. Environmental Science & Technology, 2014, 48(23): 13751-13759. [11] CHEN K Y, CHEN T Y, CHAN Y T, et al. Stabilization of natural organic matter by short-range-order iron hydroxides [J]. Environmental Science & Technology, 2016, 50(23): 12612-12620. [12] WANG H, ZHANG J, ZHU J Q, et al. Synergistic/antagonistic effects and mechanisms of Cr(Ⅵ) adsorption and reduction by Fe(III)-HA coprecipitates [J]. Journal of Hazardous Materials, 2021, 409: 124529. doi: 10.1016/j.jhazmat.2020.124529 [13] 徐仁扣. 酸化红壤的修复原理与技术[M]. 北京: 科学出版社, 2013. [14] DU H H, HUANG Q Y, ZHOU M, et al. Sorption of Cu(Ⅱ) by Al hydroxide organo-mineral coprecipitates: Microcalorimetry and NanoSIMS observations [J]. Chemical Geology, 2018, 499: 165-171. doi: 10.1016/j.chemgeo.2018.09.026 [15] DAS S, ESSILFIE-DUGHAN J, HENDRY M J. Fate of adsorbed arsenate during phase transformation of ferrihydrite in the presence of gypsum and alkaline conditions [J]. Chemical Geology, 2015, 411: 69-80. doi: 10.1016/j.chemgeo.2015.06.031 [16] DAS S, HENDRY M J, ESSILFIE-DUGHAN J. Transformation of two-line ferrihydrite to goethite and hematite as a function of pH and temperature [J]. Environmental Science & Technology, 2011, 45(1): 268-275. [17] DAS S, HENDRY M J, ESSILFIE-DUGHAN J. Effects of adsorbed arsenate on the rate of transformation of 2-line ferrihydrite at pH 10 [J]. Environmental Science & Technology, 2011, 45(13): 5557-5563. [18] ZHENG Z Y, ZHENG Y, TIAN X C, et al. Interactions between iron mineral-humic complexes and hexavalent chromium and the corresponding bio-effects [J]. Environmental Pollution, 2018, 241: 265-271. doi: 10.1016/j.envpol.2018.05.060 [19] BARNIE S, ZHANG J, WANG H, et al. The influence of pH, co-existing ions, ionic strength, and temperature on the adsorption and reduction of hexavalent chromium by undissolved humic acid [J]. Chemosphere, 2018, 212: 209-218. doi: 10.1016/j.chemosphere.2018.08.067 [20] 孟令利. 氢氧化铝在苛性碱中溶解动力学研究 [J]. 轻金属, 2012(9): 23-27. doi: 10.3969/j.issn.1002-1752.2012.09.006 MENG L L. Study on dissolution kinetics of the aluminium hydroxide in the caustic soda [J]. Light Metals, 2012(9): 23-27(in Chinese). doi: 10.3969/j.issn.1002-1752.2012.09.006
[21] BANFIELD J F, WELCH S A, ZHANG H Z, et al. Aggregation-based crystal growth and microstructure development in natural iron oxyhydroxide biomineralization products [J]. Science, 2000, 289(5480): 751-754. doi: 10.1126/science.289.5480.751 [22] 李波, 邵玲玲. 氧化铝、氢氧化铝的XRD鉴定 [J]. 无机盐工业, 2008, 40(2): 54-57. doi: 10.3969/j.issn.1006-4990.2008.02.019 LI B, SHAO L L. Appraisal of alumina and aluminium hydroxide by XRD [J]. Inorganic Chemicals Industry, 2008, 40(2): 54-57(in Chinese). doi: 10.3969/j.issn.1006-4990.2008.02.019
[23] YU G, SAHA U K, KOZAK L M, et al. Combined effects of tannate and ageing on structural and surface properties of aluminum precipitates [J]. Clays and Clay Minerals, 2007, 55(4): 369-379. doi: 10.1346/CCMN.2007.0550405 [24] 张哲, 李殿卿, 白立光, 等. 双铝法制拟薄水铝石的制备条件对其胶溶性能的影响 [J]. 化学推进剂与高分子材料, 2021, 19(1): 48-51. ZHANG Z, LI D Q, BAI L G, et al. Influence of preparation conditions of pseudo-boehmite prepared by double aluminum method on its peptization performance [J]. Chemical Propellants & Polymeric Materials, 2021, 19(1): 48-51(in Chinese).
[25] 苗壮, 史建公, 郝建薇, 等. 拟薄水铝石的胶溶性与结构的关系 [J]. 石油学报(石油加工), 2016, 32(3): 493-500. MIAO Z, SHI J G, HAO J W, et al. Relationship between peptization and structure of pseudo-boehmite [J]. Acta Petrolei Sinica (Petroleum Processing Section), 2016, 32(3): 493-500(in Chinese).
[26] YU G D, FU F L, YE C J, et al. Behaviors and fate of adsorbed Cr(Ⅵ) during Fe(Ⅱ)-induced transformation of ferrihydrite-humic acid co-precipitates [J]. Journal of Hazardous Materials, 2020, 392: 122272. doi: 10.1016/j.jhazmat.2020.122272 [27] CHEN K Y, TZOU Y M, CHAN Y T, et al. Removal and simultaneous reduction of Cr(Ⅵ) by organo-Fe(Ⅲ) composites produced during coprecipitation and coagulation processes [J]. Journal of Hazardous Materials, 2019, 376: 12-20. doi: 10.1016/j.jhazmat.2019.04.055 -




 下载:
下载: