-
在饮用水输配过程中,铁质管材管件普遍存在,管网铁腐蚀和铁释放能够造成颗粒物增多,直接影响饮用水水质。尽管全球多地已开始将老旧无内衬铸铁管更换淘汰,但无内衬铸铁管在给水管网中仍然广泛使用。输配过程中,管网颗粒物能够进一步团聚、沉降、又累积在管壁上,颗粒积累会对饮用水质量产生许多负面影响,严重时能够引发“黄水”。在颗粒物界面,通常伴随着微生物的生长、各类有机无机成分的结合等反应[1],在水力冲击下,管垢会重新释放到自来水中并释放出有机物,进一步加剧水质恶化[2]。因此,以铁颗粒物为代表的颗粒物通常被视为致浊致色的污染物,少有研究关注以铁颗粒物“以废治废”作为催化剂进行“黄水”处理净化。
氯化是一种广泛使用的饮用水处理工艺,但会产生具有潜在致癌作用和毒性风险的消毒副产物 (DBPs) [3],常见的是三卤甲烷 (THMs) 、卤乙酸 (HAAs) 、卤乙腈 (HANs) 等。以二价铁离子催化过氧化氢的芬顿氧化是去除水中有机污染物的有效方法,过氧化氢一定条件下可以分解产生具有强氧化性的羟基自由基[4] (E0=2.80 V) 。为了避免二价铁离子反应后产生大量污泥的局限,将具有催化能力的铁离子进行固定化,形成金属、金属氧化物、金属负载型以及金属离子掺杂型固体催化剂,去催化过氧化氢的非均相芬顿反应获得了广泛的关注[5-6]。我们在前有研究中发现,铁基芬顿催化剂对DBPs均有良好的催化降解效果[7]。OLIVEIRA等[8]利用管网颗粒物作为新型类芬顿催化剂来降解百草枯,并表现出优异的催化性能,颗粒物界面的存在以及浸出离子的产生对该过程发挥了重要作用。
本研究以无内衬铸铁管道中收集的管网颗粒物作为非均相芬顿催化剂去除水中DBPs,基于毒性评估探究其对常规DBPs三卤甲烷、卤乙酸、卤乙腈的处理效果,基于非靶向识别技术探究其对未知DBPs的去除效果,通过对浊度、颗粒数、总有机碳含量、天然有机物含量等指标进行分析进一步分析去除机制,研究将为给水管网中DBPs的去除提供为一种低成本、高效率的去除思路。
-
1) 管网颗粒物采集方法。在中国北方某城市频繁发生“黄水”区域的给水管网截取管道,管材为无内衬铸铁管,管径为DN100,管龄约为20年。利用软毛刷刷取管网颗粒物,将获得的管网颗粒物冷冻干燥,再通过90目 (160 μm) 筛网进行筛分。
2) 芬顿催化实验方法。实验水样为上述给水管网对应的龙头水,浊度为(0.3±0.1) NTU、余氯为(0.5±0.1) mg·L−1 (Cl2) 、溶解氧为(9.2±0.4) mg·L−1,当日龙头水测得TOC为(3.2±0.1) mg·L−1,天然有机物归化浓度718.45,pH=7.7±0.1。将自来水静置30 min至余氯完全被消耗。配制管垢浓度为100 mg·L−1,双氧水有效浓度为450 μL·L−1,在加入双氧水后,将反应容器密封,置于摇床中以180 r∙min−1速度震荡,在反应的0.5、1、3、6 h分别取样,并测试相关水质指标。
-
浊度计 (2100Q,美国HACH公司) ;便携式多参数仪 (HQ 40d,美国HACH公司) ;表面电位和粒径使用zeta电位分析仪 (Zetasizer2000,英国Malvern仪器有限公司) 测试;用电感耦合等离子体质谱仪 (ICP-MS NexlON 300X,美国 PerkinElmer公司) 测试样品的金属离子浓度。为了测定THMs、HAAs和HANs,使用甲基叔丁基醚作为萃取剂提取水样,并通过配备电子捕获检测器 (GC/ECD 7890B,美国安捷伦公司) 和HP-5熔融石英毛细管柱 (30 m×0.25 mm 0.25 μm,美国安捷伦公司) 的气相色谱仪进行分析,THMs、HAAs和HANs标准品购于天津阿尔塔科技有限公司,THMs、HAAs和HANs的毒性分析依据自PLEWA和MUELLNER等人的研究结果[9-11],单位细胞毒性 (UCI) 定义为各类 DBPs CHO 细胞毒性%C1/2 值 (M) 的倒数,单位遗传毒性 (UGI) 定义为各类 DBPs CHO 遗传潜力值 (M) 的倒数。样品的晶体结构用使用X射线衍射仪 (XRD D/Max-2200,日本Rigaku公司) 进行分析,参数为铜靶 (40 kV,40 mA) ,扫描角度10°~90°,并用Highscore plus软件分析处理数据。傅里叶变换红外光谱仪 (FTIR Nicolet iN10MX,美国Thermo Fisher Scientific公司) 用于分析样品表面的官能团。样品的表面形貌和元素组成利用场发射扫描电子显微镜 (SEM H-7500,日本Hitachi公司) 获得。颗粒数用台式激光粒子分析仪 (GR-1500A,杭州绿洁科技股份有限公司) 测定。溶解性的天然有机物使用F-7000荧光分光光度计 (F-7000,日本Hitachi公司) 记录荧光光谱,并使用激发发射矩阵 (EEM) 表征DOM的特征。激发波长范围为200~400 nm,增量为5 nm,发射波长范围为220~550 nm,增量为5 nm,利用matlab软件使用积分法计算天然有机物含量,最终值取为3个重复的平均值。 (2) 使用傅里叶变换离子回旋共振质谱仪 (FT-ICR-MS SolariX,美国Bruker公司) 对溶解的有机物进行分析,其磁场强度为15.0 T。离子源为电喷雾离子源 (ESI) ,负离子模式,并用Bruker Compass DataAnalysis软件对数据进行处理。
-
图1(a)~(c)为THMs、HAAs、HANs在管网颗粒物芬顿反应中的变化。在反应进行的6 h内,HAAs含量几乎不变。在反应初始的0.5 h内THMs、HANs含量明显降低。反应6 h后,THMs和HANs去除率分别为51.8%和47.6%。在此基础上,计算了各样品计算毒性和遗传毒性,DBPs 的毒性数据来自 PLEWA[9, 12]和MUELLNER等人的研究结果,DBPs 细胞毒性定义为单位细胞毒性与样品中DBPs浓度的乘积,同样的,遗传毒性定义为单位遗传毒性与样品中 DBPs 浓度的乘积[13],毒性的变化如图1(d)~(f)所示,管网颗粒物芬顿反应6 h后,THMs、HAAs、HANs3种DBPs的总UCI降低了81.07%、总UGI降低了30.46%。虽然THMs和HAAs的浓度明显高于HANs,但不受管制的HANs在 DBPs总毒性中占主导地位,因此芬顿过程对HANs的高效去除有效降低了水质的毒性风险。
-
尽管文献中已报道了 600 多种 DBPs,但氯化水产生的总有机卤素中仍有超过 50% 尚未被识别[14]。利用傅里叶变换离子回旋共振质谱仪对对照组和实验组的未知DBPs进行非靶向识别分析,如图2所示。结果表明,管网颗粒物芬顿反应6 h后,未知DBPs种类明显降低,由85种降低至49种。管网颗粒物芬顿对DBP(1-Cl) (含1个氯原子的DBPs) 去除率为81.3%,对DBP(2-Cl) (含2个氯原子的DBPs) 去除率为28.2%,对DBP(3-Cl) (含3个氯原子的DBPs) 去除率为40.0%,DBP(1-Cl)下降程度最为明显,表明芬顿过程对于DBP(1-Cl)具有更高的降解性能,而DBP(3-Cl)有可能在降解中转化为DBP(2-Cl),导致DBP(2-Cl)的去除率最低。在处理前后,DBPs中占比最高的都是DBP(2-Cl)。由此可见,经过芬顿处理之后,不同氯原子个数的DBPs含量均有所降低,表明芬顿过程对DBPs具有良好的降解性能。
-
XRD分析如图3(a)所示,管垢占比最多的两种晶体分别是磁赤铁矿和针铁矿,分别为25%和23%。羟基氧化铁中具有代表性的六方纤铁矿、针铁矿、纤铁矿和四方纤铁矿共占所有晶体总量的52%(表1),这为芬顿反应提供了重要的金属活性位点。管道沉积物中的羟基氧化铁组分在催化过程中可释放出铁离子进而促进羟基自由基的产生,提升催化效率[15]。FTIR分析如图3(b)所示,管垢在3 400 和3 100 cm−1处分别有较宽的特征峰,这是由于氢键表面的羟氢基团吸收和羟氢拉伸而产生的。在890 和790 cm−1 附近的两个特征峰为 Fe-O-H 的弯曲振动,进一步表明铁氧化物是该反应中的关键催化位点。样品的表面形貌如图3(c)SEM测试所示,可见管垢表面粗糙、具有针刺状结构,进一步表明样品具有丰富的反应位点。OLIVEIRA等[16]将长度为0.5~14 m的旧铸铁段安装到聚氯乙烯管道回路系统中发现其对农药的降解率产生显着的积极影响,铁管段越长农药降解速度越快。本研究进一步证实了管网颗粒物基于铁基组分的催化活性,在消毒副产物处理方面也具有良好的应用潜力。
-
浊度是评估水质变色的常用指标[17]。管网颗粒物芬顿反应过程中样品的浊度和颗粒数随着反应时间的增加而增大。6 h后,样品浊度从82.9 NTU变为105.8 NTU, 增加了27.6%,颗粒数从17 075 个∙mL−1变为27 798 个∙mL−1,增加了62.8%。这可能是由于管垢在芬顿反应过程中大颗粒物发生破碎,逐步变为小颗粒物,进而造成浊度增大[18],颗粒物由大变小将有助于提升其在芬顿反应过程中的活性位点数量。然而,虽然颗粒物的变化有助于提升对DBPs的降解速率,但同时也增大了变色风险。
-
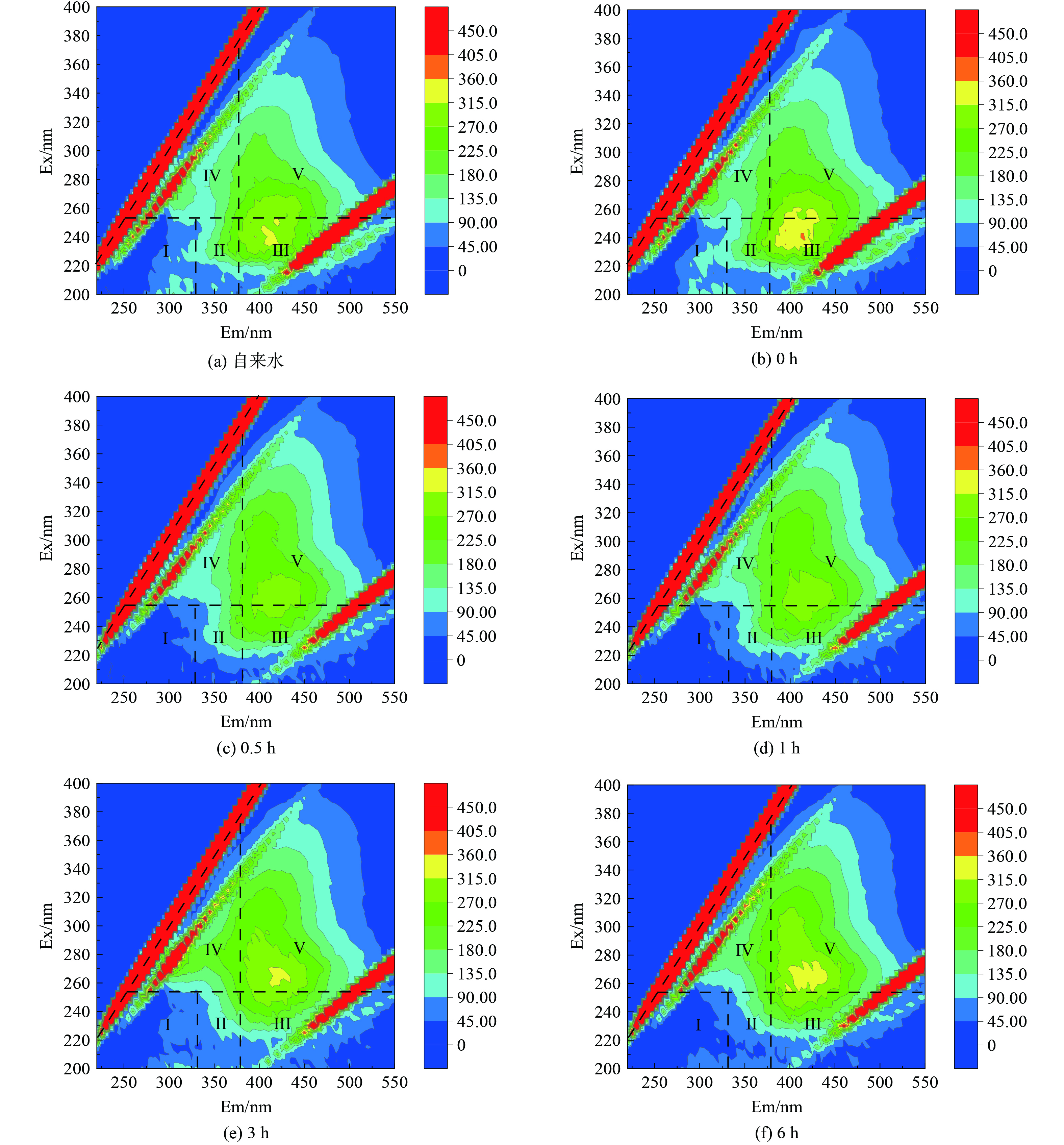
反应过程中总有机碳和天然有机物 (NOM) 的变化如图5(a)和(b)所示,三维荧光图如图6所示。三维荧光光谱分为5个区域分别对应酪氨酸类蛋白质 (Ⅰ区,Ex<250 nm,Em<330 nm) 、色氨酸类蛋白质 (Ⅱ区,Ex<250 nm,330 nm<Em<380 nm) 、富里酸类 (Ⅲ区,Ex<250 nm,Em>380 nm) 、微生物代谢产物类 (Ⅳ区,250 nm<Ex<280 nm,Em<380 nm) 和腐殖酸类 (Ⅴ区,Ex>280 nm,Em>380 nm) 有机物[19]。虽然芬顿催化过程能够降解DBPs,但水中TOC没有明显变化,可能是因为管垢颗粒物的破碎会向水中释放有机物,这与上述浊度和颗粒数的变化相一致。NOM中酪氨酸和色氨酸明显降低,可能是酪氨酸和色氨酸更易被自由基降解。腐殖酸含量几乎不变,表明管网颗粒物可能向水中释放了腐殖酸。HE等[15]发现水中还原性小分子有机物羟胺等的存在能够有效提升管网颗粒物主要组分羟基氧化铁的催化性能,这是由于还原性小分子有机物加速了Fe(Ⅲ)向Fe(Ⅱ)的转变,有效促进了芬顿催化过程中的限速步骤。颗粒物中溶出的NOM可以增加铁颗粒之间的空间排斥力,从而有助于抑制聚集[20]。腐殖酸通过影响表面电荷特性来控制颗粒与颗粒之间的相互作用。腐殖酸对胶体颗粒的稳定作用可归因于静电稳定作用的增强,从而增加了颗粒的分散性[21]。颗粒界面NOM重新分布也可通过改变静电、疏水和氢键等相互作用来抑制颗粒团聚[22]。腐殖酸与酪氨酸除了存在疏水作用和氢键外,腐殖酸的羧基和羟基还可以直接与酪氨酸的氨基相互作用[23]。因此,腐殖酸和酪氨酸在颗粒界面的浸出和再吸附将使NOM在颗粒表面形成更均匀的分布,从而抑制团聚,有助于进一步提升催化过程中的活性位点数量。
-
1)管网颗粒物芬顿后,HAAs含量几乎不变,THMs和HANs去除率分别为51.8%和47.6%。
2)基于上述三种消毒副产物浓度变化,细胞毒性降低了81.07%、遗传毒性降低了30.46%,可见管垢的芬顿反应对于毒性消减具有良好的处理效能。
3)非靶向识别分析表明,未知DBPs种类由85降低至49,DBP(1-Cl)去除率高达81.3%,DBP(1-Cl)下降程度最为明显,表明芬顿过程对于DBP(1-Cl)具有更高的降解性能,而DBP(3-Cl)有可能在降解中转化为DBP(2-Cl),导致DBP(2-Cl)的去除率最低。
4)管垢占比最多的两种晶体分别是磁赤铁矿和针铁矿,分别为25%和23%,是发挥催化作用的关键组分,管垢表面具有丰富的针刺状结构,有助于增加催化活性位点。
5)管垢颗粒物的破碎会向水中释放腐殖酸有机物,阻碍颗粒物团聚,有助于进一步提升催化活性位点。
由此可见,管网颗粒物芬顿能够有效降解DBPs、降低毒性风险,为给水管网“黄水”颗粒物的“以废治废”提供了新思路。
给水管网颗粒物对消毒副产物的芬顿催化去除机制
Removal of DBPs by particles from drinking water distribution system through in-situ Fenton reaction
-
摘要: 给水管网中以铁颗粒物为代表的颗粒物通常被视为致浊致色的污染物,本研究以铁颗粒物作为催化剂“以废治废”进行“黄水”处理净化,探究其对水中消毒副产物的降解净化效能。结果表明,管网颗粒物非均相催化对三卤甲烷和卤乙腈去除率分别为51.8%和47.6%,对卤乙酸去除效果不明显。基于上述三种消毒副产物的细胞毒性降低了81.07%、遗传毒性降低了30.46%。管垢占比最多的两种晶体分别是磁赤铁矿和针铁矿,分别为25%和23%,是发挥催化作用的关键组分。管垢颗粒物的破碎会向水中释放腐殖酸有机物,阻碍颗粒物团聚,有助于提升催化活性位点。由此可见,管网颗粒物芬顿能够有效降解DBPs、降低毒性风险,为给水管网“黄水”颗粒物芬顿反应削弱水质毒性风险提供了新思路。Abstract: Iron particles in drinking water distribution systems are usually regarded as pollutants that causes turbidity and color problem. This study used iron particles as a catalyst to "treat waste with waste" for in-situ removal of disinfection by-products (DBPs) in "yellow water". The results showed that the removal rates of trihalomethane and haloacetonitrile by in situ catalysis of iron particles were 51.8% and 47.6%, respectively, while the removal effect of haloacetic acid was not significant. Based on the three DBPs mentioned above, the cytotoxicity was reduced by 81.07% and the genetic toxicity was reduced by 30.46%. The two main types of crystals in the iron particles were magnetite and goethite, which are 25% and 23%, respectively, and they were key catalytic sites. The iron particles would release humic acid organic compounds into the water, hindering particle aggregation and helping to enhance catalytic activity sites. Hence, the results revealed that in-situ Fenton reaction of iron particles in the drinking water distribution systems can effectively degrade DBPs and reduce toxicity risks, providing a new approach for the in-situ Fenton reaction to weaken the toxicity risk of "yellow water".
-

-
表 1 管垢样品的晶体组成
Table 1. Crystal types composition of the pipe scale
矿物名称 方程式 含量/% 磁铁矿 Fe3O4 5 赤铁矿 α-Fe2O3 12 磁赤铁矿 γ-Fe2O3 25 六方纤铁矿 δ-FeOOH 7 针铁矿 α-FeOOH 23 纤铁矿 γ-FeOOH 17 四方纤铁矿 β-FeOOH 5 菱铁矿 FeCO3 2 石英 SiO2 4 -
[1] LI G, DING Y, XU H, et al. Characterization and release profile of (Mn, Al)-bearing deposits in drinking water distribution systems[J]. Chemosphere, 2018, 197: 73-80. doi: 10.1016/j.chemosphere.2018.01.027 [2] QI P, LI T, HU C, et al. Effects of cast iron pipe corrosion on nitrogenous disinfection by-products formation in drinking water distribution systems via interaction among iron particles, biofilms, and chlorine[J]. Chemosphere, 2022, 292: 133364. doi: 10.1016/j.chemosphere.2021.133364 [3] DING S, DENG Y, BOND T, et al. Disinfection byproduct formation during drinking water treatment and distribution: A review of unintended effects of engineering agents and materials[J]. Water Research, 2019, 160: 313-329. doi: 10.1016/j.watres.2019.05.024 [4] POURAN S R, RAMAN A A A, WAN M A W D J J O C P. Review on the application of modified iron oxides as heterogeneous catalysts in Fenton reactions[J]. Journal of Cleaner Production, 2013, 64(2): 1-12. [5] GUO S, ZHANG G, GUO Y, et al. Graphene oxide–Fe2O3 hybrid material as highly efficient heterogeneous catalyst for degradation of organic contaminants[J]. Carbon, 2013, 60: 437-444. doi: 10.1016/j.carbon.2013.04.058 [6] XU L, WANG J J E S, TECHNOLOGY. Magnetic Nanoscaled Fe3O4/CeO2 Composite as an Efficient Fenton-Like Heterogeneous Catalyst for Degradation of 4-Chlorophenol[J]. Environmental Science & Technology, 2017, 46(18): 10145-10153. [7] WANG X, ZHUANG Y, SHI B. Degradation of trichloroacetic acid by MOFs-templated CoFe/graphene aerogels in peroxymonosulfate activation[J]. Chemical Engineering Journal, 2022, 450: 137799. doi: 10.1016/j.cej.2022.137799 [8] OLIVEIRA C, SANTOS M S F, MALDONADO-HODAR F J, et al. Use of pipe deposits from water networks as novel catalysts in paraquat peroxidation[J]. Chemical Engineering Journal, 2012, 210: 339-349. doi: 10.1016/j.cej.2012.09.001 [9] WAGNER E D, PLEWA M J. CHO cell cytotoxicity and genotoxicity analyses of disinfection by-products: An updated review[J]. Journal of Environmental Sciences, 2017, 58: 64-76. doi: 10.1016/j.jes.2017.04.021 [10] PLEWA M J, WAGNER E D, RICHARDSON S D, et al. Chemical and Biological Characterization of Newly Discovered Iodoacid Drinking Water Disinfection Byproducts[J]. Environmental Science & Technology, 2004, 38(18): 4713-4722. [11] MUELLNER M G, WAGNER E D, MCCALLA K, et al. Haloacetonitriles vs. Regulated Haloacetic Acids: Are Nitrogen-Containing DBPs More Toxic?[J]. Environmental Science & Technology, 2007, 41(2): 645-651. [12] PLEWA M J, MUELLNER M G, RICHARDSON S D, et al. Occurrence, synthesis, and mammalian cell cytotoxicity and genotoxicity of haloacetamides: an emerging class of nitrogenous drinking water disinfection byproducts[J]. Environmental Science & Technology, 2008, 42: 955-961. [13] DING H, MENG L, ZHANG H, et al. Occurrence, profiling and prioritization of halogenated disinfection by-products in drinking water of China[J]. Environmental Science: Processes & Impacts, 2013, 15(7) ): 1424-1429. [14] KIMURA S Y, CUTHBERTSON A A, BYER J D, et al. The DBP exposome: Development of a new method to simultaneously quantify priority disinfection by-products and comprehensively identify unknowns[J]. Water Research, 2019, 148: 324-333. doi: 10.1016/j.watres.2018.10.057 [15] HE F, MA W, ZHONG D, et al. Degradation of chloramphenicol by α-FeOOH-activated two different double-oxidant systems with hydroxylamine assistance[J]. Chemosphere, 2020, 250: 126150. doi: 10.1016/j.chemosphere.2020.126150 [16] OLIVEIRA C, GRUSKEVICA K, JUHNA T, et al. Removal of paraquat pesticide with Fenton reaction in a pilot scale water system[J]. Drinking Water Engineering & Science Discussions, 2014, 7(1): 11-21. [17] 张楷立, 林大瑛, 邱楚茵, 等. 家庭常用处理方法控制氯化消毒饮用水中消毒副产物的研究进展[J]. 净水技术, 2021, 40(7): 60-70. [18] LI P, ZHUANG Y, SHI B, et al. Effects of boiling on iron particles in drinking water[J]. Aqua: water infrastructure, ecosystems and society, 2023, 72(1): 83-95. [19] SORENSEN J P R, DIAW M T, POUYE A, et al. In-situ fluorescence spectroscopy indicates total bacterial abundance and dissolved organic carbon[J]. Science of the Total Environment, 2020, 738: 139419. doi: 10.1016/j.scitotenv.2020.139419 [20] ZHAO J, GIAMMAR D E, PASTERIS J D, et al. Formation and aggregation of lead phosphate particles: Implications for lead immobilization in water supply systems[J]. Environmental Science & Technology, 2018, 52(21): 12612-12623. [21] PAN C, TROYER L D, LIAO P, et al. Effect of humic acid on the removal of chromium(VI) and the production of solids in iron electrocoagulation[J]. Environmental Science & Technology, 2017, 51(11): 6308-6318. [22] MYAT D T, STEWART M B, MERGEN M, et al. Experimental and computational investigations of the interactions between model organic compounds and subsequent membrane fouling[J]. Water Research, 2014, 48: 108-118. doi: 10.1016/j.watres.2013.09.020 [23] WU S, HUA X, MA B, et al. Three-dimensional analysis of the natural-organic-matter distribution in the cake layer to precisely reveal ultrafiltration fouling mechanisms[J]. Environmental Science & Technology, 2021, 55(8): 5442-5452. -




 下载:
下载: