-
我国城市环境充斥着各种各样的恶臭气体,其中有部分气体是由随处可见的污水暂存空间中释放而来。污水暂存空间是指为污水提供短期存储的有限空间,比如露天厕所及城市地下轨道交通附属厕所的化粪坑、污水池,压力流排水管道提升泵站的污水池,以及各种用途的污水暂存池等。暂存空间污水中的微生物群落,将复杂有机物水解转化为小分子有机物(主要为VFA),并在产氢产乙酸菌的作用下转化为氢和乙酸,进一步在甲烷菌(MA)的作用下产生甲烷和二氧化碳[1]。此外,在硫酸盐存在的条件下,生物膜或沉积物中的硫酸盐还原菌(SRB)可将硫酸盐还原为硫化氢气体[2]。因此,生活污水成分比例较高的密闭空间会产生H2S、CH4、CO等有害气体[3-4]。目前,控制硫化氢释放的方法主要有投加铁盐[5]、氧化剂[6]和杀菌剂[7],还有利用“烟囱效应”的自然通风法。但是,由于经济成本及季节性因素的限制,这些控制措施并未被广泛采用。
标准大气压下,在30 ℃时,H2S在水中的饱和浓度大约3 580 mg·L−1;在20 ℃时,H2S在水中的饱和溶解度大约为5 000 mg·L−1。虽然H2S在水中的饱和溶解度较大,但经常检测到污水上方气相中有较高浓度的H2S,而此时污水中的H2S并未达到饱和溶解度。因此,可在污水表面覆盖一种物质使H2S传质阻力增加,从而充分利用饱和溶解度让H2S尽可能溶解,进而无法进入气相,称这种物质为掩蔽剂。此种做法的重要意义在于:对数量较多、面积较小的污水池,控制H2S的产生与释放措施成本较高;对环境要求较高但又不具备处理条件的污水池,可以使其中的硫化物流至集中处理处或适宜排放处。关于这方面的研究在石油开采领域较多。JACOBSON等[8]和KIM等[9]的研究表明,使用大豆油和精油可以使H2S处在油层下面,能显著降低排放到周围环境中的H2S。相比之下,菜籽油无效,但产生这种不同效果的原因目前尚不清楚[10-11]。
同时,污水中的H2S浓度到达一定值时,可以抑制相关微生物。REIS等[12]的研究表明:在低pH下,SRB生长期间会受到产生的未离解的乙酸的抑制作用;在较高的pH下,H2S的抑制作用占主导地位;在接近中性pH下,发酵主要受所产生的H2S的影响,并且在较小程度上受乙酸浓度的影响。REIS等[12]还发现,硫酸盐还原产生的H2S对SRB的毒性作用具有直接性和可逆性,当硫化氢浓度为547 mg·L−1时,可完全抑制SRB的生长。ABRAM等[13]的研究表明,H2S对未经驯化的产甲烷菌致害浓度为50 mg·L−1。抑制作用是由于H2S进入微生物细胞内,与细胞内色素中的铁和含铁物质结合,导致电子传递系统失活,进而破坏其中的蛋白质[14]。因此,当硫酸盐浓度过高时,硫酸盐还原菌和产甲烷菌均受到了抑制,但溶解性硫化物对硫酸盐还原菌的毒性阈值比产甲烷菌更高[15]。
由于大豆油和精油在水中会扩散和挥发,故有必要寻找一种更实用的掩蔽剂。本研究通过实验筛选出合适的H2S掩蔽剂,并探究了掩蔽剂成分的组成比例和平铺厚度对掩蔽效果的影响。此外,还考察了掩蔽剂对下部水体水质的影响情况,讨论了掩蔽剂下部水体中高浓度溶解态H2S对相关微生物的抑制作用。研究结果可为控制恶臭气体释放对所处环境的危害提供参考。
全文HTML
-
作为阻挡H2S气体的掩蔽剂,应当具有以下几个特点:其密度比污水密度小;H2S气体分子不溶于且不能扩散进入该掩蔽剂中;H2S气体形成的气泡不能穿过该掩蔽剂进入污水上部的空气中(H2S气泡在液体中的上浮速度取决于浮力、黏性阻力和污水清洁度,当液体黏性阻力足够大,将会制止H2S的析出);掩蔽剂向污水中的分子扩散应尽可能小(否则随着扩散,掩蔽剂将损耗);掩蔽剂与水互不相溶,保持稳定;掩蔽剂不易挥发,不易燃,无毒。
由于H2S是极性分子,故依据相似相溶的原理,寻找的物质应当是非极性的。相似相溶的原理仅为一般规律,所以也需对分子间作用力、偶极作用以及范德华力进行考量。同时,还需要对所选的物质进行实验来验证是否可以隔绝H2S。
实验选用的H2S掩蔽剂有肉豆蔻酸异丙酯(IPM)、芝麻油、LSR、二甲基硅油(分析纯)、液体石蜡(MSDS)(化学纯)。各物质的基本性质见表1。实验用H2S依据式(1)制得。
针对密度比水小的掩蔽剂,取5个500 mL的烧杯,分别向其中加入300 mL自来水和3 g Na2S,并加入2 mL的2.5 mol·L−1 HCl,轻晃摇匀。然后,立即向其中4个烧杯中分别加入等体积的IPM、芝麻油、二甲基硅油、MSDS,从而将烧杯内的液体表面完全覆盖,随后用封口膜封闭烧杯口,并用胶带缠紧四周,以防止产生的H2S释放出来。使用M40气体检测仪测量各个烧杯上部气相中的H2S气体浓度。作为对照组,最后1个烧杯不加入掩蔽剂,当加入HCl后,立即用封口膜封闭烧杯口。
针对密度比水大的掩蔽剂,取2个500 mL烧杯,各加入3 g Na2S,再加入2 mL的2.5 mol·L−1 HCl,然后分别向其中加入等体积的乳白色LSR和半透明LSR,随后密封烧杯口。使用M40气体检测仪测量各个烧杯气相中的H2S浓度。
针对乳白色LSR和半透明LSR的密度问题,可考虑加入二甲基硅油或直径为1 mm 的EPS作为载体,以改善其密度。
-
确定了最优的掩蔽剂后,在满足浮力的前提下,探究半透明LSR和EPS在不同质量比下的掩蔽效果。用质量变化和表面扩散面积分别表征稳定性和流动性。称其初始重量Mns,随即加入到放置在水面的底部开口的纸杯,使其初始扩散面积一致。加入后,将纸杯移除,开始进行扩散。静置3 h后,测量形成的扩散面积,并将样品回收,晾干,称其最终重量Mnf。掩蔽剂样品的质量变化可根据式(2)进行计算。
式中:Mns为烧杯和其中的残余物的质量,g;Mnf为洗净和晾干烧杯和其中的残余物的质量,g。
-
确定了掩蔽剂的最适质量比后,为了满足生产实践的要求,进一步考察了6种配比比例在不同平铺厚度条件下的效果,得出最适的平铺厚度。
取多个500 mL烧杯,分别加入300 mL自来水,将配制好的同一配比的掩蔽剂样品加入其中,控制平铺厚度为0.1、0.2、0.3、0.4、0.5、1.0、1.5、2.0、2.5 cm,随后使用不同配比的样品,依次重复以上实验。平铺后静置24 h,将表面样品捞出、倒掉水、晾干。杯内残余物质量的计算如式(3)所示。
式中:Nts为烧杯和其中的残余物的质量,g;Ntf为洗净和晾干烧杯和其中的残余物的质量,g。
-
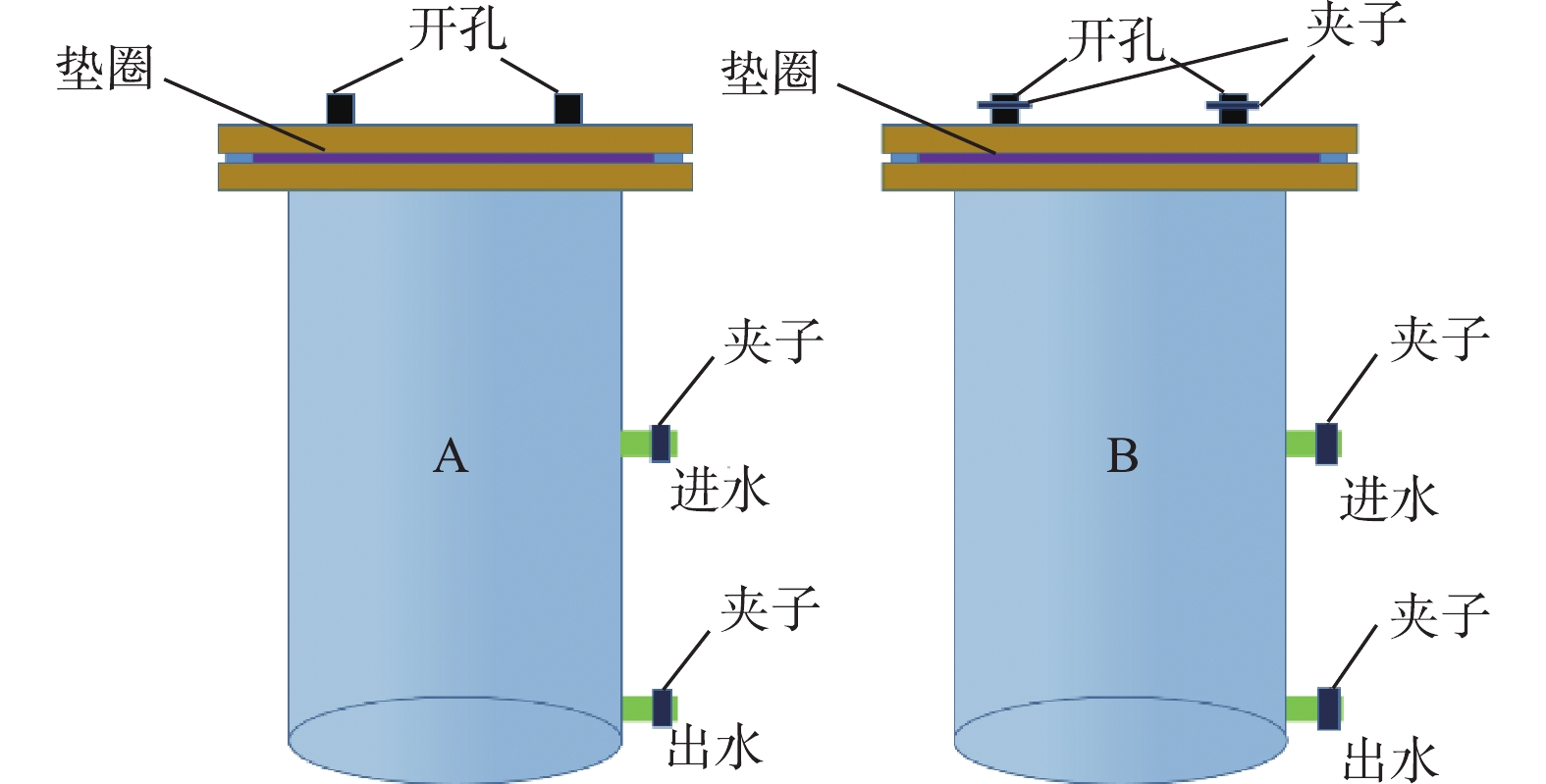
为探究掩蔽剂下部的水质随时间的变化,分别构建反应器A和B(图1),其高为320 mm,直径为80 mm,并放入20 ℃水中保温。分别向2个反应器中加入4 L配制的人工污水,并放入4个附着硫酸盐还原菌的载体滤料。在反应器B中的污水表面平铺掩蔽剂。每间隔3 d,分别从出水口取水样,测定其中硫化物的含量。将出水口打开流出2 L污水,从进水口补充2 L新鲜污水,从而为硫酸盐还原菌提供营养物质。在反应器A上部开2个小孔,模拟现实中的非密封条件。使用英思科M40 Pro气体组分仪,通过小孔测量上部气相中的H2S浓度。
-
实验所用的人工污水配方(每50 L)为葡萄糖10 g、NH4Cl 3 g、Na2HPO4·12H2O 1.25 g、NaH2PO4·12H2O 1.25 g、KHCO3 2.5 g、NaHCO3 6.5 g、MgSO4·7H2O 2.5 g、MnSO4·H2O 0.1 g、FeSO4·7H2O 0.1 g、无水CaCl2 0.15 g、酵母1.5 g、尿素1.5 g、蛋白胨1 g、大豆蛋白胨1 g、胰蛋白胨1 g、酪蛋白胨1 g。实验中硫化物的浓度测定采用《水质硫化物的测定亚甲基蓝分光光度法》(GB/T 16489-1996)。
1.1. 较优掩蔽剂的筛选
1.2. 掩蔽剂成分最适比例的确定
1.3. 最适平铺厚度的确定
1.4. 水质影响实验
1.5. 药剂和分析方法
-
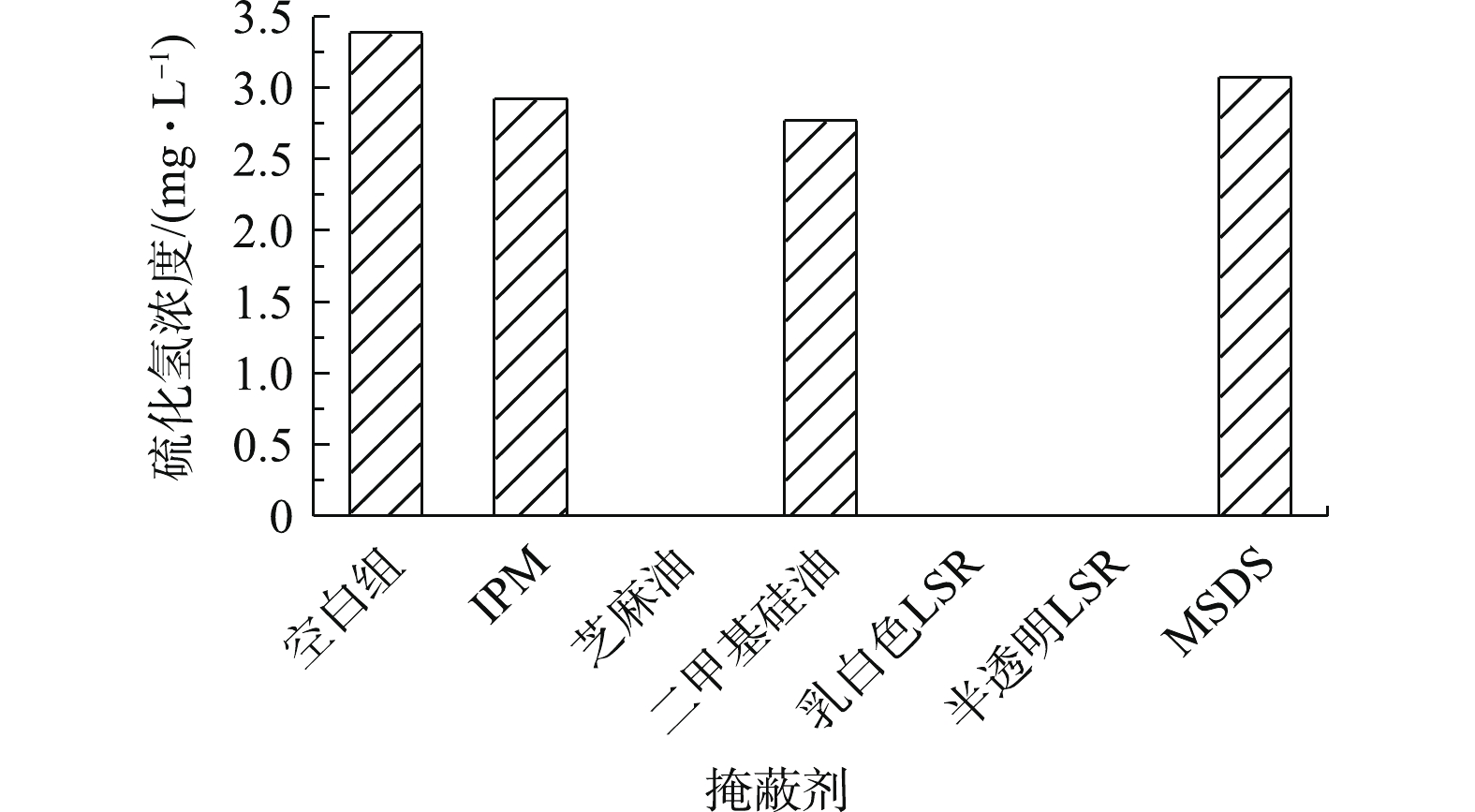
各种掩蔽剂对H2S的掩蔽效果通过各烧杯上部气相中的H2S浓度进行评价,其结果如图2所示。由图2可知,将IPM、二甲基硅油、MSDS平铺到液面之后,被液面下部的H2S穿透,没有起到阻挡H2S的作用,使得上部气相中H2S浓度升高。而芝麻油、乳白色LSR、半透明LSR上部气相没有出现H2S气体,说明其起到了掩蔽的作用。通过以上实验,初步排除了IPM、二甲基硅油、MSDS作为备用的掩蔽剂,在后续研究中选用LSR作为掩蔽剂。
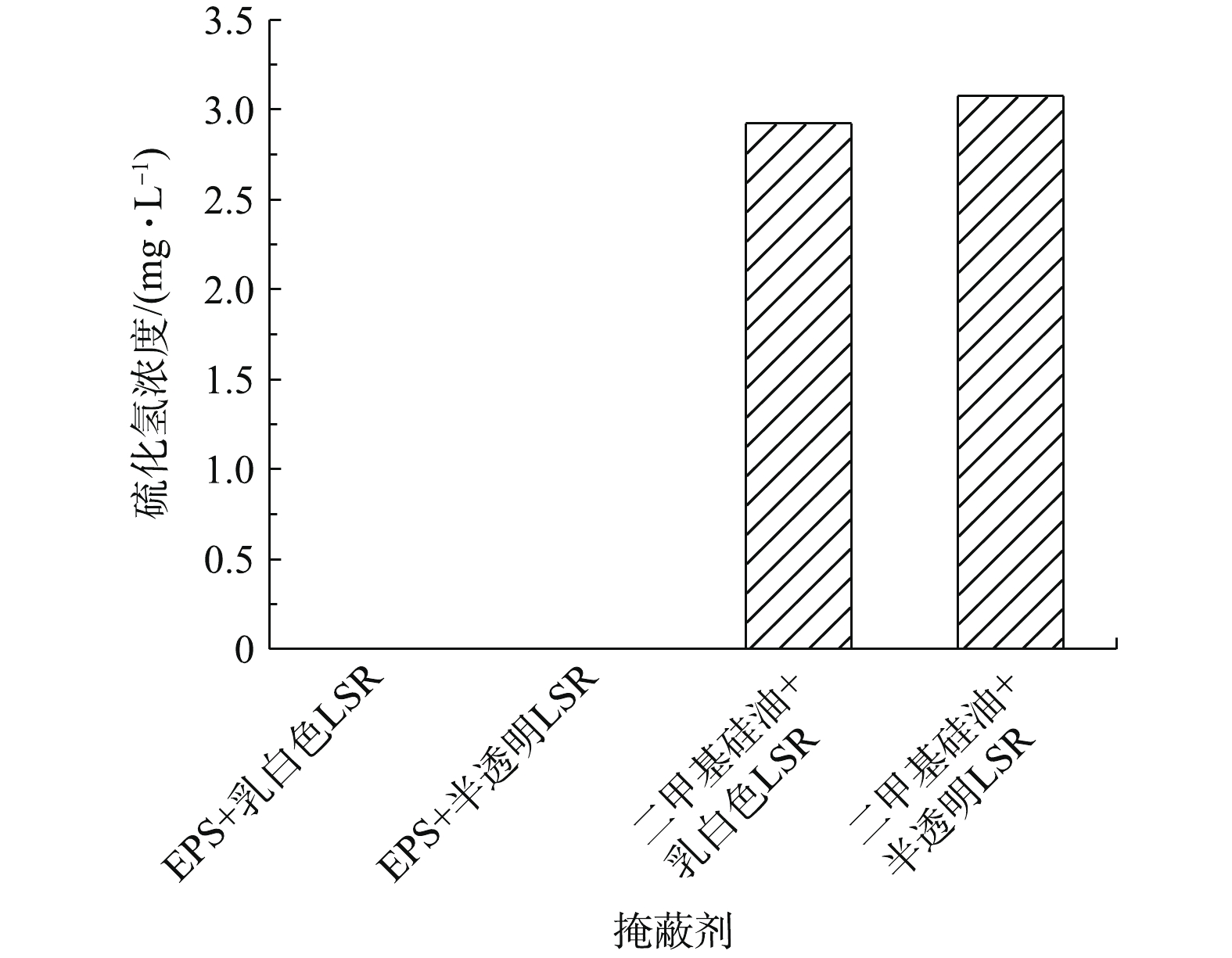
图3反映了LSR的密度对掩蔽效果的影响情况。由图3可知:在含有二甲基硅油和LSR的掩蔽剂中,均出现了H2S析出的现象;而以EPS作为载体的LSR,完全可以阻止H2S的析出。其原因可能有2种:二甲基硅油通过打断LSR的化学键,改善了LSR的黏度、流动性和密度,当黏度下降时,液相中的H2S分子通过热运动,更易扩散并穿透LSR;当二甲基硅油和LSR的混合物被覆盖在液体表面上时,该混合物形成的覆盖层内有二甲基硅油通路和LSR通路。因液体表面的H2S分子无法通过LSR通路进入大气,但因H2S可以扩散穿透二甲基硅油,所以被LSR通路阻挡的H2S扩散穿透二甲基硅油通路进入大气,进而使得掩蔽剂失效。
图4反映了不同种类LSR对掩蔽剂的影响情况。由图4可知,在4种不同配比下,乳白色LSR比半透明LSR质量变化更大。其原因在于,半透明LSR是利用硅胶原胶生产的,而乳白色LSR则充填CaCO3、白炭黑,因此,半透明LSR比乳白色LSR更抗拉抗撕,在水面处更易保持稳定的状态。
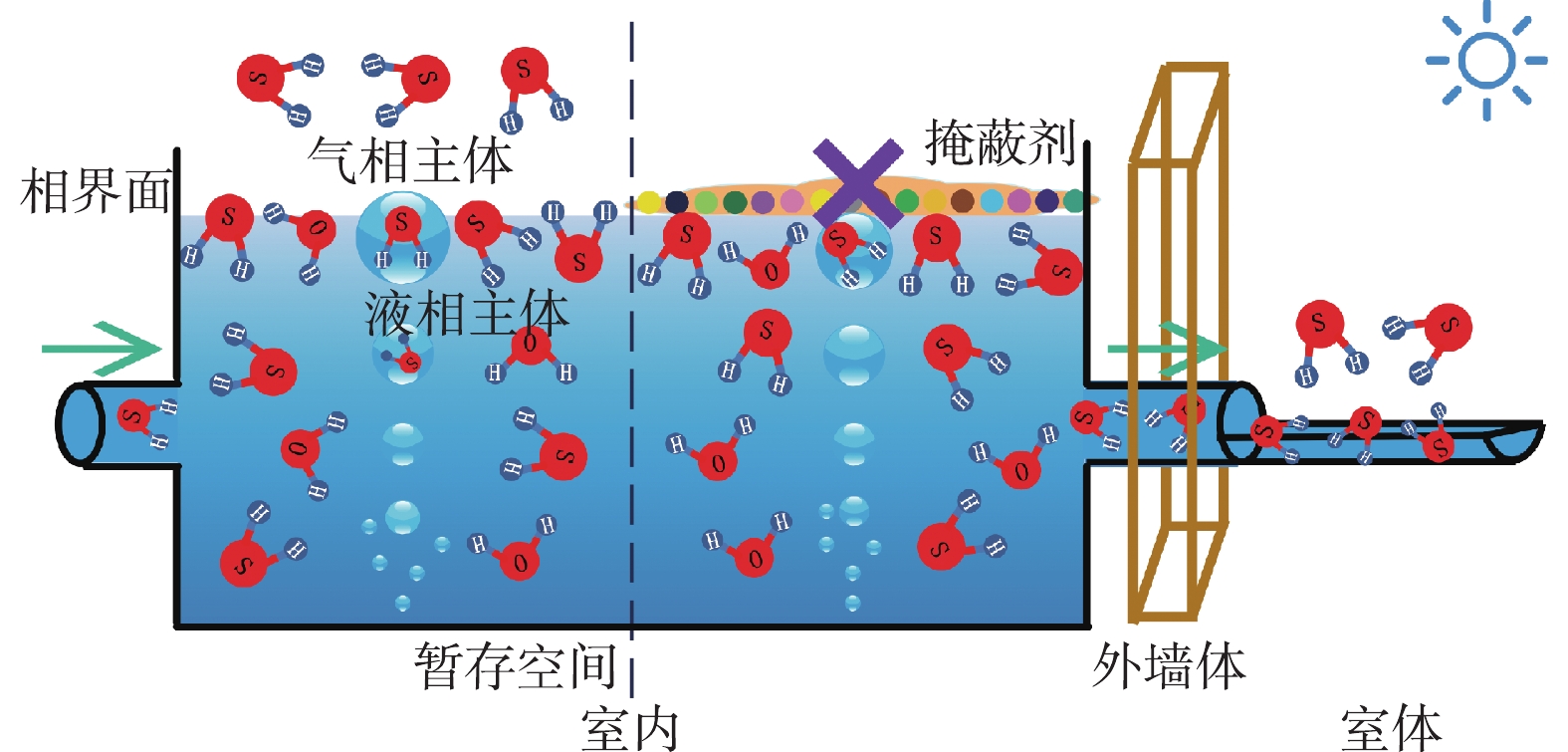
图5为掩蔽剂阻挡H2S的可能机理图。从宏观角度看,H2S产生于污水底部的底泥中,由于水流紊动,使局部压力降低,故导致H2S析出。当产生的H2S形成气泡后,其中的微气泡在水中可稳定存在,之后相互融合形成大气泡,或在表面张力的作用下适时泯灭;而其中的大气泡则在浮力作用下,一边溶解,一边上浮,若无法在到达液面前完全溶解,则气泡浮出水面后,会造成H2S的析出,从而进入气相中。此时H2S的析出,并不是因为水中的H2S已达到饱和,相反,水中还有很大的H2S容纳量。而掩蔽剂就是在气水界面处增大传质阻力,增加H2S气泡在水中的溶解时间,使H2S重新溶解进入水体中,从而不会释放到外部气相中。从微观角度看,相界面处液膜内的H2S分子依靠分子扩散进入气膜,随后进入气相主体中。但因掩蔽剂的传质阻碍,减少了H2S分子在液面处的扩散。
-
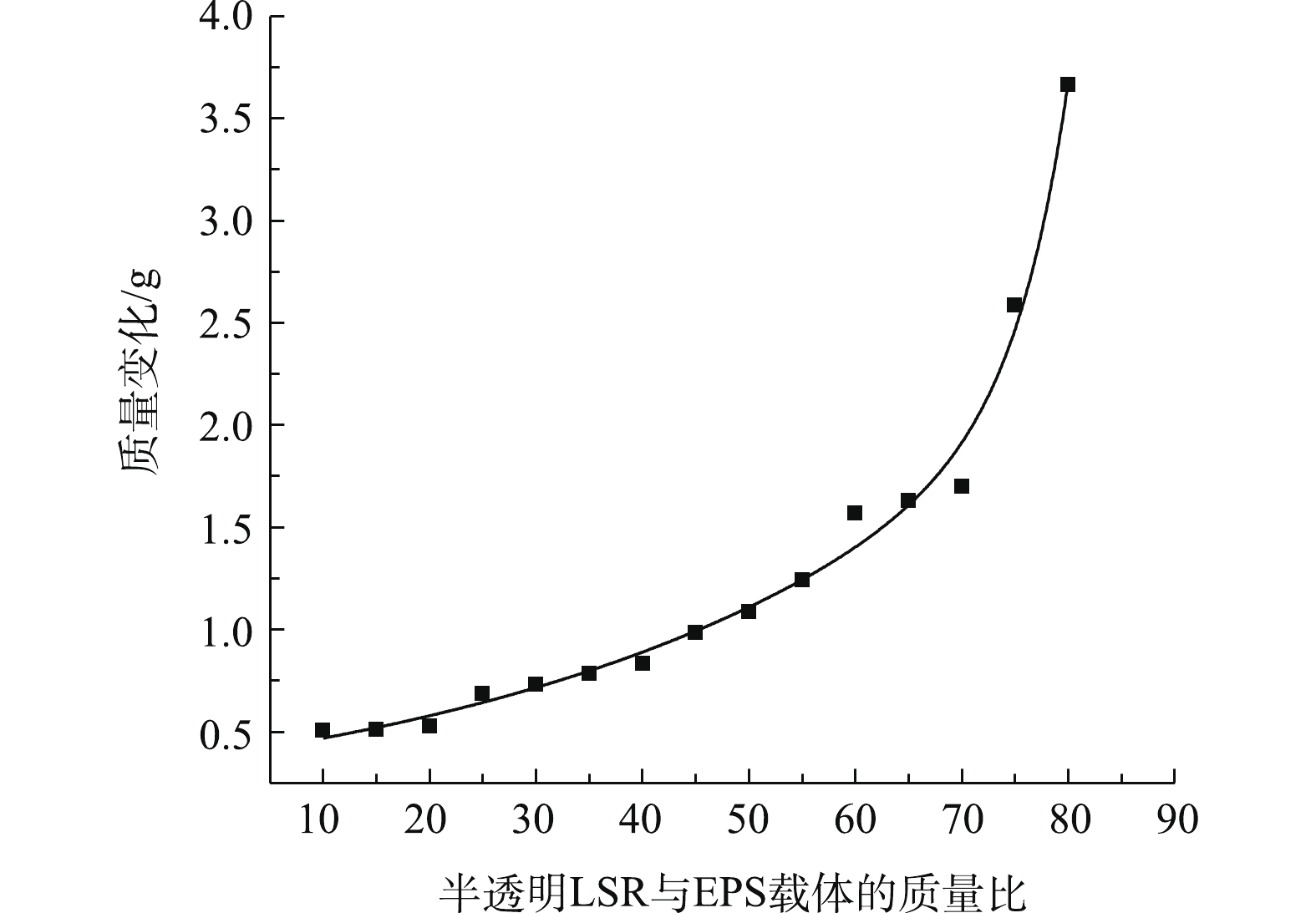
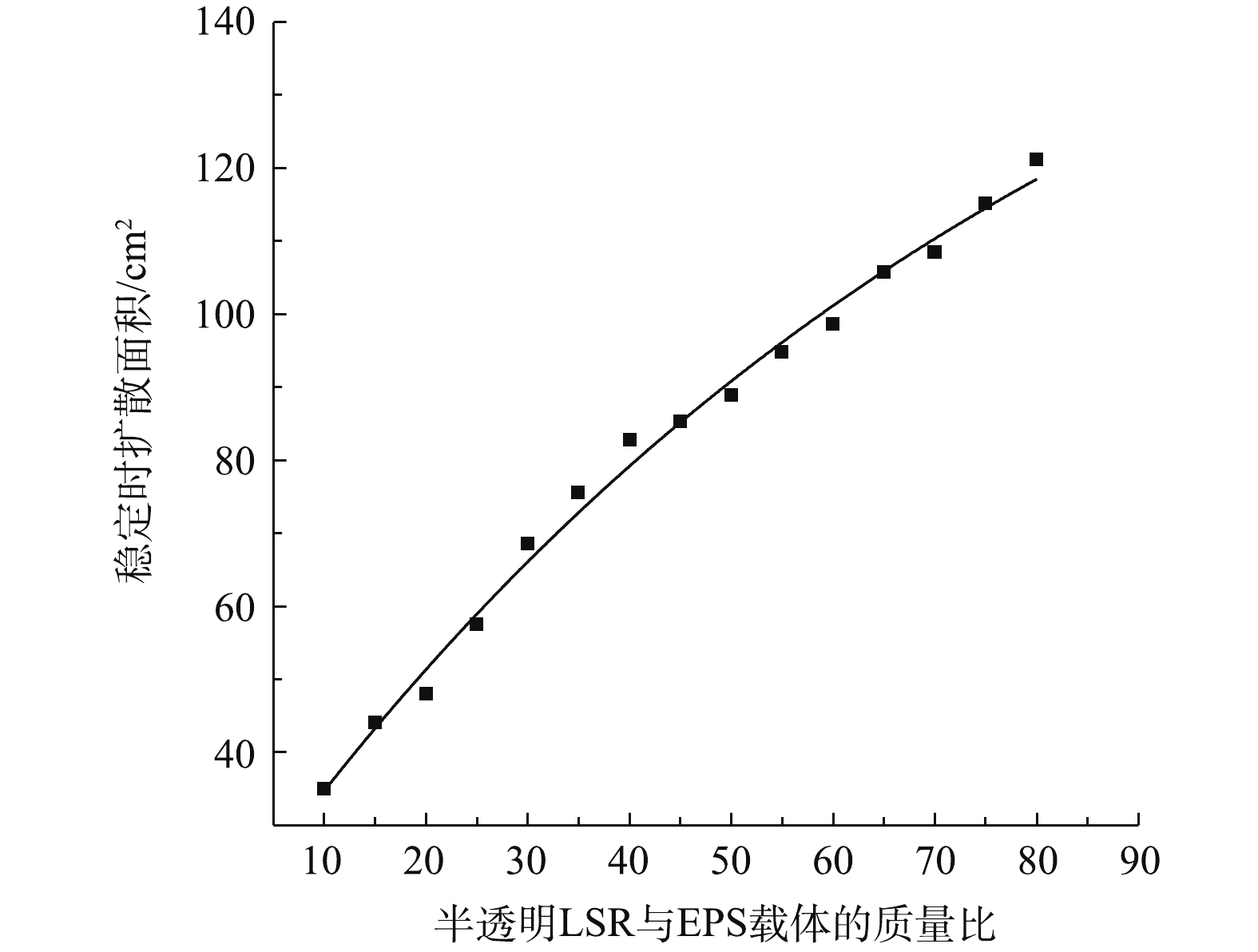
图6反映了半透明LSR与EPS在不同配比下对掩蔽剂的影响情况。由图6可知:在二者配比为10~70时,质量损耗变化较为平缓;当配比大于70时,质量损耗急剧增长。这是因为在较高的配比下,LSR与EPS载体之间的黏结性变差,大部分的LSR均不能附着在EPS上,其在重力作用下将会脱离层体结构。掩蔽剂质量变化越小,其稳定性越好。因此,为了使层体结构较稳定,二者配比应该为10~40。图7反映了半透明LSR与EPS载体在不同配比时对掩蔽剂流动性的影响情况。由图7可知,随着半透明LSR与EPS质量比的增加,掩蔽剂扩散面积也随之增加。其原因在于,随着LSR与EPS配比的增加,掩蔽剂流动性相应增加。但在配比逐渐增大的同时,扩散面积也趋于稳定,由于配比较大,导致EPS载体对LSR的流动性影响并不明显;而在配比较低时,LSR流动性受到EPS载体的影响较大。较好的流动性可以对掩蔽剂表面有一定的恢复作用。因此,结合图5和图6可知,当二者的配比为15~40时,稳定性和流动性均可以得到较好的满足。
-
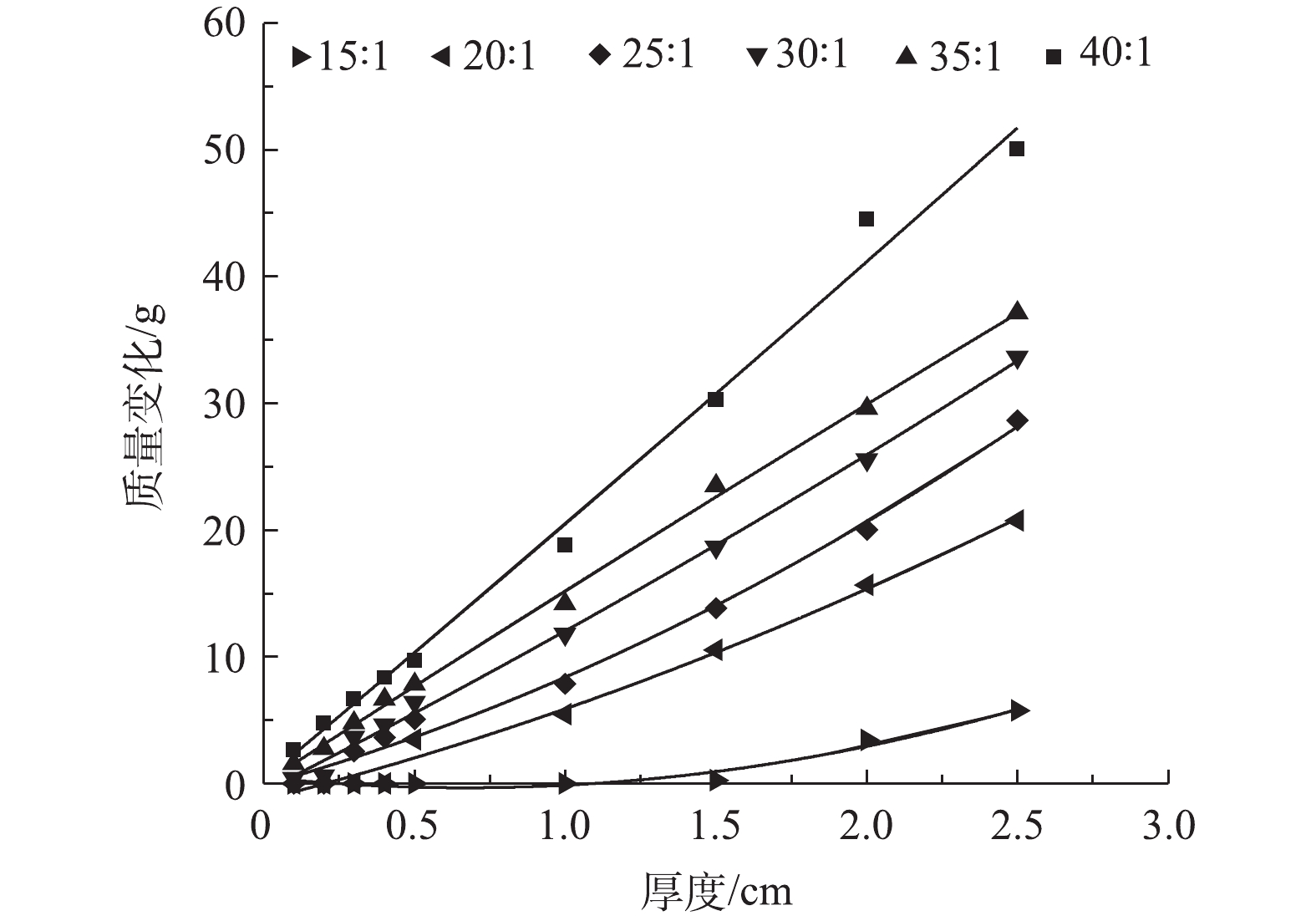
图8反映了掩蔽剂中LSR与EPS在6种配比下的相应平铺厚度对其稳定性的影响情况。由图8可知,在相同厚度下,二者配比越高,质量变化越大,导致其稳定性越差。而在同一配比下,随着厚度的增加,质量变化越大,导致稳定性变差。当LSR和EPS配比为15时,质量变化趋于平缓。随着配比的进一步增大,质量变化也越来越显著。其原因为:当厚度变大时,层体上部LSR会在重力作用下进入层体下部,从而出现明显的分层现象。因此,当配比为15~40时,最优的相应平铺厚度应为0.1~0.5 cm。
-
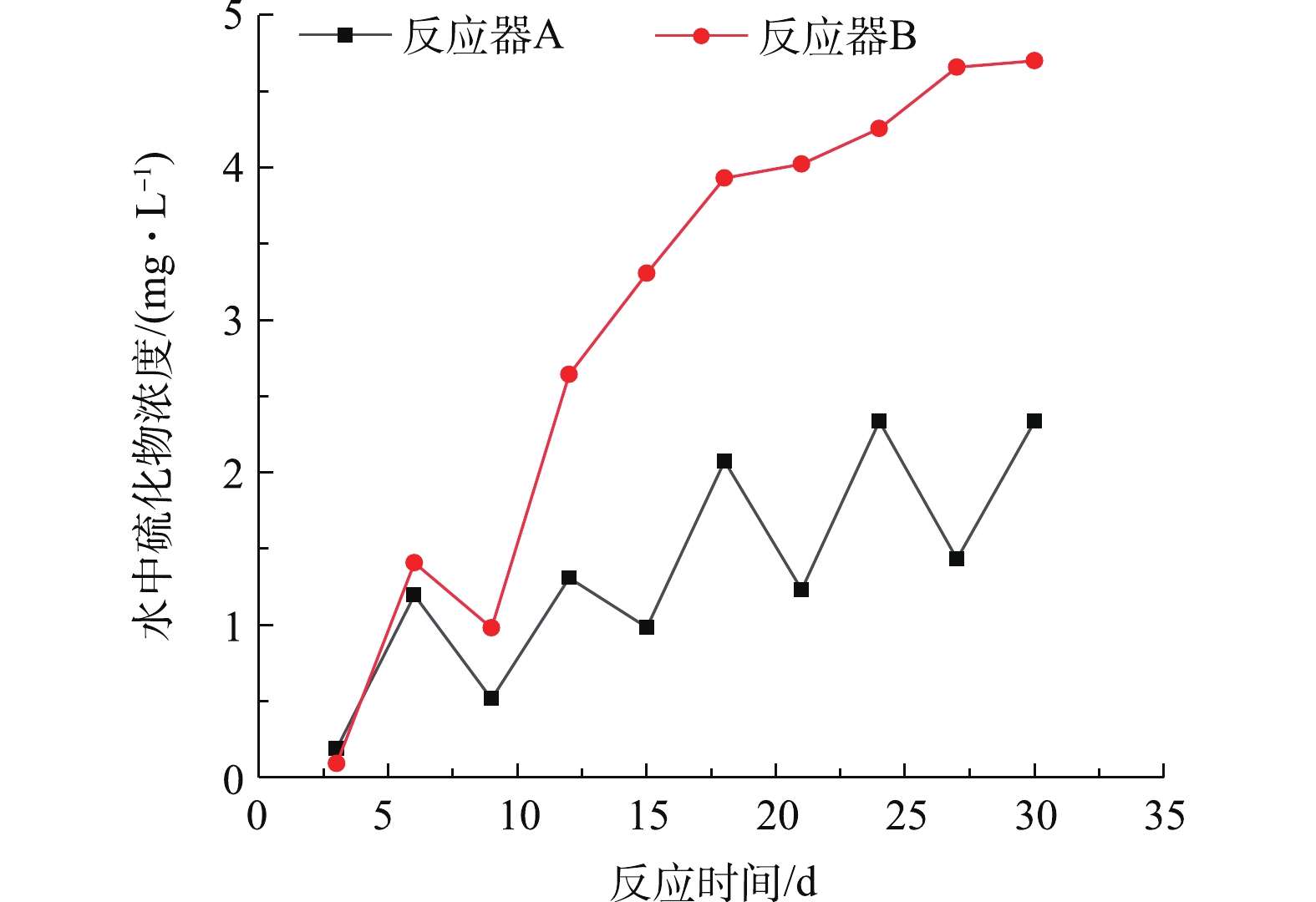
图9反映了反应器A和反应器B水体中的硫化物浓度随反应时间的变化情况。由图9可知,在反应器A中没有加入掩蔽剂,水中硫化物多以H2S形式释放。由于每次出水会使水中的硫化物随水流走,且进水会带入部分的溶解氧,因此,曲线会有所下降,之后由于SRB的作用,会使得水中硫化物再次上升。由于在反应器B中加入了掩蔽剂,虽然出水带走了部分硫化物,但厌氧环境使得SRB可以迅速恢复,所以导致水中硫化物含量呈缓慢增加的趋势。当停留时间较短时,水中的硫化物会伴随水流流走,导致其浓度增加较为缓慢;当停留时间较长时,水中的硫化物浓度有较快的上升。因此,H2S浓度能否达到SRB、产甲烷菌的毒性阈值,取决于污水停留时间及进出水量占池体水体的体积分数等影响因素。
2.1. 掩蔽剂对H2S的掩蔽效果比较及其机理分析
2.2. 不同配比掩蔽剂的稳定性与流动性比较
2.3. 不同平铺厚度掩蔽剂的质量变化
2.4. 掩蔽剂下部的水质变化及产物抑制分析
-
1)以半透明LSR+EPS为主体的掩蔽剂,可以增加气液传质阻力,对阻断H2S的释放效果较好,可以控制恶臭气体的有害影响。
2)为满足较好的稳定性和流动性,掩蔽剂中半透明LSR与EPS的配比应为15~40。在此配比下,掩蔽剂的使用效果较好。
3)掩蔽剂厚度过大时,不能忽略材料自身重力的影响。当重力大于层间黏滞力时,组分会发生分离,对掩蔽剂性质会有一定的影响。当平铺厚度降低至0.1~0.5 cm时,层体分离现象会消失或变得不明显。
4)掩蔽剂下部水体硫化物的浓度随着污水停留时间的增加而增大。当污水停留时间较小时,硫化物浓度不高;停留时间较长时,硫化物浓度会有所上升。H2S能否达到产物抑制的浓度,不仅和污水停留时间有关,也与进出水量占池体水体的体积分数有关。



 下载:
下载: