-
随着工业生产的发展,致酸性气体大量排放,导致环境中酸沉降严重;加之农业生产中氮肥的不合理施用,我国土壤的酸化程度日益加剧[1]。酸化导致土壤整体质量下降,交换性酸增加,盐基离子流失过快,有效肥力下降,有机质含量减少,影响了作物的生长。其中,强酸化土壤危害更为严重[2-3],探索研究有效的酸化土壤的改良方法显得尤为重要。
现有的酸化土壤改良方法能起到一定效果,但也存在不足。施加生石灰的传统方法能快速提升土壤pH,是目前的主流方法。但大量或长期施用易导致土壤板结,不利于作物生长[4]。据冀建华等[5]报道,施用磷石膏、碱渣等工业副产品也能降低土壤酸度,但会导致土壤中阳离子成分失衡,且其中可能含有重金属成分。施用养殖废弃物、作物秸秆及其制备的生物炭碱性较低,对于强酸化土壤改良效果不明显[6-7]。同时,大量施加上述改良剂短时间内不宜农作物种植,需要通过长时间的缓耕或休耕,如此改良后的土壤还可能出现复酸情况[8],且在种植过程中仍需施加大量肥料。
据汤秋云等[9]研究发现,蛋白多肽可作为一种高效有机肥促进植物生长(5~7 d变绿,肥效持久),并且蛋白多肽呈碱性。基于此,本研究根据蛋白多肽既具有生石灰的优点,又具有有机肥的功能,研究其对强酸化土壤的改良效应,以期达到施肥就能直接解决土壤酸化问题,实现强酸化土壤改良与作物种植同步化进行,克服强酸化土壤改良过程中不能种植的缺点。
全文HTML
-
本实验供试土样选取湖北省恩施州利川市汪营镇石坝村农田(30°17´N,108°40´E,海拔1 122 m)酸化黄黏土,样品均采自去除覆盖物杂质的0~30 cm表层土,运至实验室。自然风干后,将土样中的石粒及肉眼可见的动植物残体去除,粉碎过2 mm 尼龙筛,混合均匀,备用。测得供试土样pH为4.30,全氮、有效磷、速效钾和全钙含量分别为90.24、43.83、78.31和196.20 mg·kg−1,有机质含量为10.03 g·kg−1,容重为1.13 g·cm−3,阳离子交换量(CEC)为5.62 cmol·kg−1。
-
供试作物为十字花科芸薹属的结球甘蓝,选用中国农科院蔬菜花卉所育成的“京丰一号”春冬季品种。结球甘蓝属于高山蔬菜,富含营养物质,较耐酸[10],在恩施州当地普遍种植。近年来,由于土壤酸化程度加重,极大地影响了结球甘蓝的生长,此为所选供试土样与作物的依据。
-
供试材料是以含蛋白植物饼粕为原料,将氧化钙和氢氧化钾与之混合,在120~150 ℃条件下转化为全水溶性蛋白多肽,平均分子质量在5 kDa左右,由本实验室自主研发制备。制备的蛋白多肽pH为10.85,全氮、全磷、全钾和全钙含量分别为90.53、0.36、71.62和53.20 g·kg−1。
-
WYS2200型原子吸收分光光度计(安徽皖仪科技股份有限公司);FSP6650火焰光度计(上海悦丰仪器仪表有限公司);PB-10pH计(德国赛多利斯Sartorius)。
-
在进行土壤培养实验时,设置4个实验组合,即仅施加复混肥空白组(CK)、施加生石灰和复混肥的生石灰组(SH)、施加氢氧化钾和氮、磷肥的氢氧化钾组(KOH)、仅施加蛋白多肽的蛋白多肽组(KDT),每个组合进行3次重复。各实验组合采用模拟施肥方法:按结球甘蓝全生长期的需氮量(约700 kg·hm−2)计算,即1 kg土壤需施氮量约为1.0 g,结球甘蓝生长需氮磷钾比例约为3∶1∶4[11];复混肥组和生石灰组按常规施肥方式施加复混肥,生石灰按酸化土壤石灰需求量施加[12],氢氧化钾依据多肽中含钾量施加。其中,各实验组1 kg土壤中的施加成分以及施加量为:复混肥组仅施加7.20 g复混肥;生石灰组施加7.20 g复混肥和1.40 g生石灰;氢氧化钾组施加2.12 g尿素、1.25 g过磷酸钙和1.20 g氢氧化钾;蛋白多肽组仅施加10.36 g蛋白多肽。
将4个处理组中模拟施肥成分分别加入到500 g装于塑料杯的土壤中充分混合均匀,添加去二氧化碳超纯水,调节含水量为土壤田间持水量的70%。采用恒温好气培养法[13],用带有孔隙的聚乙烯塑料膜将烧杯封口,用橡皮筋扎紧,目的是保证土壤培养体系呈通气状态又不使水分蒸发散失过快,然后将各处理以随机排列方式放置于25 ℃的恒温培养箱中培养,每隔3 d称重1次并补充水分,保持土壤含水量恒定,最终的培养时间为120 d。在培养开始后的第1、3、5、7、10、15、20、30、60、90和120天,取新鲜土样测定pH动态变化,培养结束后,测定土壤的交换性酸、交换性盐基离子、CEC和有机质含量。
2018年11月17日开始进行结球甘蓝种植实验。实验以盆栽方式进行,与土壤培养实验对应,设置4个处理,即复混肥组(CK)、生石灰组(SH)、氢氧化钾组(KOH)、蛋白多肽组(KDT),每个组合进行9次重复,共36盆。称取4 kg过2 mm筛的风干土壤,按土壤培养模拟施肥方案施加不同处理组成分,混合均匀后,装于内直径为20 cm、高为15 cm的塑料花盆中,加水至土壤含水量在田间持水量的70%左右(用称量法保持花盆中土壤的水分)。移栽已培育至高10 cm左右长势相同的结球甘蓝(京丰一号春冬季品种)幼苗,生长过程中模拟室外环境调控光照、温度、保持土壤湿度,共计培养120 d,于2019年3月15日收获。在种植后的第10、30、60和120天,测定土壤pH,在结球甘蓝生长的第30、90和120天,拍照记录长势,在第120天收获,测定土壤容重和结球甘蓝平均生物量。
-
土壤pH采用复合电极pH计(土水比1∶2.5)[14]测定;土壤有机质含量采用重铬酸钾-硫酸溶液外加热法[15];土壤容重采用环刀法[16];土壤的交换性盐基离子用乙酸铵浸提原子吸收分光光度法[17]测定;土壤CEC用乙酸铵交换法[18]测定;土壤交换性酸采用氯化钾交换-中和滴定法[19];土壤的有效磷和速效钾的测定采用联合浸提-比色法[20]。
1.1. 供试土壤
1.2. 供试植物
1.3. 供试材料
1.4. 实验仪器
1.5. 实验设计
1.6. 测试方法
-
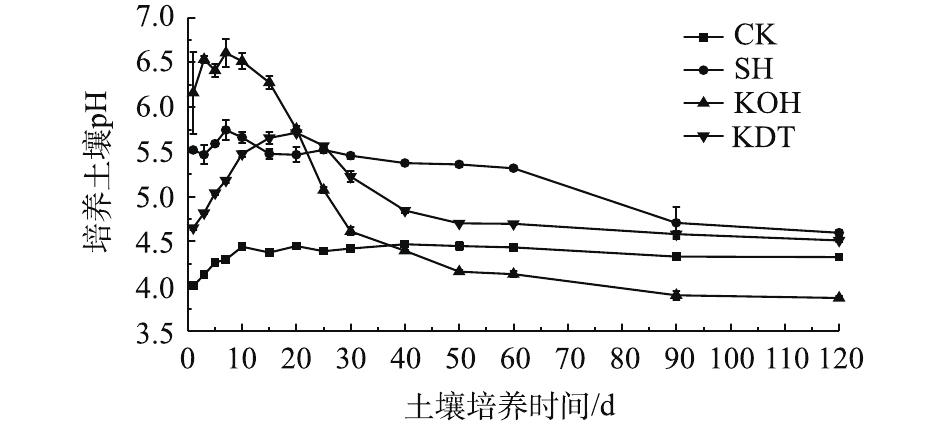
pH是酸化土壤改良最为重要最为直观的指标。在土壤培养的第1、3、5、7、10、15、20、30、40、50、60、90和120天进行pH的动态测定。结果表明,生石灰和蛋白多肽均能提升土壤pH。如图1所示,在土壤培养的第30天,生石灰组pH最高(5.46),其次是蛋白多肽组(5.22),复混肥组最低(4.42)。在30 d前,复混肥组和生石灰组pH变化较平稳,氢氧化钾组起始pH最高,然后迅速降低,蛋白多肽组pH先持续提升后较缓慢降低。随着培养时间的进行,在第60天,生石灰组pH最高(5.32),其次是蛋白多肽组(4.70),氢氧化钾组最低(4.13)。60 d之后,蛋白多肽组和复混肥组pH基本保持稳定,而生石灰组和氢氧化钾组处于降低趋势,培养至第120天基本保持稳定。最终,生石灰组(4.60)和蛋白多肽组(4.53)土壤pH与初始值(4.30)相比分别提高了0.30和0.23个单位,复混肥组提高了0.02个单位,而氢氧化钾组比初始值还降低0.43个单位。生石灰按土壤的石灰需求量添加,土壤pH提升较高且稳定。这是由于生石灰碱度高,含有的大量钙素在土壤中稳定性好。但随着时间的增加(在土壤培养至60 d后),pH也会出现缓慢降低的趋势,这与朱经伟等[21]的研究结果一致。氢氧化钾为强碱性物质,加入土壤后,pH提升最高,下降也最迅速。这是由于加入的大量氢氧根对土壤体系产生刺激,与土壤中的二氧化硅发生反应。汪吉东等[22]的研究表明,有机氮发生矿化反应,转化为无机氮(铵态氮),消耗土壤中的H+,这一过程使土壤pH提高,铵态氮在土壤中进行硝化反应,转化为硝态氮释放H+。这一过程使土壤pH降低,蛋白多肽中含有大量稳定的有机氮,在土壤培养开始时发生矿化反应,使土壤pH持续提升至第20天,而后硝化反应速率大于矿化反应,土壤pH出现降低趋势,直至第50天才保持平稳。由于蛋白多肽矿化总量大于硝化反应量,并且蛋白多肽呈碱性,总的来说,蛋白多肽对强酸化土壤具有明显的碱化效应。以上结果表明,生石灰提升土壤pH效果最明显,其次是蛋白多肽,氢氧化钾不能有效提升土壤pH。
-
交换性酸是土壤中的潜在酸,包括交换性氢和交换性铝,可以转化为活性酸,是土壤酸度容量的重要指标[23]。在土壤培养实验结束时测定交换性酸的含量,其中,交换性酸与交换性氢差值为交换性铝。如表1所示,生石灰组和蛋白多肽组与复混肥组相比均显著降低了土壤中交换性酸含量。其中,交换性氢和交换性铝也都显著降低。与复混肥组相比,氢氧化钾组虽然降低了交换性氢含量,但是显著增加了交换性铝含量,这导致交换性酸与复混肥组相比显著增加。在4个实验组土壤交换性酸中,交换性铝含量远多于交换性氢,这与何淑勤等[24]的研究结果一致。生石灰组、氢氧化钾组和蛋白多肽组交换性铝占比均大于复混肥组。这是由于,复混肥碱度低不能降低土壤酸度,而其他3个组合碱度高,能直接降低H+含量,相应的交换性铝占比增加。以上结果表明,生石灰和蛋白多肽能够有效降低强酸化土壤中的潜在酸含量。
-
酸化使土壤中H+浓度增加,与钠、钾、钙、镁等盐基离子竞争交换位点,使这些盐基离子大量淋失,土壤交换性能降低[25]。为了检测不同实验组土壤交换性能的情况,在土壤培养结束后测定交换性钠、钾、钙、镁离子含量和阳离子交换换量(CEC),结果如表2所示。可以看出,生石灰组和蛋白多肽组交换性盐基总量与复混肥组相比显著增加,氢氧化钾组与复混肥组之间无显著差异。对于土壤中的阳离子交换量(CEC)来说,生石灰组、氢氧化钾组、蛋白多肽组与复混肥组相比均显著增加。土壤盐基饱和度为交换性盐基总量与CEC之比。生石灰组盐基饱和度最高;其次是蛋白多肽组;复混肥组较低;氢氧化钾组最低。生石灰组交换性能最好。这主要是由于施加生石灰后补充大量的钙,直接显著增加交换性钙离子含量。蛋白多肽组也能有效提升土壤交换性能。这是由于蛋白多肽自身含有钾、钙等盐基离子;也可能是由于其所含有机成分中的β-OH等特殊功能基团与盐基离子耦合成稳定结构,从而减少盐基离子的交换流失[26]。氢氧化钾组与复混肥组相比交换性盐基总量无显著差异。这由于交换性酸的显著增多使CEC显著增加,降低了盐基饱和度,反而减弱土壤的交换性能。由此表明,生石灰提升强酸化土壤的交换性能效果最好,蛋白多肽仅次于生石灰。
-
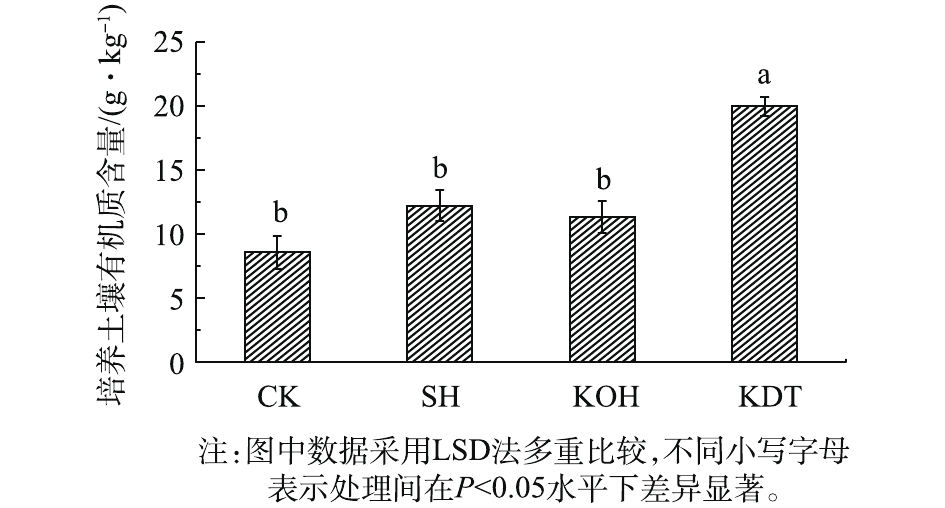
土壤有机质是土壤有机物质的主体,能吸附大量的盐基离子;同时也能降低酸化土壤中的铝毒害,增强土壤抗逆性。土壤有机质含量是反映土壤整体质量情况的重要指标,是衡量酸化土壤改良效果的重要依据[27-28]。在土壤培养结束时对其进行测定,结果如图2所示。可以看出:蛋白多肽组土壤有机质含量最高(19.96 g·kg−1),比复混肥组(8.58 g·kg−1)显著增加11.37 g·kg−1;生石灰组(12.23 g·kg−1)和氢氧化钾组(11.33 g·kg−1)与复混肥组相比无显著差异。复混肥组与氢氧化钾组土壤的酸度较高,降低土壤微生物的活性,有机物质不稳定,导致土壤的有机质含量较低[29]。据NILSSON等[30]的报道,施加生石灰使土壤产生矿化作用,在一定程度上增加了土壤的碳排放,对有机质含量的提升无显著作用,甚至会降低土壤有机质含量;蛋白多肽本身所含的有机成分可转化为土壤中稳定的有机物质,能显著提高土壤的有机质含量,更有利于提升强酸化土壤的整体质量。
-
由于植物生长需要吸收土壤中的养分(尤其是氮肥),这会对土壤pH产生影响[31]。与土壤培养实验相比,探究在种植的条件下施用蛋白多肽是否仍能提高土壤pH,因此,在种植结球甘蓝后的第10、30、60和120天对土壤pH进行测定,结果如图3所示。在同步化种植结球甘蓝过程中,各处理组土壤pH的变化趋势与土壤培养实验结果基本一致。在种植后的第10天,生石灰组、蛋白多肽组和氢氧化钾组土壤pH与复混肥组相比均显著增加。随着培养的继续,氢氧化钾组土壤pH迅速降低,生石灰组和蛋白多肽组降低趋势较缓慢。最终,在结球甘蓝种植结束时,生石灰组(4.66)和蛋白多肽组(4.62)土壤pH分别比复混肥组(4.27)显著增加0.39和0.35个单位,氢氧化钾组(4.18)比复混肥组降低0.09个单位。与土壤培养实验相比,生石灰组、蛋白多肽组和氢氧化钾组种植结球甘蓝的土壤pH有进一步提高。这可能是由于结球甘蓝为偏喜铵态氮肥作物,在苗期生长较快时,从土壤中吸收大量的铵态氮[10],从而减缓土壤中的硝化反应速率。由此可知,在同步化种植结球甘蓝的条件下,生石灰和蛋白多肽均依然能显著提升强酸化土壤的pH。
-
在结球甘蓝移栽种植后的第30、90和120天进行拍照记录长势,结果如图4所示。结球甘蓝生长至第30天处于苗期,由图4(a)可知,各处理组长势已有明显差别,蛋白多肽组结球甘蓝长势最好,其次是氢氧化钾组,复混肥组最差;在图4(b)中,结球甘蓝生长至第90天处于结球期,复混肥组长势最差,生石灰组和氢氧化钾组长势一致,蛋白多肽组长势仍明显好于其他组,并且蛋白多肽组结球甘蓝能正常结球,而其他组未出现结球趋势;结球甘蓝生长至第120天开始收获,生长情况如图4(c)所示,蛋白多肽组结球较紧实,且生物量明显较高,而其他处理组仍未出现结球。在结球甘蓝的整个生长期,蛋白多肽组长势最好,没有出现烂根烂叶现象,且能正常结球。由此表明,蛋白多肽能促进结球甘蓝的正常生长且效果显著。
-
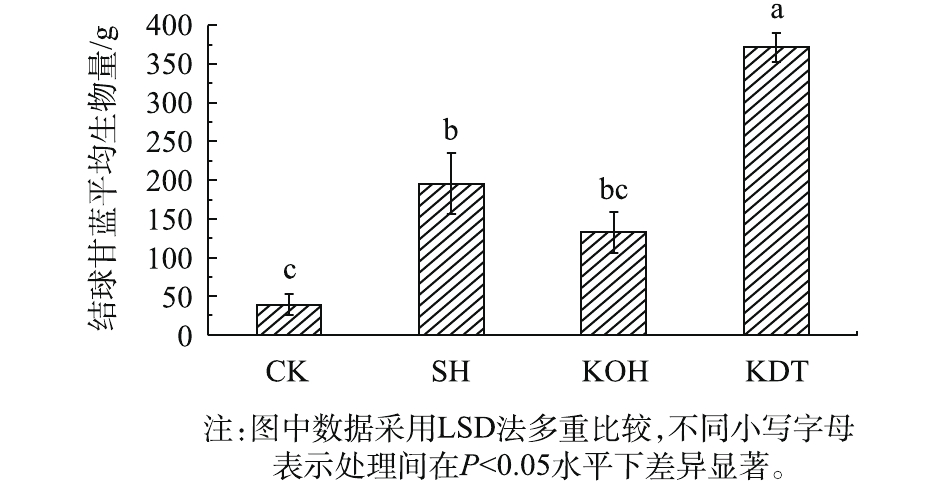
在结球甘蓝生长至第120天进行收获,测定各组合结球甘蓝的平均生物量,结果如图5所示。可以看出,与复混肥组相比,蛋白多肽组、生石灰组和氢氧化钾组均能提高结球甘蓝生物量。其中,蛋白多肽组结球甘蓝平均生物量最高(371.78 g),且显著高于其他组合,是复混肥组(38.97 g)的9.54倍,是生石灰组(195.47 g)的1.90倍,是氢氧化钾组(132.79 g)的2.80倍。结球甘蓝可生长于偏酸性土壤,苗期能承受土壤pH阈值约为5.0,苗期过后植株具有一定抗逆性[32],生石灰、氢氧化钾和蛋白多肽均能使结球甘蓝苗期土壤pH升高至5.0左右,与复混肥相比均能增强结球甘蓝抗酸性。除此以外,蛋白多肽增加土壤有机质含量,提升土壤的抗逆性,提供持效养分,更有利于结球甘蓝在偏低pH条件下生长。由此表明,蛋白多肽能够保证结球甘蓝在酸化土壤中的正常生长,并且能提高结球甘蓝产量,具有很好的种植效果。
2.1. 蛋白多肽对培养土壤pH的影响
2.2. 蛋白多肽对培养土壤交换性酸含量的影响
2.3. 蛋白多肽对培养土壤交换性能的影响
2.4. 蛋白多肽对培养土壤有机质含量的影响
2.5. 蛋白多肽对种植土壤pH的影响
2.6. 蛋白多肽对结球甘蓝生长的影响
2.7. 蛋白多肽对结球甘蓝产量的影响
-
1)酸化土壤改良的第一指标是pH,施加生石灰的传统方法可快速提高土壤pH,在目前的应用最为广泛;蛋白多肽也可显著提高土壤pH,具有同样的碱化效应,可用于酸化土壤改良。
2)利用蛋白多肽与生石灰进行土壤改良具有本质的区别。蛋白多肽是一种有机肥,利用蛋白多肽改良酸化土壤后无需再施肥;而且,所种植作物的生物量显著高于生石灰改良再施加复混肥的生物量。
3)蛋白多肽与生石灰对酸化土壤具有相似的碱化改良效应,均难以将强酸化土壤一次性改良至pH为6.5以上的中性程度。但是,经蛋白多肽修复的土壤,可在低pH条件下种植出优质高产的结球甘蓝,实现强酸化土壤改良与种植的同步化,具有对强酸化土壤递进式改良的潜力。



 下载:
下载: