纳米二氧化钛(titanium dioxide nanoparticles, TiO2 NPs)具有良好的光学特性,同时化学性质较为稳定,特殊的性质决定了其广泛的用途。目前TiO2 NPs已被广泛应用在涂料生产、污水治理、气体净化、抗菌杀菌、化妆品制造、食品包装和特殊医疗技术等各个方面,颜料、纸、纤维、陶瓷、食品、化妆品和药品等产品制造中都有TiO2 NPs的使用[1-5]。由于TiO2 NPs的尺寸小、比表面积大,具有良好的紫外线吸收反射能力,化学惰性,热稳定性及不溶性,有较好的白度和着色性,故而被广泛地应用于个人护理品(personal care products, PCPs),特别是牙膏、防晒霜和粉底液等有增白和防晒需求的产品中[6]。我国《化妆品安全技术规范》(2015年版)中规定二氧化钛(titanium dioxide, TiO2)是准用着色剂和防晒剂[7]。
目前PCPs中TiO2 NPs含量的研究已经引起了国内外有关学者的关注。Zachariadis和Sahanidou[8]和Botta等[9]均利用电感耦合等离子体原子发射光谱(ICP-AES)对面膜、防晒霜等产品中的TiO2含量进行了测定。Contado和Pagnoni[10]提出了利用方波伏安法(square wave voltammetry, SWV)测定商业基础霜中TiO2含量,但该方法容易受到Cu2+的干扰。Weir等[11]利用电感耦合等离子体质谱(ICP-MS)对牙膏、防晒霜和洗发水等产品中的TiO2含量进行检测,但样品的预处理采用硝酸、氢氟酸和双氧水进行消解,步骤较为繁琐并且安全风险较大。
国内也有少数防晒化妆品中TiO2含量测定的研究。王传庆[12]利用单宁酸与安替比林选择性沉淀Ti4+的方法对10种防晒化妆品的TiO2含量进行了测定,包括3种粉底霜、3种粉饼、2种粉条和2种防晒霜。陈昌等[13]利用钛与二安替比林甲烷在强酸中形成黄色络合物的原理对10种防晒化妆品进行了分光光度法测定。
PCPs中TiO2 NPs的广泛使用和释放导致人们关注其对人体的健康风险。已有的研究主要从呼吸道吸入、皮肤接触和经口摄入等暴露途径考虑其对消化道、心血管系统和神经系统造成的健康风险[14-18]。但是目前针对人体的实验数据较少,主要是以鼠、猪、藻类和细胞等为研究对象。一些针对鼠类的吸入研究表明TiO2 NPs可能会引发肺部炎症和组织损伤[19]。关于TiO2 NPs能否透过表皮进入皮肤深处的问题也有不同的研究结果[17, 20]。而针对藻类和细胞的研究发现TiO2 NPs可能存在氧化胁迫效应或影响细胞的转录过程[21-23]。以上研究是通过实验的方法评估TiO2 NPs的健康风险,而通过模型评估也是重要的方法。李伟[24]通过计算比较人体针对食品中TiO2 NPs的暴露范围和可接受范围,认为TiO2 NPs对肝脏和脾脏的风险不大,但不排除对生殖系统的影响。本研究采用的美国环境保护局(US EPA)推荐的人体健康风险评价模型也是常用的评价方法之一[25]。
利用单颗粒电感耦合等离子体质谱(spICP-MS)进行单颗粒的粒径分布和数量信息检测是近年来新兴的一种测定技术[26-29]。梁维新等[28]利用超声辅助提取了防晒化妆品中的TiO2 NPs颗粒。通过对比不同种类和浓度的提取剂的提取效果,确定了0.1%曲拉通-100(Triton X-100, TX-100)和5%乙醇的混合溶液作为提取剂的提取效果最好。实验得出的spICP-MS的粒径检出限在35 nm,颗粒浓度检出限约为1×104 个·mL-1,在低于4×107 个·mL-1的数量浓度时可以对防晒化妆品中的TiO2 NPs颗粒进行准确测定。王丹红等[29]在2018年利用强碱四甲基氢氧化铵对食品中的TiO2 NPs进行了提取,然后利用spICP-MS进行了粒径分布和颗粒浓度的测定。实验结果表明四甲基氢氧化铵的提取效果较好,粒度检出限在45 nm,颗粒浓度检出限约为8.3×105 个·mL-1。单颗粒的测定中提取剂的选择与用量、粒径检出限和颗粒浓度检出限等是影响检测结果的重要因素。
TiO2 NPs在PCPs中的大量使用可能存在的健康风险引起了广泛关注,但是目前对于PCPs中TiO2 NPs含量和粒径分布的定量检测研究较少,研究方法也具有一定的局限性。为了进一步了解目前我国市场上PCPs中TiO2 NPs的使用情况,合理筛选市售PCPs作为研究对象,利用ICP-MS对样品中的钛含量进行定量检测并利用US EPA推荐的人体健康风险评价模型计算钛的非致癌风险商(hazard quotient, HQ)。同时利用spICP-MS这种新兴的检测技术对PCPs中的TiO2 NPs进行检测,定量分析其粒径分布特征。
1 材料与方法(Materials and methods)
1.1 材料
本研究所用的浓硝酸、浓硫酸和硫酸铵均为购自上海阿拉丁生化科技股份有限公司的分析纯试剂。钛单元素标准溶液(中国计量科学研究院,100 mg·L-1)用于制备标准曲线以测定钛含量。选择硫酸-硫酸铵溶液(将60 g硫酸铵加入100 mL浓硫酸中,加热至80 ℃以上并不断搅拌直至溶液澄清透明)溶解TiO2。TiO2 NPs标准品购自美国纳米材料研究公司(US Research Nanomaterials, Inc.),晶型为金红石型,粒径为100 nm,纯度>99.9%,表面具有聚乙烯比咯烷酮(polyvinyl pyrrolidone, PVP)包覆层。选择TX-100提取TiO2,购自上海阿拉丁生化科技股份有限公司,纯度为生化试剂级。实验用水均为超纯水(泽拉布仪器科技(上海)有限公司,Dura 12FV)。实验仪器主要有消解仪(德国WTW,CR3200)和电感耦合等离子体质谱仪(Perkin Elmer,美国,NexION 350D)。实验用玻璃仪器均在酸缸中浸泡过夜后用超纯水冲洗干净。
1.2 PCPs来源
本研究选用了23种PCPs产品(表1),其中包括9种牙膏、10种防晒类产品、2种洁面类产品和2种面膜类产品。产品采购自京东(https://www.jd.com/)、淘宝(https://www.taobao.com/)等电商平台及某超市(北京昌平)。产品的状态描述参考我国推荐标准《化妆品名词术语》(GB/T 27578—2011)[30]。我国《化妆品安全技术规范》(2015年版)中规定TiO2作为着色剂使用时的索引号为CI 77891,索引通用名为颜料白6(pigment white 6),在各类化妆品中使用时应当在商品标签中注明[7]。上述产品中均未标明TiO2的具体浓度及粒径信息。
1.3 总钛含量测定
TiO2 NPs不易消解,在对比不同文献消解方法的基础上,综合考虑成本及安全因素采用了Liang等[31]的消解方法,即采用硫酸-硫酸铵溶液消解。称取0.05 g左右的样品并加入2 mL浓硝酸和1 mL硫酸-硫酸铵溶液后置于消解仪中在148 ℃下加热2 h。余热赶酸结束后待冷却至室温再定容至10 mL。接着将定容后的溶液转移到10 mL的离心管中在4 000 r·min-1下离心10 min。待离心结束取上清液稀释过膜后使用ICP-MS进行测定。
1.4 TiO2 NPs粒径分布测定
为确定PCPs中TiO2 NPs的含量及粒径分布,按照梁维新等[28]的方法对PCPs样品进行前处理。具体方法是称取0.05 g左右的样品于100 mL的锥形瓶中,用0.1%TX-100+5%乙醇的混合溶液定容至50 mL。然后利用振荡混匀器充分混匀后置于超声波发生器中超声提取30 min。待超声结束后取混合溶液稀释过膜后使用spICP-MS进行测定。1.4与1.3除样品的消解步骤不同外,在ICP-MS的使用模式上也有所不同。在进行粒径分布的测定时,需将ICP-MS调整为时间分辨率模式,此时测定的实验仪器的参数设置如表2所示。
1.5 人体健康风险评价
本研究采用US EPA推荐的人体暴露健康风险评价模型对PCPs中钛的健康风险进行评价[25, 32]。本研究中将TiO2作为非致癌物质来考虑其健康风险。使用公式(1)~(3)计算了TiO2的皮肤日均吸收剂量(dermal absorbed dose, DAD)和日均慢性摄入剂量(chronic daily ingestion, CDI)。
表1 本研究选用的个人护理品(PCPs)的相关信息
Table 1 Information of personal care products (PCPs) selected in this study
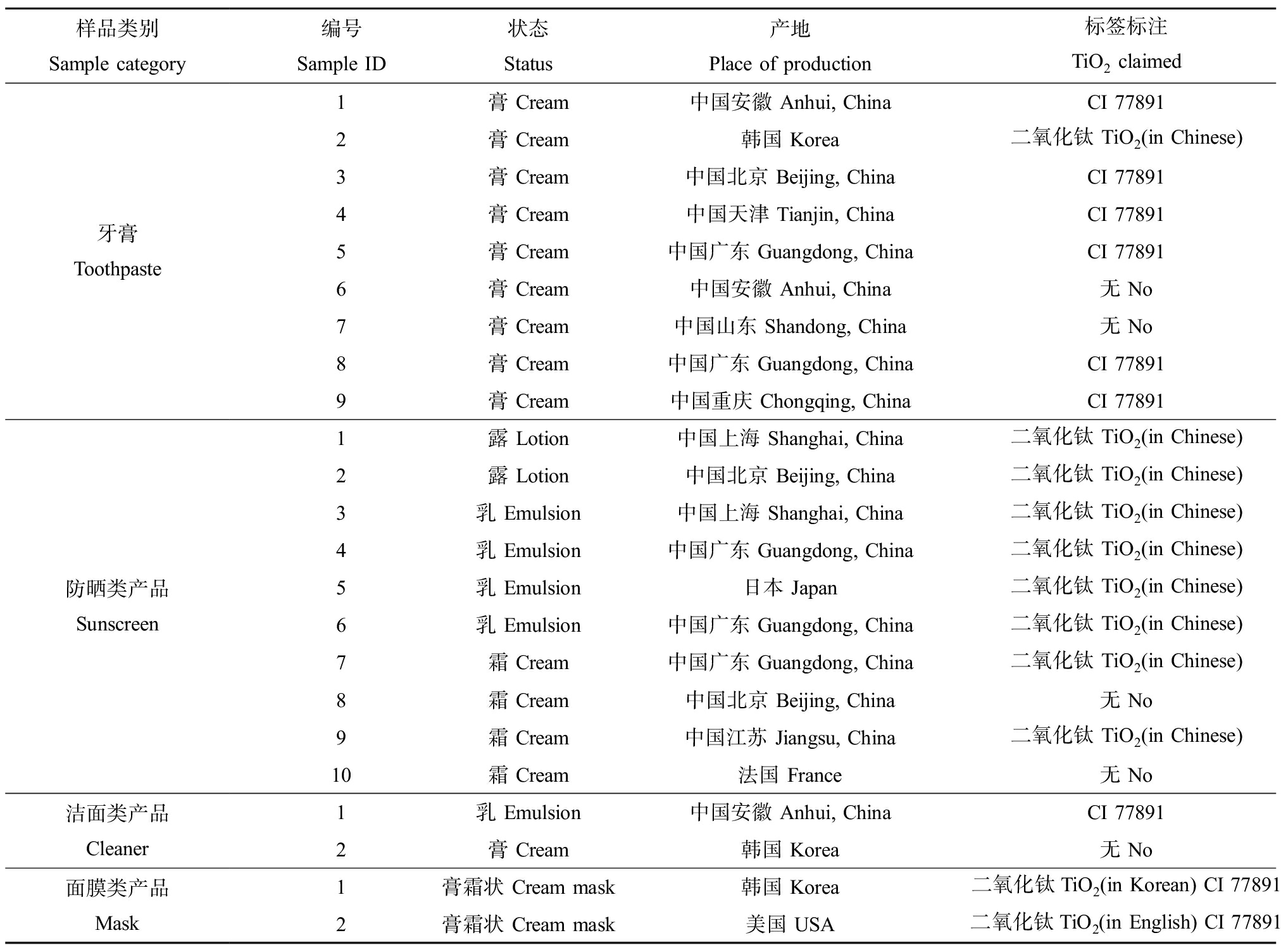
样品类别Sample category编号Sample ID状态Status产地Place of production标签标注TiO2 claimed牙膏Toothpaste1膏 Cream中国安徽 Anhui, ChinaCI 778912膏 Cream韩国 Korea二氧化钛 TiO2 (in Chinese)3膏 Cream中国北京 Beijing, ChinaCI 778914膏 Cream中国天津 Tianjin, ChinaCI 778915膏 Cream中国广东 Guangdong, ChinaCI 778916膏 Cream中国安徽 Anhui, China无 No7膏 Cream中国山东 Shandong, China无 No8膏 Cream中国广东 Guangdong, ChinaCI 778919膏 Cream中国重庆 Chongqing, ChinaCI 77891防晒类产品Sunscreen1露 Lotion中国上海 Shanghai, China二氧化钛 TiO2 (in Chinese)2露 Lotion中国北京 Beijing, China二氧化钛 TiO2 (in Chinese)3乳 Emulsion中国上海 Shanghai, China二氧化钛 TiO2 (in Chinese)4乳 Emulsion中国广东 Guangdong, China二氧化钛 TiO2 (in Chinese)5乳 Emulsion日本 Japan二氧化钛 TiO2 (in Chinese)6乳 Emulsion中国广东 Guangdong, China二氧化钛 TiO2 (in Chinese)7霜 Cream中国广东 Guangdong, China二氧化钛 TiO2 (in Chinese)8霜 Cream中国北京 Beijing, China无 No9霜 Cream中国江苏 Jiangsu, China二氧化钛 TiO2 (in Chinese)10霜 Cream法国 France无 No洁面类产品Cleaner1乳 Emulsion中国安徽 Anhui, ChinaCI 778912膏 Cream韩国 Korea无 No面膜类产品Mask1膏霜状 Cream mask韩国 Korea二氧化钛TiO2 (in Korean) CI 778912膏霜状 Cream mask美国 USA二氧化钛TiO2 (in English) CI 77891
表2 单颗粒电感耦合等离子体质谱(spICP-MS)参数设置
Table 2 Instrument parameters of single particle inductively coupled plasma mass spectrometer (spICP-MS)
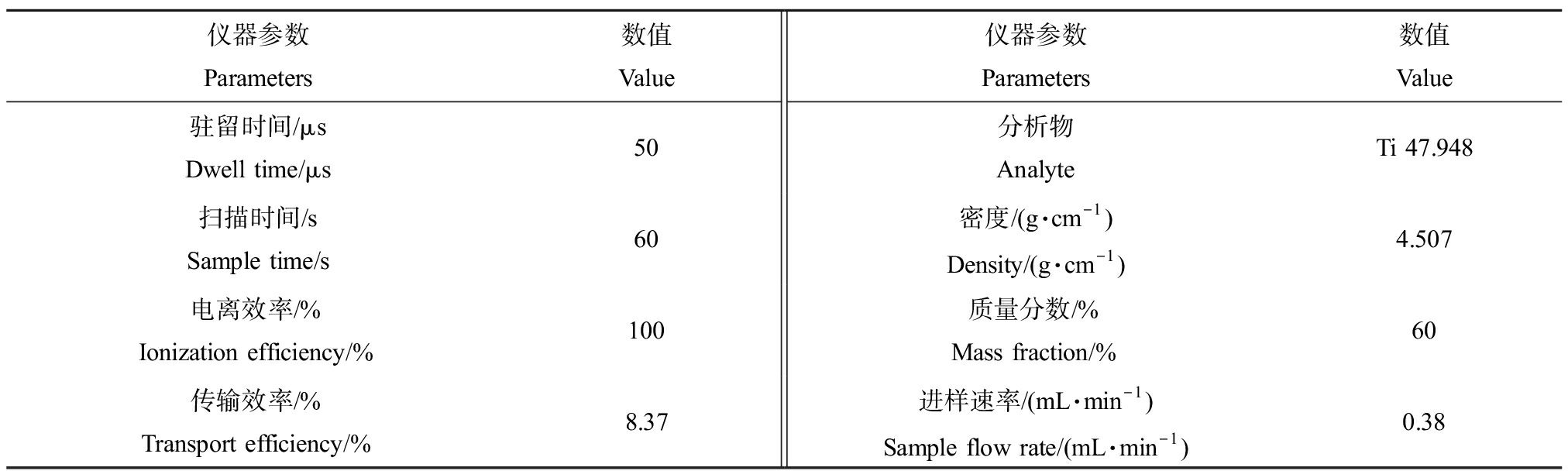
仪器参数Parameters数值Value仪器参数Parameters数值Value驻留时间/μsDwell time/μs50分析物AnalyteTi 47.948扫描时间/sSample time/s60密度/(g·cm-1)Density/(g·cm-1)4.507电离效率/%Ionization efficiency/%100质量分数/%Mass fraction/%60传输效率/%Transport efficiency/%8.37进样速率/(mL·min-1)Sample flow rate/(mL·min-1)0.38
![]()
(1)
DAevent=Cs×CF×AF×ABSd
(2)
(3)
式中:DAD为皮肤日均吸收剂量(mg·kg-1·d-1),DAevent为单次吸收剂量(mg·cm-2),EF为年暴露频率(d·a-1),ED为暴露期(a),EV为日均暴露频率(d-1),SA为皮肤接触面积(cm2),BW为体质量(kg),AT为非致癌效应的暴露期(AT=ED×365 d·a-1)。Cs为固体介质中污染物浓度(mg·kg-1),CF为体积转换因子(10-6 kg·mg-1),AF为固体介质的皮肤附着因子(mg·cm-2),ABSd为皮肤吸收系数,量纲为1。CDI为经口摄入的日均慢性摄入剂量(mg·kg-1·d-1),IR为经口摄入的日均摄入量(kg·d-1)。上述各参数使用的参考值如表3所示。
US EPA模型中未给出钛的ABSd值,本研究中选取与钛在同一周期的元素砷的ABSd值作为参考,即0.03。本研究中SA的估算主要采用了王宗爽等[33]的研究结果。关于我国人群的皮肤暴露面积的估算在许多文献中都有提到,并且建议考虑人种等情况的差异,不宜直接应用US EPA推荐的数据[33-35]。对于防晒类产品,皮肤暴露面积估算为头部、前臂、小腿的暴露面积之和,估计为0.428 m2。对于洁面类和面膜类产品,皮肤暴露面积估算为头部面积,估计为0.121 m2。本研究认为人体暴露于牙膏样品中的TiO2属于经口摄入这一暴露途径并且假定每日牙膏用量的10%被人体摄入[36]。因此,本研究假定牙膏的每日用量为0.001 kg·d-1,则牙膏的TiO2日均摄入量为0.0001 kg·d-1。进一步使用公式(4)~(5)计算TiO2的非致癌风险商(HQ)。
(4)
表3 人体健康风险评价参数的参考值
Table 3 Parameter values for human health risk assessment
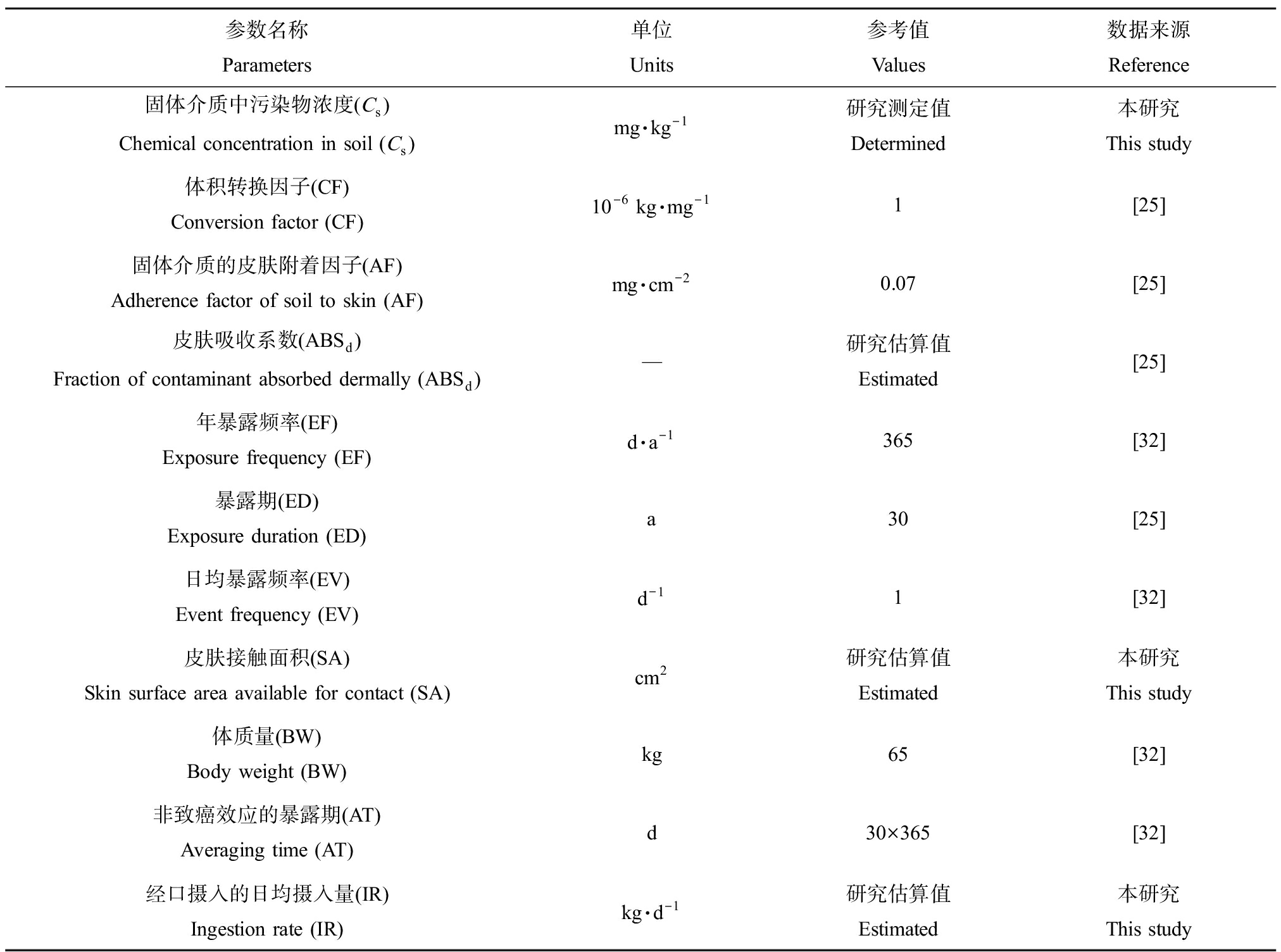
参数名称Parameters单位Units参考值Values数据来源Reference固体介质中污染物浓度(Cs)Chemical concentration in soil (Cs)mg·kg-1研究测定值Determined本研究This study体积转换因子(CF)Conversion factor (CF)10-6 kg·mg-11[25]固体介质的皮肤附着因子(AF)Adherence factor of soil to skin (AF)mg·cm-20.07[25]皮肤吸收系数(ABSd)Fraction of contaminant absorbed dermally (ABSd)—研究估算值Estimated[25]年暴露频率(EF)Exposure frequency (EF)d·a-1365[32]暴露期(ED)Exposure duration (ED)a30[25]日均暴露频率(EV)Event frequency (EV)d-11[32]皮肤接触面积(SA)Skin surface area available for contact (SA)cm2研究估算值Estimated本研究This study体质量(BW)Body weight (BW)kg65[32]非致癌效应的暴露期(AT)Averaging time (AT)d30×365[32]经口摄入的日均摄入量(IR)Ingestion rate (IR)kg·d-1研究估算值Estimated本研究This study
![]()
(5)
式中:HQdermal为皮肤暴露的非致癌风险商,HQoral为经口摄入的非致癌风险商,二者均量纲为1。RfD0为皮肤接触/经口摄入的日均参考剂量(mg·kg-1·d-1),ABSGI为消化道吸收效率因子,量纲为1。钛的RfD0在文献中无参考值,本研究中选取了Wang等[37]的预测值,即1.06 mg·kg-1·d-1。钛的ABSGI值亦无参考值,因此选取与钛相邻元素钒的ABSGI值作为参考,即2.6%[25]。HQ≤1表示风险较小可忽略,HQ>1表示存在非致癌风险。
2 结果与讨论(Results and discussion)
2.1 PCPs样品中总钛含量
利用ICP-MS检测样品中的总钛含量,结果表示为单位质量样品中钛的质量(mg·kg-1)(以Ti计),并计算了相应的TiO2的质量分数(表4)。我国《化妆品安全技术规范》(2015年版)中规定TiO2作为防晒剂使用时的最大允许浓度为25%(以质量分数计),可见样品的检测结果均远小于这一标准用量。对比检测结果可以发现,除牙膏7、防晒8和防晒10等3种样品中未检出TiO2外,其余样品中总钛的含量差异很大,含量在(16.8±3.7)~(14 264.2±4 302.3) mg·kg-1。牙膏样品中的钛含量在(16.8±3.7)~(1 384.4 ±314.9) mg·kg-1,这与Weir等[11]对8种牙膏的检测结果700~5 600 mg·kg-1相比有较大差异。通过防晒类产品的测定结果与部分已有研究结果的对比(表5),发现本研究所选用的防晒产品中的钛含量普遍小于之前研究报道的结果。本研究中钛含量较低的原因一方面可能与本研究采用的样品本身的性质有关,防晒类产品中TiO2的含量确实较低。另一方面,由于仪器操作规程的要求,在测定前进行滤膜过滤时也可能引起样品中Ti含量的损失。
表4 个人护理品(PCPs)样品中总钛含量
Table 4 Total content of Ti in personal care products (PCPs) samples
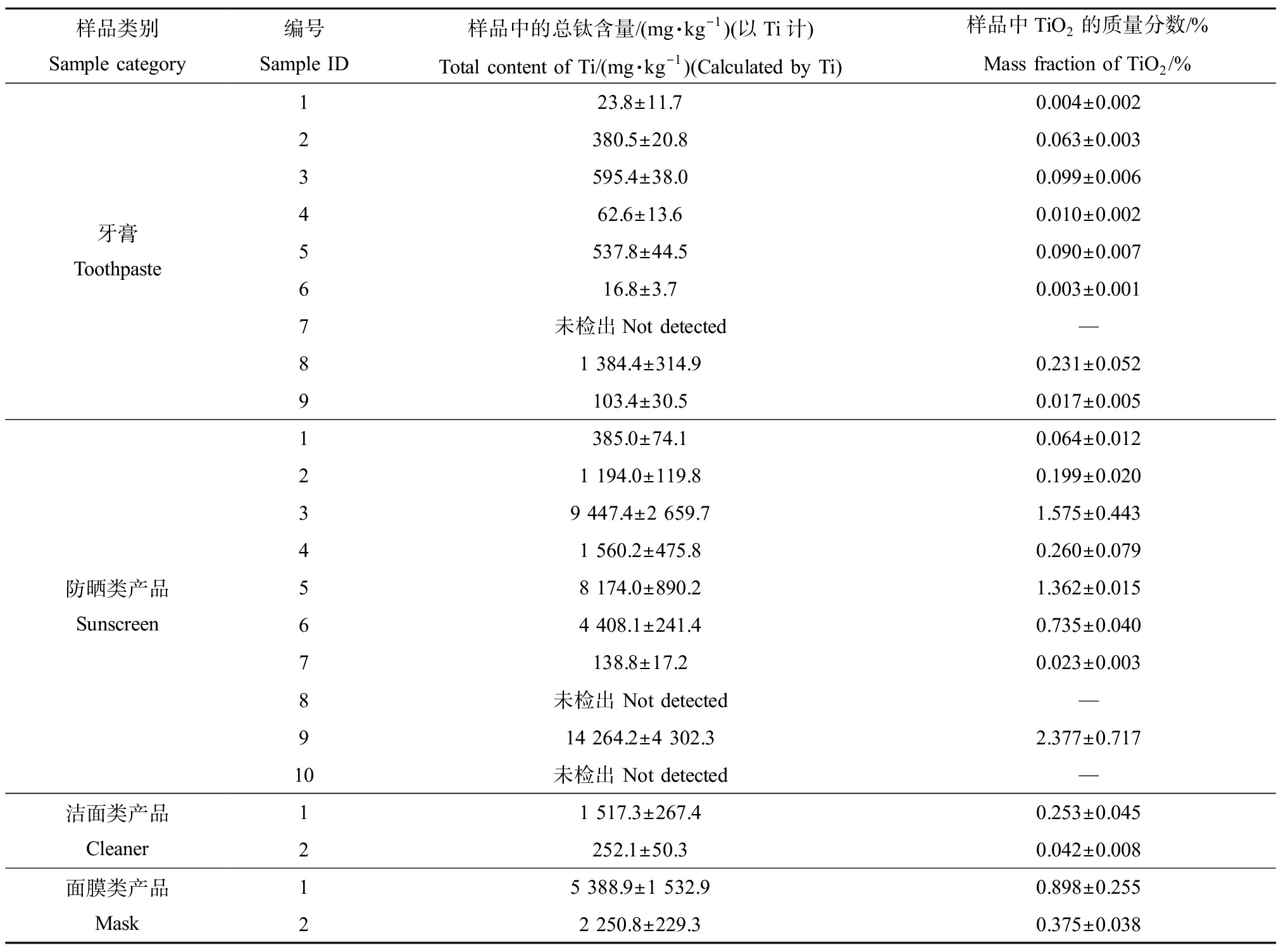
样品类别Sample category编号Sample ID样品中的总钛含量/(mg·kg-1)(以Ti计)Total content of Ti/(mg·kg-1)(Calculated by Ti)样品中TiO2的质量分数/%Mass fraction of TiO2/%牙膏Toothpaste123.8±11.70.004±0.0022380.5±20.80.063±0.0033595.4±38.00.099±0.006462.6±13.60.010±0.0025537.8±44.50.090±0.007616.8±3.70.003±0.0017未检出Not detected—81 384.4±314.90.231±0.0529103.4±30.50.017±0.005防晒类产品Sunscreen1385.0±74.10.064±0.01221 194.0±119.80.199±0.02039 447.4±2 659.71.575±0.44341 560.2±475.80.260±0.07958 174.0±890.21.362±0.01564 408.1±241.40.735±0.0407138.8±17.20.023±0.0038未检出 Not detected—914 264.2±4 302.32.377±0.71710未检出 Not detected—洁面类产品Cleaner11 517.3±267.40.253±0.0452252.1±50.30.042±0.008面膜类产品Mask15 388.9±1 532.90.898±0.25522 250.8±229.30.375±0.038
表5 防晒类产品中总钛含量比较
Table 5 The comparison of total content of Ti in sunscreen samples

测定方法Method总钛含量/(mg·kg-1)(以Ti计)Total content of Ti/(mg·kg-1)(Calculated by Ti)TiO2的质量分数/%Mass fraction of TiO2/%数据来源Reference电感耦合等离子体原子发射光谱 ICP-AES—3.72~5.33[9]方波伏安法 SWV—5.2~10.8电感耦合等离子体原子发射光谱 ICP-AES—7.4~11.0[10]电感耦合等离子体质谱 ICP-MS14 000~90 000—[11]重量法 Gravimetric method—5.23~16.2[12]分光光度法 Spectrophotography—0.71~6.67[13]电感耦合等离子体质谱 ICP-MS—0.13~1.7[28]电感耦合等离子体质谱 ICP-MS138.8~14 264.20.023~2.377本研究This study
之前的相关研究中普遍关注防晒产品,而洁面类产品研究较少,本研究选用的2种洁面类产品均检测到了TiO2。面膜类产品中通常也会添加TiO2作为着色剂,Zachariadis和Sahanidou[8]就曾在1种清洁面膜中检测出了(13.9±0.48) mg·kg-1的钛,而这一结果明显低于本研究的测定值(2 250.8±229.3) mg·kg-1和(5 388.9±1 532.9) mg·kg-1。这表明需要更加全面地考虑市售PCPs产品中TiO2的使用情况,从而对人体可能接触的TiO2含量进行更加科学的评估。
对比含量检测结果与标签标注情况可以发现,防晒类产品和面膜类产品的检测结果与商品本身标签注明的成分是相符的。对比同一种品牌2种不同系列牙膏样品(牙膏1和6)的钛含量水平,发现二者含量相近,故牙膏6可能未按实际情况标明产品中含有TiO2。同时,牙膏7样品确实未检出TiO2,这说明虽然TiO2在牙膏中是应用广泛的着色剂,但是并不是所有的产品均会使用。洁面类产品2中也检测到了TiO2的存在,这与商品的标注情况不一致。这表明我国应当进一步加强对商品标签标注的管理,包括加强对进口商品的监督和管理。
2.2 PCPs样品中TiO2 NPs的粒径分布
为了初步探究典型PCPs样品中TiO2 NPs的粒径分布,本研究进一步选取了12种PCPs,包括4种牙膏(牙膏1、2、3和4)、4种防晒类产品(防晒露1、2,防晒乳1、2)、2种洁面类产品和2种面膜类产品进行spICP-MS的测定。根据仪器检测出的单一粒径下的颗粒出现的次数进行统计分析。
从粒径分布的统计结果上可知,4种牙膏中TiO2 NPs的粒径分布存在差异(图1(a)~(d))。牙膏1和4中TiO2 NPs的粒径分布比较集中(60~120 nm),2和3相对来说较为分散。并且2和3中TiO2 NPs的粒径普遍大于1和4。这表明虽然都是牙膏产品,但是其使用的TiO2 NPs的种类可能是不同的。4种防晒类产品中只有防晒露2检测到了TiO2 NPs,并且粒径分布也比较集中(140~200 nm)(图1(g))。但是这一结果明显要比牙膏1和4中TiO2 NPs的粒径分布集中的粒径区间要高。其余防晒类产品均检测出了钛但未检测出TiO2 NPs的原因可能与spICP-MS方法的检出限有关。防晒类产品中TiO2 NPs粒径测定的主要方法有扫描电子显微镜(SEM)和透射电子显微镜(TEM)等,单颗粒电感耦合等离子体质谱(sp ICP-MS)是近年来的一种新兴技术。Lorenz等[38]利用TEM观测到防晒霜中的TiO2 NPs的形貌有球形、针形多种。球形的TiO2 NPs的粒径在20~160 nm,针形的长为40~80 nm,宽为5~18 nm。Lu等[39]也利用TEM观测到商业防晒霜粉中TiO2 NPs的粒径在(24.5±8.1)~(49.6±17.0) nm,与spICP-MS的测定结果基本一致。Philippe等[40]也利用TEM观测到了形态各异的TiO2 NPs,有2种防晒类产品中TiO2 NPs的粒径在20 nm以下。而本研究测定中spICP-MS的检测限为21.43 nm。所以部分防晒类产品中Ti含量高但未检测到TiO2 NPs粒径分布的可能与spICP-MS的检测限有关。单颗粒粒径分布测定方法的检出限与仪器参数的设定有关,已有的研究中粒径检出限普遍在30~50 nm左右[26-29]。粒径过小的纳米颗粒很难用spICP-MS方法检出,这说明其余防晒类产品中TiO2 NPs的粒径分布可能均小于此次测定的粒径检出限。而粒径更小的TiO2 NPs更有可能堵塞毛孔或者渗透进入人体皮肤,对人体的健康风险可能更大。未来可以考虑结合SEM等方法对样品中的TiO2 NPs进行进一步的表征来验证相关结论。2种洁面类产品(图1(e)~(f))和2种面膜类产品(图1(h), 1(i))中均检测到了TiO2 NPs,但粒径分布整体来说较为分散,并且随着粒径的增加相应的TiO2 NPs数量也减少。
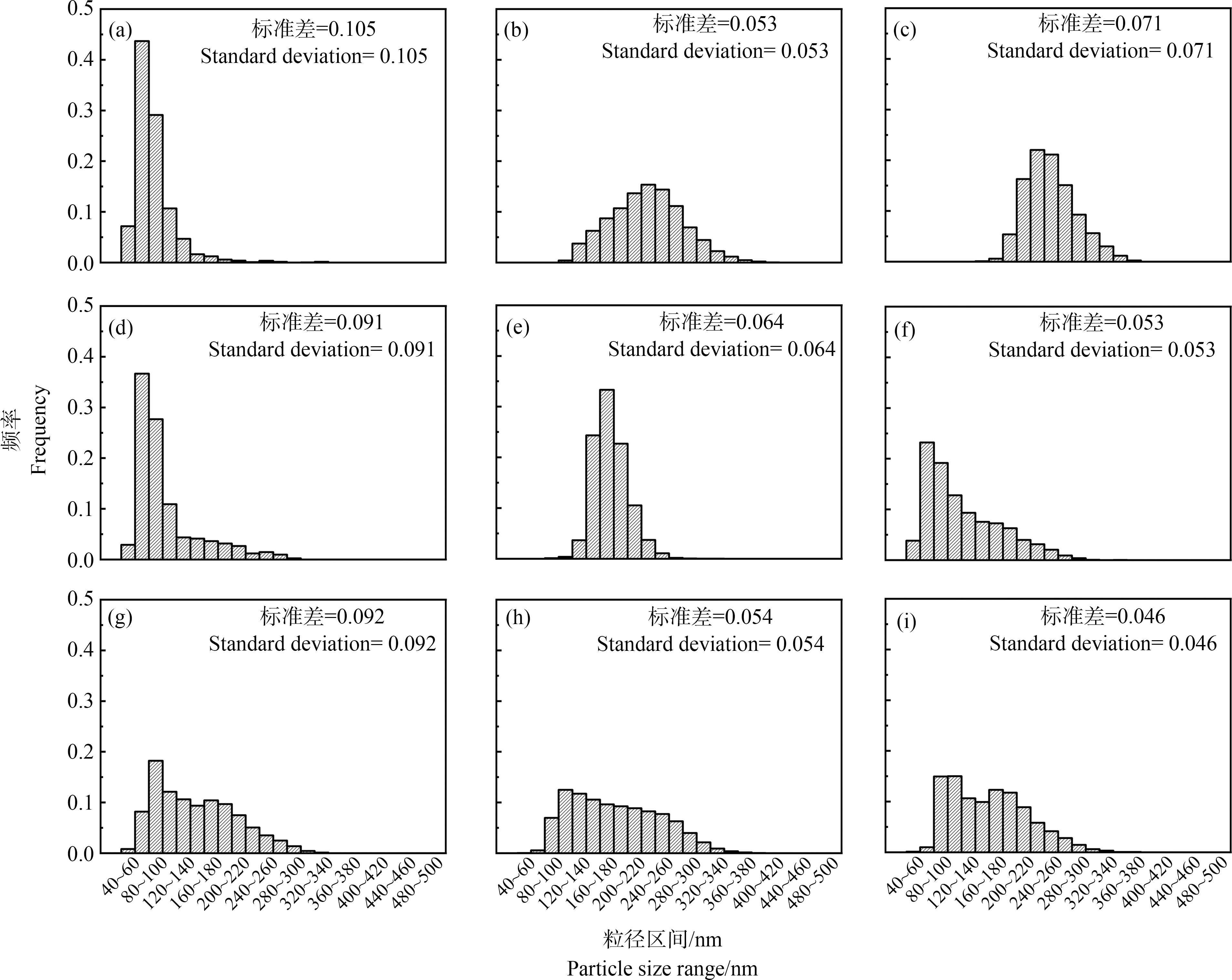
图1 部分个人护理品(PCPs)中TiO2 NPs粒径分布统计图
注:(a)~(d)代表牙膏1~4;(e)~(f)代表洁面1~2;(g)代表防晒2;(h)~(i)代表面膜1~2。
Fig. 1 TiO2 NPs particle size distribution in some personal care products (PCPs) samples
Note: (a)~(d) for toothpaste 1~4; (e)~(f) for cleaner 1~2; (g) for sunscreen 2; (h)~(i) for mask 1~2.
上述12种PCPs样品中TiO2 NPs的最大频率粒径和平均粒径的结果如图2所示。根据测定结果发现,检测出的TiO2 NPs的平均粒径总是在一定程度上高出最大频率粒径,这可能是由于样品中存在较大粒径的TiO2 NPs导致的。由于最大频率粒径在一定程度上反映了样品中大多数TiO2 NPs的粒径分布情况,所以重点对样品的最大频率粒径进行分析。在4种牙膏中均检测到了TiO2 NPs,最大频率粒径分别为(76.6±6.2)、(188.8±3.5)、(235.0±8.0)和(88.2±16.4) nm。2种洁面类样品的最大频率粒径也均在100 nm以下,分别为(75.4±7.2) nm和(83.9±2.1) nm。2种面膜类样品的最大频率粒径分别为(145.7±45.6) nm和(122.7±21.4) nm。这表明选择的大部分PCPs中均存在TiO2 NPs,但是粒径分布的差异较大,表明这些产品可能使用了不同的TiO2 NPs。相对来说,牙膏1中的钛含量虽然较其他产品更低,但是平均粒径及最大频率粒径却是所有检测产品中最小的,需要进一步评估其对人体的健康风险。
2.3 PCPs样品中钛的健康风险评价
本研究中选用的PCPs中钛的日均暴露量及钛的非致癌风险商的计算结果如表6所示。本研究中PCPs中钛的非致癌风险商在1.75×10-5~9.30×10-2之间,表明钛的人体健康风险较小可以忽略。此外,与江媛媛等[32]对抗菌消费品中银的非致癌风险商的研究结果相比,可以发现个人护理品中钛的健康风险也远小于部分抗菌消费品中银的健康风险。通过对比可以发现,虽然牙膏产品与其他产品的暴露量差异不大,但其非致癌风险商却更低,这主要与牙膏是经口暴露有关。并且对于同样是皮肤暴露的防晒、洁面和面膜类产品,按照1.5中的评价方法,很可能高估了洁面类产品和面膜类产品的日均暴露频率,这可能会引起较大的误差。
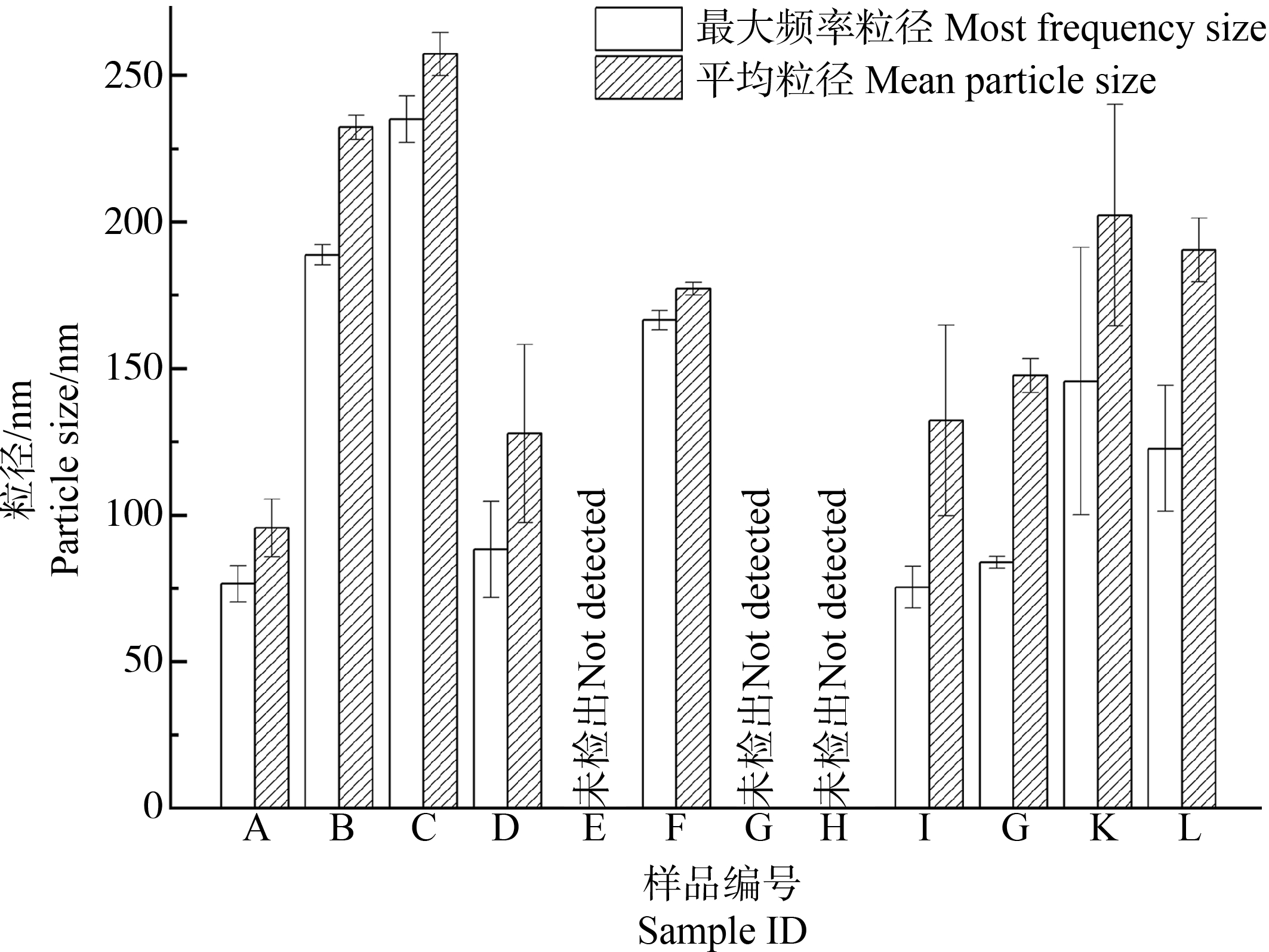
图2 个人护理品(PCPs)样品中TiO2 NPs的最大频率粒径与平均粒径
注:A~D代表牙膏1~4;E~H代表防晒1~4;I、G代表洁面1~2;K、L代表面膜1~2。
Fig. 2 Most frequency size and mean size of TiO2 NPs in personal care products (PCPs) samples
Note: A~D represent toothpaste 1~4; E~H represent sunscreen 1~4; I~G represent cleaner 1~2; K~L represent mask 1~2.
表6 个人护理品(PCPs)样品中钛的健康风险评价结果
Table 6 Results of health risk assessment of Ti in personal care products (PCPs) samples

样品类别Sample category编号Sample IDDAD or CDI/(mg·kg-1·d-1)HQ牙膏Toothpaste11.86×10-5~5.46×10-51.75×10-5~5.15×10-525.53×10-4~6.17×10-45.22×10-4~5.82×10-438.58×10-4~9.74×10-48.09×10-4~9.19×10-447.54×10-5~1.17×10-47.11×10-5~1.11×10-457.59×10-4~8.96×10-47.16×10-4~8.45×10-462.02×10-5~3.16×10-51.90×10-5~2.98×10-57——81.65×10-3~2.61×10-31.55×10-3~2.47×10-391.12×10-4~2.06×10-41.06×10-4~1.94×10-4防晒类产品Sunscreen14.29×10-5~6.34×10-51.56×10-3~2.30×10-321.48×10-4~1.81×10-45.38×10-3~6.58×10-339.37×10-4~1.67×10-33.40×10-2~6.07×10-241.50×10-4~2.81×10-45.43×10-3~1.02×10-251.01×10-3~1.25×10-33.65×10-2~4.54×10-265.75×10-4~6.42×10-42.09×10-2~2.33×10-271.68×10-5~2.16×10-56.10×10-4~7.82×10-48——91.38×10-3~2.56×10-34.99×10-2~9.30×10-210——洁面类产品Cleaner14.89×10-5~6.98×10-51.77×10-3~2.53×10-327.89×10-6~1.18×10-52.86×10-4~4.29×10-4面膜类产品Mask11.51×10-4~2.71×10-45.47×10-3~9.82×10-327.90×10-5~9.70×10-52.87×10-3~3.52×10-3
注:DAD代表皮肤日均吸收剂量,CDI代表日均慢性摄入剂量,HQ代表非致癌风险商。
Note: DAD stands for dermal absorbed dose; CDI stands for chronic daily ingestion; HQ stands for hazard quotient.
综上所述,目前市售的部分PCPs中添加TiO2 NPs作为原材料,并且没有在标签中特别说明,spICP-MS测定的结果显示粒径大小约为40~400 nm。钛的健康风险评价的结果表明本研究选择的PCPs中的TiO2 NPs在人们日常生活中的健康风险较小。本研究尚存在一定的局限性,例如产品的检测范围有待进一步扩大,人体健康风险评价模型中钛的皮肤吸收系数、消化道吸收效率因子等参数需要进一步研究确定。未来亟需开展更多关于纳米尺寸的健康风险评价研究,提高对TiO2等纳米材料的人体健康影响的认识,更好地管理和使用纳米材料。
[1] Gázquez M J, Bolívar J P, Garcia-Tenorio R, et al. A review of the production cycle of titanium dioxide pigment [J]. Materials Sciences and Applications, 2014, 5(7): 441-458
[2] 崔玉民, 王洪涛. 二氧化钛光催化技术在污水处理领域中应用[J]. 水处理技术, 2009, 35(4): 9-12, 17
Cui Y M, Wang H T. Application of titanium oxide photocatalytic technology in the field of sewage treatment [J]. Technology of Water Treatment, 2009, 35(4): 9-12, 17 (in Chinese)
[3] 王学川, 任龙芳, 强涛涛. 纳米材料在化妆品中的应用[J]. 日用化学品科学, 2006, 29(4): 15-18
Wang X C, Ren L F, Qiang T T. Application of nano-material in cosmetics [J]. Detergent & Cosmetics, 2006, 29(4): 15-18 (in Chinese)
[4] Hoseinnejad M, Jafari S M, Katouzian I. Inorganic and metal nanoparticles and their antimicrobial activity in food packaging applications [J]. Critical Reviews in Microbiology, 2018, 44(2): 161-181
[5] Ziental D, Czarczynska-Goslinska B, Mlynarczyk D T, et al. Titanium dioxide nanoparticles: Prospects and applications in medicine [J]. Nanomaterials, 2020, 10(2): 387
[6] Musial J, Krakowiak R, Mlynarczyk D T, et al. Titanium dioxide nanoparticles in food and personal care products—what do we know about their safety? [J]. Nanomaterials, 2020, 10(6): 1110-1133
[7] 国家食品药品监督管理总局. 化妆品安全技术规范[EB/OL]. (2015-12-23) [2022-01-31] https://www.nmpa.gov.cn/hzhp/hzhpggtg/hzhpqtgg/20151223120001986.html
[8] Zachariadis G A, Sahanidou E. Analytical performance of a fast multi-element method for titanium and trace elements determination in cosmetics and pharmaceuticals by ICP-AES [J]. Central European Journal of Chemistry, 2011, 9(2): 213-217
[9] Botta C, Labille J, Auffan M, et al. TiO2-based nanoparticles released in water from commercialized sunscreens in a life-cycle perspective: Structures and quantities [J]. Environmental Pollution, 2011, 159(6): 1543-1550
[10] Contado C, Pagnoni A. TiO2 nano- and micro-particles in commercial foundation creams: Field flow-fractionation techniques together with ICP-AES and SQW voltammetry for their characterization [J]. Analytical Methods, 2010, 2(8): 1112-1124
[11] Weir A, Westerhoff P, Fabricius L, et al. Titanium dioxide nanoparticles in food and personal care products [J]. Environmental Science & Technology, 2012, 46(4): 2242-2250
[12] 王传庆. 防晒化妆品中二氧化钛含量的测定[J]. 安徽电子信息职业技术学院学报, 2006, 5(6): 121-122
[13] 陈昌, 冯燕华, 戴士乔. 化妆品中二氧化钛含量的测定[J]. 科技风, 2010(22): 263-264
[14] Baranowska-Wójcik E, Szwajgier D, Oleszczuk P, et al. Effects of titanium dioxide nanoparticles exposure on human health—A review [J]. Biological Trace Element Research, 2020, 193(1): 118-129
[15] Luo Z, Li Z Q, Xie Z, et al. Rethinking nano-TiO2 safety: Overview of toxic effects in humans and aquatic animals [J]. Small, 2020, 16(36): e2002019
[16] 王江雪, 李炜, 刘颖, 等. 二氧化钛纳米材料的环境健康和生态毒理效应[J]. 生态毒理学报, 2008, 3(2): 105-113
Wang J X, Li W, Liu Y, et al. Environmental health and ecotoxicological effect of titanium dioxide nanomaterials [J]. Asian Journal of Ecotoxicology, 2008, 3(2): 105-113 (in Chinese)
[17] 张智, 杨浩, 郭衡, 等. 纳米TiO2的健康风险与环境毒性研究进展[J]. 环境科学与管理, 2017, 42(3): 52-56
Zhang Z, Yang H, Guo H, et al. Research progresses in health risk and environmental toxicity effects of nano-sized TiO2 [J]. Environmental Science and Management, 2017, 42(3): 52-56 (in Chinese)
[18] Dréno B, Alexis A, Chuberre B, et al. Safety of titanium dioxide nanoparticles in cosmetics [J]. Journal of the European Academy of Dermatology and Venereology, 2019, 33(S7): 34-46
[19] 刘焕亮, 袭著革, 张华山, 等. 3种典型纳米材料对大鼠肺的毒性效应[J]. 环境与健康杂志, 2010, 27(4): 299-302, 377
Liu H L, Xi Z G, Zhang H S, et al. Pulmonary toxicity of three typical nanomaterials on rats [J]. Journal of Environment and Health, 2010, 27(4): 299-302, 377 (in Chinese)
[20] Adler B L, DeLeo V A. Sunscreen safety: A review of recent studies on humans and the environment [J]. Current Dermatology Reports, 2020, 9(1): 1-9
[21] 侯东颖, 冯佳, 谢树莲. 纳米二氧化钛胁迫对普生轮藻的毒性效应[J]. 环境科学学报, 2012, 32(6): 1481-1486
Hou D Y, Feng J, Xie S L. Toxic effects of nanoparticle TiO2 stress on Chara vulgaris L [J]. Acta Scientiae Circumstantiae, 2012, 32(6): 1481-1486 (in Chinese)
[22] Mishra V, Baranwal V, Mishra R K, et al. Titanium dioxide nanoparticles augment allergic airway inflammation and Socs3 expression via NF-κB pathway in murine model of asthma [J]. Biomaterials, 2016, 92: 90-102
[23] Fuster E, Candela H, Estévez J, et al. Titanium dioxide, but not zinc oxide, nanoparticles cause severe transcriptomic alterations in T98G human glioblastoma cells [J]. International Journal of Molecular Sciences, 2021, 22(4): 2084
[24] 李伟. 食品中纳米二氧化钛的健康风险评价研究: 以食品口香糖为例[D]. 长春: 东北师范大学, 2019: 12-14
Li W. Health risk assessment of nano-titanium dioxide in food: A case study on chewing gum [D]. Changchun: Northeast Normal University, 2019: 12-14 (in Chinese)
[25] United States Environmental Protection Agency (US EPA). Risk assessment guidance for superfund volume I: Human health evaluation manual (Part E, supplemental guidance for dermal risk assessment) [R/OL]. (2020-01-29) [2021-06-23]. https://www.epa.gov/risk/risk-assessment-guidance-superfund-rags-part-e
[26] Mackevica A, Olsson M E, Hansen S F. Quantitative characterization of TiO2 nanoparticle release from textiles by conventional and single particle ICP-MS [J]. Journal of Nanoparticle Research, 2018, 20(1): 6
[27] Salou S, Larivière D, Cirtiu C M, et al. Quantification of titanium dioxide nanoparticles in human urine by single-particle ICP-MS [J]. Analytical and Bioanalytical Chemistry, 2021, 413(1): 171-181
[28] 梁维新, 刘宁, 郭鹏然, 等. 超声辅助提取/单颗粒电感耦合等离子体质谱法测定防晒化妆品中的纳米二氧化钛[J]. 分析测试学报, 2018, 37(10): 1238-1243
Liang W X, Liu N, Guo P R, et al. Determination of nano-TiO2 in sunscreen by single particle inductively coupled plasma-mass spectrometry with ultrasound-assisted extraction [J]. Journal of Instrumental Analysis, 2018, 37(10): 1238-1243 (in Chinese)
[29] 王丹红, 唐庆强, 陈祥明, 等. 食品中纳米二氧化钛的单颗粒-电感耦合等离子质谱法表征及其测定[J]. 福建分析测试, 2018, 27(5): 1-5
Wang D H, Tang Q Q, Chen X M, et al. Characterization and determination of titanium dioxide nanoparticle in foods using single particle-inductively coupled plasma-mass spectrometry [J]. Fujian Analysis & Testing, 2018, 27(5): 1-5 (in Chinese)
[30] 国家质量监督检验检疫总局, 中国国家标准化管理委员会. 化妆品名词术语: GB/T 27578—2011[S]. 北京: 中国标准出版社, 2012
[31] Liang D Y, Wang X R, Liu S, et al. Factors determining the toxicity of engineered nanomaterials to Tetrahymena thermophila in freshwater: The critical role of organic matter [J]. Environmental Science: Nano, 2020, 7(1): 304-316
[32] 江媛媛, 付庆龙, 施维林, 等. 抗菌消费品中纳米银含量调查及银的健康风险评价[J]. 生态毒理学报, 2016, 11(5): 57-64
Jiang Y Y, Fu Q L, Shi W L, et al. Contents of nanosilver in commercially antimicrobial products and silver health risk assessment to adult consumers [J]. Asian Journal of Ecotoxicology, 2016, 11(5): 57-64 (in Chinese)
[33] 王宗爽, 段小丽, 刘平, 等. 环境健康风险评价中我国居民暴露参数探讨[J]. 环境科学研究, 2009, 22(10): 1164-1170
Wang Z S, Duan X L, Liu P, et al. Human exposure factors of Chinese people in environmental health risk assessment [J]. Research of Environmental Sciences, 2009, 22(10): 1164-1170 (in Chinese)
[34] 段小丽, 王宗爽, 李琴, 等. 基于参数实测的水中重金属暴露的健康风险研究[J]. 环境科学, 2011, 32(5): 1329-1339
Duan X L, Wang Z S, Li Q, et al. Health risk assessment of heavy metals in drinking water based on field measurement of exposure factors of Chinese people [J]. Environmental Science, 2011, 32(5): 1329-1339 (in Chinese)
[35] 段小丽, 聂静, 王宗爽, 等. 健康风险评价中人体暴露参数的国内外研究概况[J]. 环境与健康杂志, 2009, 26(4): 370-373
Duan X L, Nie J, Wang Z S, et al. Human exposure factors in health risk assessment [J]. Journal of Environment and Health, 2009, 26(4): 370-373 (in Chinese)
[36] Wu F, Hicks A L. Estimating human exposure to titanium dioxide from personal care products through a social survey approach [J]. Integrated Environmental Assessment and Management, 2020, 16(1): 10-16
[37] Wang Y, Wu F C, Liu Y D, et al. Effect doses for protection of human health predicted from physicochemical properties of metals/metalloids [J]. Environmental Pollution, 2018, 232: 458-466
[38] Lorenz C, Tiede K R, Tear S, et al. Imaging and characterization of engineered nanoparticles in sunscreens by electron microscopy, under wet and dry conditions [J]. International Journal of Occupational and Environmental Health, 2010, 16(4): 406-428
[39] Lu P J, Fang S W, Cheng W L, et al. Characterization of titanium dioxide and zinc oxide nanoparticles in sunscreen powder by comparing different measurement methods [J]. Journal of Food and Drug Analysis, 2018, 26(3): 1192-1200
[40] Philippe A, ![]() ík J, Welle A, et al. Extraction and characterization methods for titanium dioxide nanoparticles from commercialized sunscreens [J]. Environmental Science: Nano, 2018, 5(1): 191-202
ík J, Welle A, et al. Extraction and characterization methods for titanium dioxide nanoparticles from commercialized sunscreens [J]. Environmental Science: Nano, 2018, 5(1): 191-202