-
磷是我国地表水环境的主要污染因子,是导致水体富营养化的重要因素[1]。水中磷的去除,对污水深度处理与回用、城市初期雨水治理等具有重要意义。“十四五”期间,国家对水环境治理提出了更高的要求,各地出台了污水排放的准四类,甚至准三类标准,磷浓度是相关标准的核心评价指标之一[2-4]。传统生物法和化学法深度除磷的成本高,实现难度大,而生态处理技术,如人工湿地、生态沟渠等,因具有成本低、能同时改善人居环境等优势,而受到广泛关注[5-6]。
然而,在生态处理系统中发现,仅靠植物和微生物,难以取得较好的磷去除效果[7-8]。人工湿地及生态沟渠的磷去除效率与其基质存在显著相关性,基质不仅可以直接吸附去除水中的磷,还可为植物和微生物的生长提供良好的微环境[9]。作为生态系统的常用基质材料,陶粒因制备简单、机械强度高、吸附性能好等特征,而备受关注[10-12]。特别是以城市固废作为基质材料所制备的陶粒,不仅可以用于对水中磷的去除,而且可同时解决固废的处理难题[13-15]。
铁锰是我国饮用水水源,特别是地下水源中的重要污染物。其去除基本原理是,利用化学或生物的方法,将水中的Fe2+和Mn2+氧化为不溶于水的高价氧化物,进而通过过滤去除[16]。水中铁锰的去除过程,会形成大量富含铁锰氧化物的反冲洗污泥。这一方面给污泥的处置带来了困难,另一方面,若直接将该污泥填埋处置,将造成铁锰资源的浪费,并产生生态安全风险[17]。同时,相对于给水厂絮凝污泥和污水厂脱水污泥,滤池反冲洗铁锰污泥具有成分相对稳定、活性组分比例高、易于回收利用、可同时去除水中氨氮和砷等特征,但目前对该污泥的资源化利用研究地相对较少[18-20]。
本研究将除铁锰滤池产生的反冲洗污泥,经脱水干燥后用作制备陶粒的添加材料,成功制备出了铁锰污泥基生态陶粒,并探究了该陶粒的结构特征及对水中磷的吸附去除性能。这一方面减少了传统陶粒制备材料的用量,另一方面改善了陶粒的污染物去除性能,并解决了铁锰污泥的处置问题,具有一定实用价值。
-
实验所用铁锰污泥为接触催化除铁锰滤池的反冲洗污泥,该滤池长期进水平均质量浓度为Fe2+=3.0 mg·L−1,Mn2+=1.0 mg·L−1。高岭土购自古丈县山磷石语矿产品有限公司,氧化钙购自天津市科密欧化学试剂有限公司,生物质为鸢尾经烘干、研磨后过100目筛网制备。实验试剂除特别说明外均为分析纯。
-
1)陶粒吸附材料的制备。按照一定质量百分比,分别称取高岭土、铁锰污泥、生物质(10%)和氧化钙(10%),并充分混匀,加适量水制成粒径为5~10 mm的生陶粒。将生陶粒置于鼓风干燥箱(DHG-9013A,上海一恒科学仪器有限公司)中于105 ℃烘干2 h后,在空气气氛下于管式高温炉(ST-12NT-40/220-2,上海久工电器有限公司)中以10 ℃·min−1的速率升温至500 ℃并保温1 h,再分别升温至600、700、800、900和950 ℃煅烧1.5 h。待炉中温度降至室温后取出,即制备出相应陶粒。
2)磷吸附实验。采用KH2PO4配制磷储备液,并根据实验需求稀释为不同浓度的反应液,在恒温水浴摇床中进行静态吸附实验。具体为,将50~100 mL溶液置于150 mL或200 mL锥形瓶中,并立即加入一定质量的陶粒,在25 ℃,80 r·min−1的条件下进行吸附反应。溶液pH通过HCl和NaOH溶液调节。反应结束后,将反应液用0.45 μm滤膜过滤,并采用钼酸盐分光光度法测定水中磷酸盐含量。
3)磷吸附动力学。分别采用准一级动力学方程(式(1))、准二级动力学方程(式(2))和颗粒内扩散方程(式(3))对吸附动力学实验数据进行拟合。
式中:qe为平衡吸附量,mg·g−1;qt为t时刻吸附量,mg·L−1;t 为吸附时间,h;k1为准一级动力学常数,L·h−1;k2为准二级动力学常数,g·(h·mg)−1; Kp为颗粒内扩散动力学常数,mg·h−0.5 ·g−1;c为曲线截距。
4)等温吸附实验。控制磷酸盐初始质量浓度为3、5、7、10、20、30 mg·L−1,反应温度为25 ℃,开展了陶粒对磷酸盐的等温吸附实验,并分别采用 Langmuir模型(式(4))和 Freundlich模型(式(5))对实验数据进行了拟合。
式中: qe为平衡吸附量,mg·g−1;qm为理论最大吸附量,mg·g−1;KL为 Langmuir常数,L·mg−1;KF为 Freundlich常数,mg·g−1·(L·mg−1)1/n;n为经验常数。
5)表征方法。采用扫描电子显微镜(SEM,捷克tescan CLARA)测定陶粒的外观形貌。采用能谱仪(EDS,英国oxford xplore)分析样品表面元素种类及分布。采用比表面积及孔隙分析仪(BET,美国ASAP2020 PLUS HD88)测试样品的比表面积、孔容和孔径分布等数据。采用傅里叶变换红外光谱仪(FTIR,美国-赛默飞-Nicolet IS5)分析样品表面的官能团结构。采用X射线光电子能谱(XPS,美国-赛默飞-Thermo Scientific ESCALAB Xi+)表征陶粒表面元素的化学性质。
-
分别考察了铁锰污泥添加量和煅烧温度对陶粒水中磷去除效果的影响,结果如图1所示。由图1(a)可以看出,铁锰污泥的添加可显著提升陶粒对磷的去除效果。当铁锰污泥的添加量为30%时,陶粒对磷的去除率由未添加时的30.12%提升至50.51%,但继续增加铁锰污泥含量至50%,陶粒对磷的吸附效率提升并不明显。因此,确定铁锰污泥的最佳添加量为30%。分别考察了煅烧温度为600、700、800、900和950 ℃时对陶粒特性的影响。当陶粒生坯于600 ℃和700 ℃煅烧后,易破碎,不能形成有效强度,无法作为生态系统基质使用,因此未考察其磷去除性能。经800、900和950 ℃煅烧所制备陶粒外观及磷去除特性如图1(b)所示。由图1(b)可知,铁锰污泥添加量为30%时,在800 ℃制备条件下,所制备陶粒表面呈浅灰棕色,当温度为900 ℃及以上时,陶粒呈红棕色,说明温度达到900 ℃后陶粒的结构发生了显著变化。随着煅烧温度的升高,陶粒对水中磷的去除率逐步降低。但在800 ℃下,铁锰污泥添加量为20%所制备的陶粒对磷酸盐的去除率低于在900 ℃、铁锰污泥添加量为30%所制备的陶粒。煅烧温度的提升,一方面使制备过程中产生的液相增多,陶粒将变得更加致密,孔隙和比表面积减小[21],另一方面过高的温度可能使陶粒中所含的Al3+、Ca2+和Na+ 等金属离子与SiO2 反应生成稳定的硅酸盐类物质[11],进而导致陶粒对磷去除效果下降。同时,对不同煅烧温度条件下,铁锰污泥的磷酸盐吸附效果进行了考察,结果如图1(c)所示。可以看出,煅烧温度在700~950 ℃时,对铁锰污泥的磷酸盐吸附效果影响不大,铁锰污泥对磷酸盐的吸附量在14.98~15.40 mg·g−1。这进一步说明煅烧温度主要是影响了陶粒的结构,进而影响陶粒对磷酸盐的吸附效果。但在实验过程中发现,在摇床中连续振荡36 h后,经800 ℃煅烧所制得的陶粒,其水样浑浊,说明该陶粒强度不足。因此,综合考虑材料机械强度和磷去除效果,确定最佳煅烧温度为900 ℃。
-
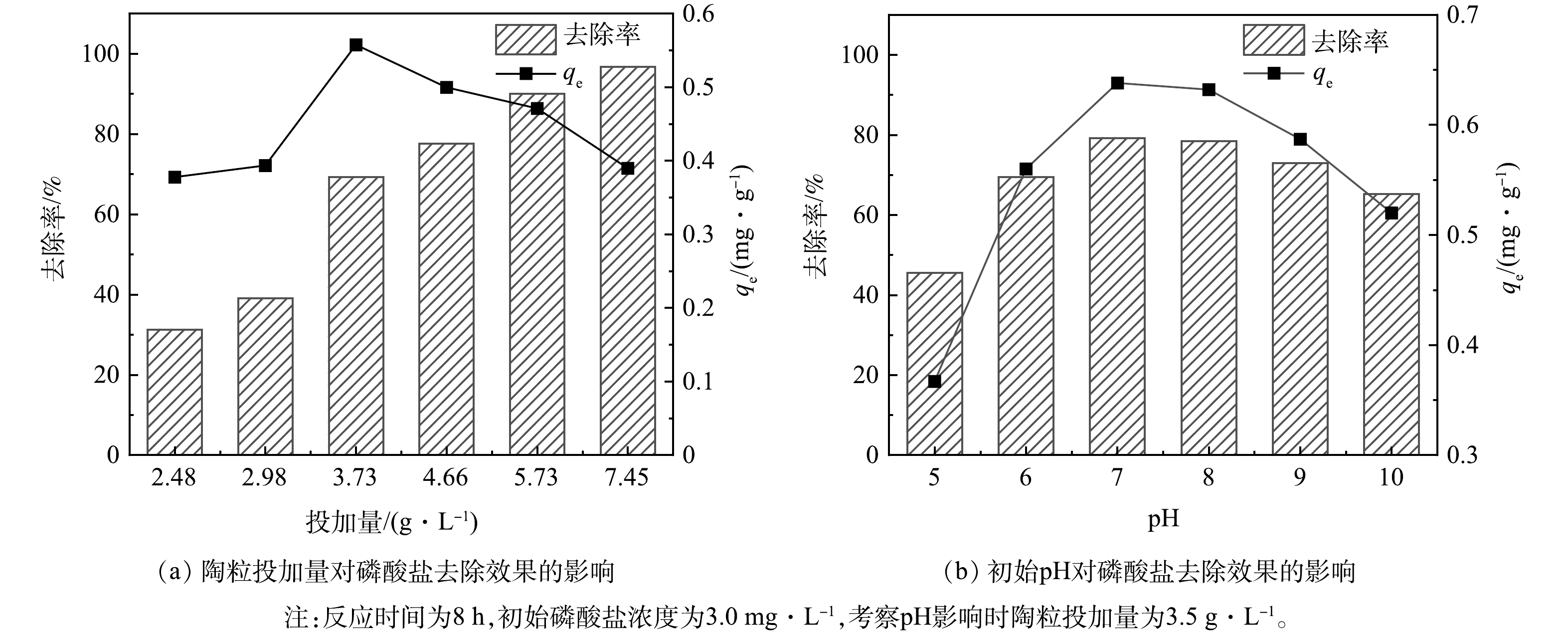
图2(a)为不同投加量条件下,陶粒对水中磷的去除效果。由图2(a)可知,磷的去除率随陶粒投加量的增加而增加。当陶粒的投加量为7.45 g·L−1时,水中磷几乎被完全去除,陶粒对磷的去除率为96.79%,水中残余磷的质量浓度小于0.096 mg·L−1。图2(b)为不同初始pH条件下陶粒对水中磷的吸附去除效果。有研究[22- 23]表明,pH是影响陶粒吸附行为的最重要因素之一。由图2(b)可以看出,随着pH的升高,陶粒对水中磷的去除率先增加再降低,在pH=7~8 时,陶粒具有最佳的磷吸附去除效果。陶粒对磷酸盐的吸附效率,一方面与陶粒中氧化物的等电荷点密切相关,另一方面受磷酸盐在水中存在形态的影响。形成陶粒的金属氧化物,其等电荷点往往较低,在实际水处理条件下,陶粒表面一般带负电[24-25],这与磷酸盐本身所带电性相同,因此,磷酸盐在陶粒表面的吸附,并非简单的静电吸附作用[22-23]。当水体pH小于2.1时,磷酸盐在水中主要以H3PO4形式存在,pH在2.1~7.2时,主要以H2PO4−形式存在,pH在7.2~12.3时,主要以HPO4−形式存在,pH大于12.3时主要以PO43−形式存在[26]。当水体pH升高时,陶粒表面负电荷数量增加,从而阻碍陶粒与磷酸盐接触。因此,当pH增加到10时,磷酸盐去除率有所降低。当pH降低至5时,陶粒对磷酸盐的去除效果下降,这与一般陶粒在pH降低时对磷的吸附效率上升有所不同[22-23]。进一步分析认为,当pH降低时,体系中H2PO4−含量增加,而与Fe/Al 有更强结合能力HPO42−含量减少,进而导致体系磷酸盐去除率下降,该结果与YIN等[25]的研究基本一致。
-
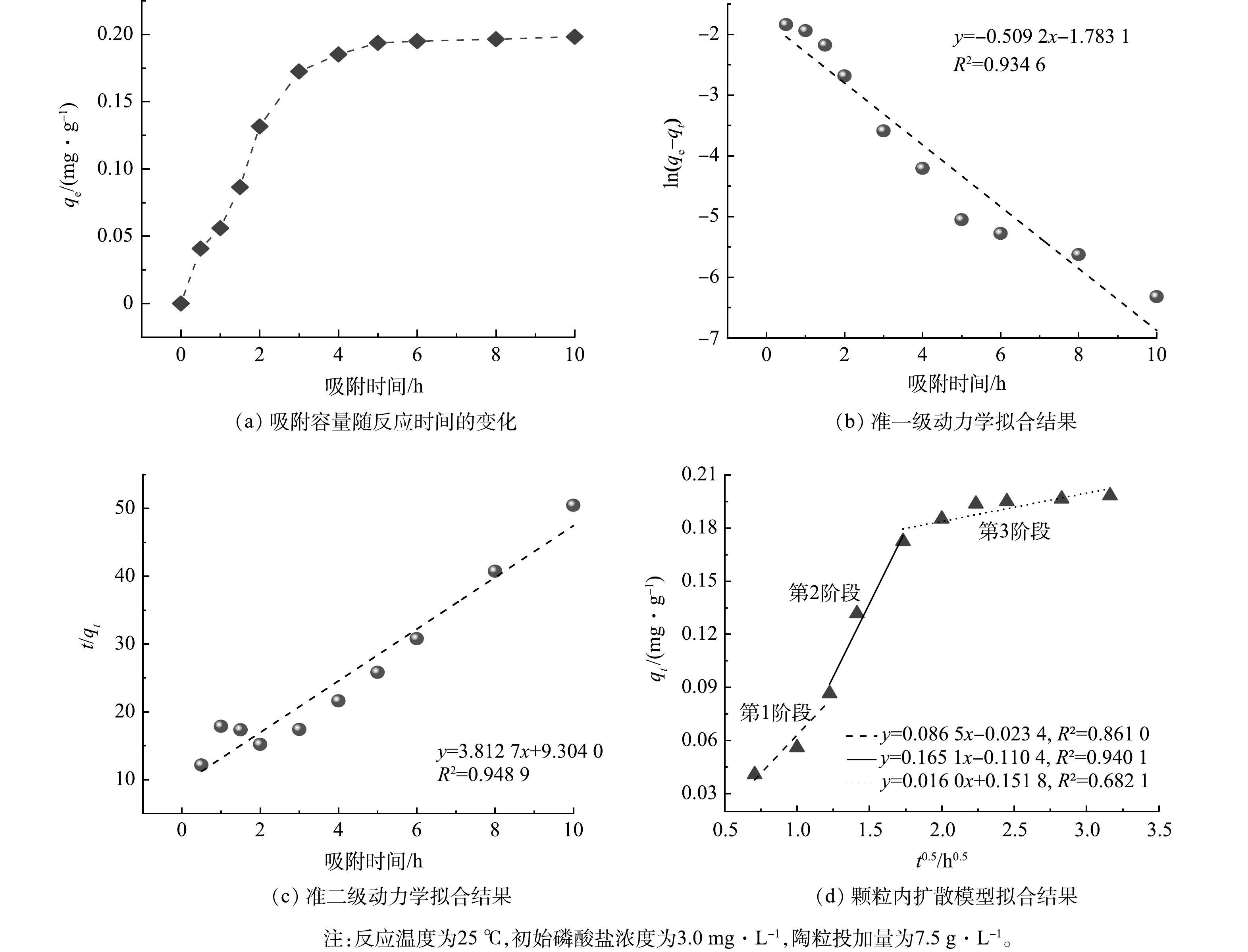
图3为陶粒对磷的去除过程及动力学拟合结果。由图3(a)可知,陶粒对磷的快速吸附发生在反应前3 h,至第6 h基本达到吸附平衡,反应至第10 h,陶粒对磷的吸附量为0.198 mg·g−1,去除率达98.46%。图3(b)~(c)的拟合结果表明,准一级动力学和准二级动力学均可准确描述陶粒对磷的吸附去除过程,由拟合所得的R2可见,准二级动力学具有更高的拟合度。准二级动力学方程假定化学吸附是限速步骤[27],因此,可认为陶粒对磷的吸附过程以化学作用为主。图3(d)为该吸附过程的颗粒内扩散模型拟合结果。由图3(d)可知,陶粒对磷酸盐的吸附可分为3个不同阶段:第1阶段为固液界面扩散过程(0~1.5 h),在此期间,磷酸盐通过固液界面扩散至陶粒外表面,此阶段主要由液膜扩散环节所控制;第2阶段为磷酸盐在陶粒孔隙内的扩散过程(1.5~3 h),在此期间,磷酸盐由陶粒外表面扩散至陶粒内部孔隙,进而扩散至陶粒内表面,此阶段主要由颗粒内扩散环节所控制;第3阶段为吸附阶段(3~10 h),此阶段磷酸盐在陶粒内表面发生吸附并逐步达到吸附平衡。这与图3(a)所揭示的反应过程基本一致。同时可以看出,第1阶段速率系数k1小于第2阶段速率系数k2, 说明磷酸盐的液膜扩散速率低于颗粒内扩散速率,该吸附过程同时受到表面扩散和颗粒内扩散的影响,增加水流在陶粒表面的剪切速率,或可进一步提升陶粒对磷的吸附效果。
-
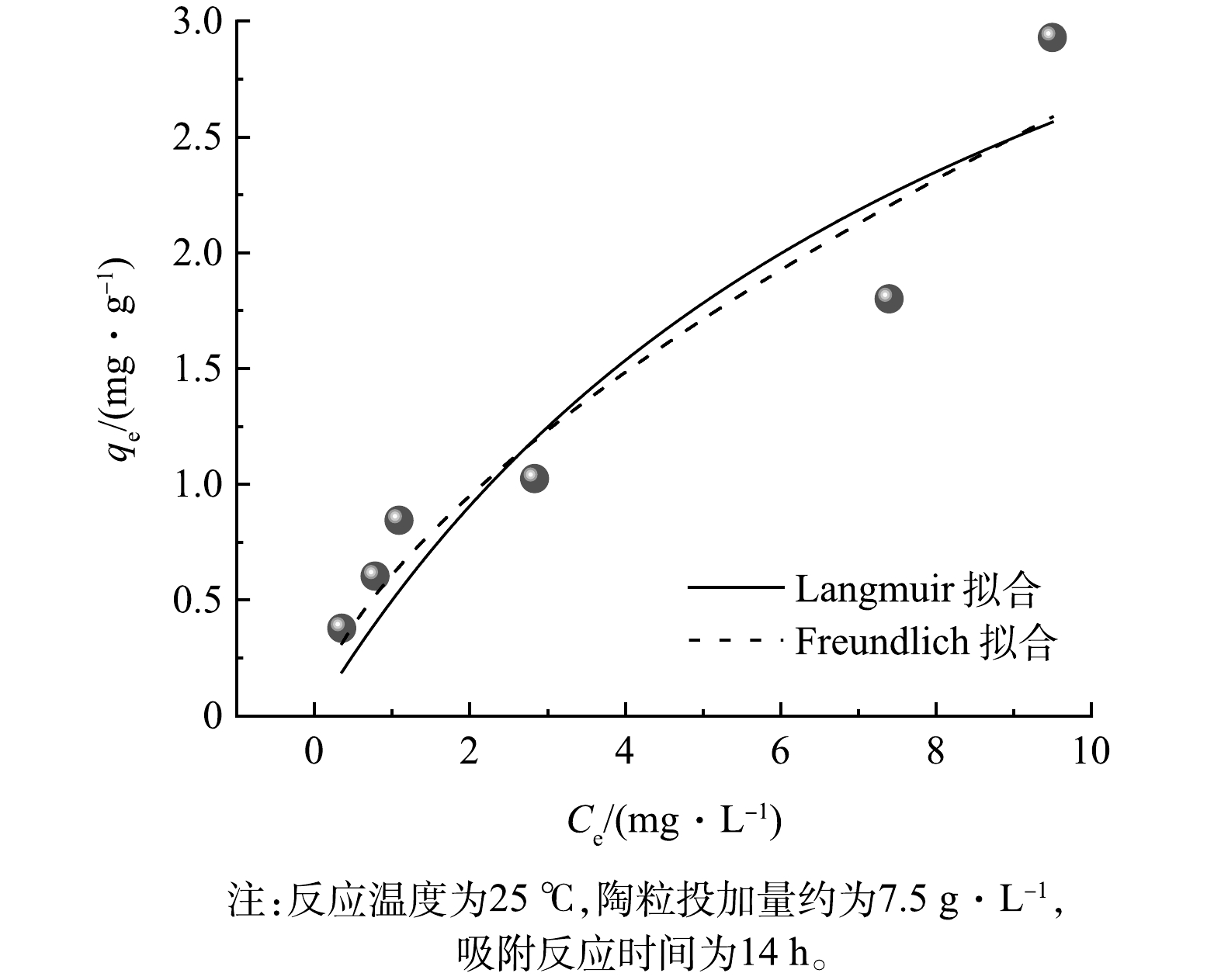
图4和表1分别为陶粒对水中磷的吸附等温线和拟合结果。实验结果表明,陶粒对磷的吸附更符合Freundlich模型。从表1数据可以看出,陶粒对磷的理论最大吸附量为5.005 mg·g−1。对固废基吸附剂材料的磷去除特性进行了总结,具体见表2。
从表2可知,李天鹏等[13]采用脱水污泥、粉煤灰等材料所制备固废基陶粒对磷的吸附容量为1.013 mg·g−1;WU等[26]研究发现,普通陶粒的磷吸附容量为1.182 mg·L−1,通过FeSO4和KMnO4改性后吸附量可提升至2.751 mg·g−1;蒋楠等[27]以磷矿粉和膨润土尾矿为主要原料烧制的复合陶粒,对磷的吸附量为0.352 mg·g−1; 张烨等[14]采用给水厂污泥和胶凝材料所制备免烧陶粒对磷的最大吸附量为5.297 mg·g−1;邢丽静等[28]利用白云石质磷尾矿和蒙脱石所制备多孔陶粒对磷的最大吸附量为4.749 mg·g−1;虞孝德等[29]通过铁尾矿和粉煤灰制备的铁尾矿陶粒对磷酸盐的最大吸附量为1.68 mg·g−1;其他常用材料包括红泥、粉煤灰、高炉矿渣等对磷的吸附量均小于1 mg·g−1[30-31]。
比较可知,本研究所制备陶粒具有较高的磷酸盐吸附容量。同时,本研究中陶粒吸附反应所需平衡时间较短,而在相关研究中陶粒对磷吸附平衡时间可达96 h[14]。研究表明铁氧化物与磷酸盐的结合速率较钙氧化物等快的多[32],因此推断本研究中相对较短的吸附平衡时间主要和铁锰污泥的加入有关。
-
1)陶粒形貌及比表面积分析。图5为陶粒SEM及表面主要元素分布图。由图5(a)~(b)可知陶粒表面粗糙,存在发达的孔隙结构,这为水中磷的吸附提供了有力条件。陶粒表面主要元素分布以图5(b)所示区域为基础进行测定。可以看出Fe、Mn、Si元素在陶粒表面分布均匀,说明不同材料在陶粒制备过程中得到了充分混合和反应;O元素分布表现出一定区域差异,这主要是不同元素的O结合能力及所形成的化学键不同所致;同时材料表面Mn元素信号密度相对较低,说明该污泥中Mn元素含量较少。
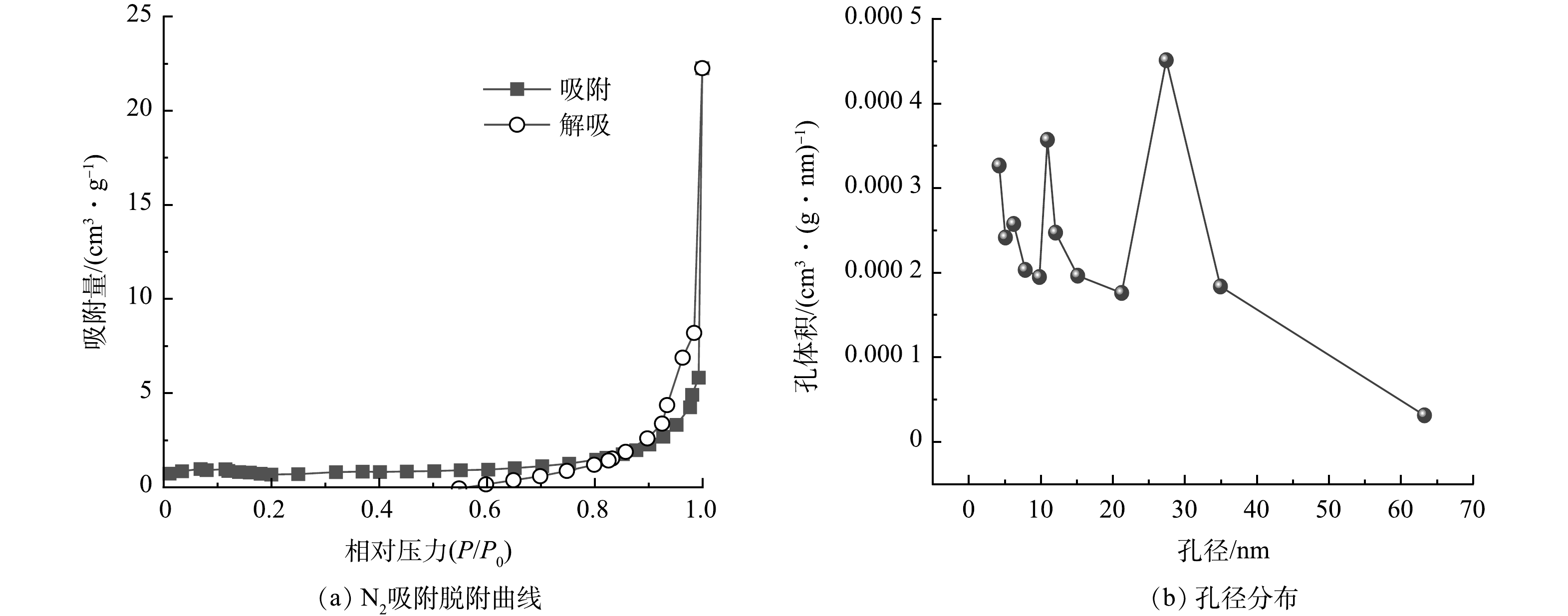
图6为陶粒N2吸附脱附曲线及孔径分布。由图6(a)中可以看出,2条曲线均属于Ⅳ型,由N2吸附曲线可以看出,在低压区陶粒与N2之间的作用力较弱,N2吸附量少,表明微孔在吸附过程中不起主导作用;同时该曲线在P/P0 为0.8~1.0时出现了H3型回滞环,表明该陶粒属介孔吸附材料[11]。由图6(b)可以看出,陶粒孔隙主要分布在4.22~63.28 nm。BET结果显示,该陶粒的比表面积为1.986 m2·g−1,孔容为
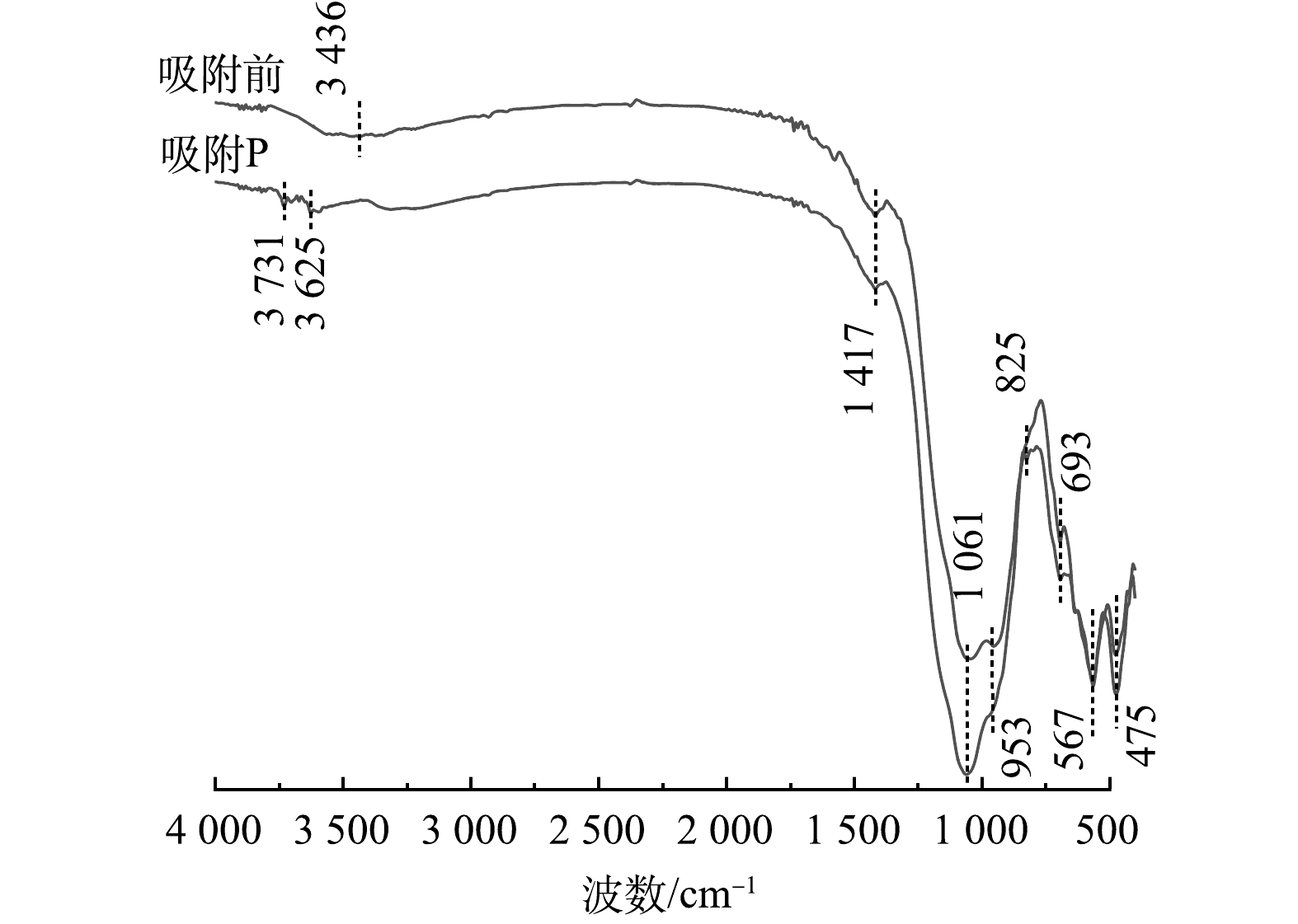
0.0187 cm3·g−1,平均孔径为17.989 nm。2)反应前后陶粒傅里叶变换红外光谱分析。 图7为陶粒反应前后的FTIR谱图。位于693、567和475 cm−1处的谱峰为Fe—O振动峰[33],其中567 cm−1处的谱峰还可能为Mn—O,Ca—O的振动峰。位于1 061 cm−1处的谱峰为T—O—Si(T为Si、Al、Fe等),Fe—OH、Si—OH和Mn—OH等的振动峰[34-37],同时还可能为磷酸盐的吸收峰[38]。吸附反应后,该峰强度明显增加,说明磷酸盐被吸附至陶粒表面。位于3 436 cm−1处的宽峰为陶粒表面吸附水或者羟基的吸收峰,反应后该峰发生变化,说明磷的吸附与陶粒表面-OH有关系。953 cm−1处的峰归属于Fe—O—OH的—OH基团[23, 39],吸附磷后其强度明显降低,说明磷酸盐和铁氧化物表面羟基发生作用而吸附在陶粒表面。
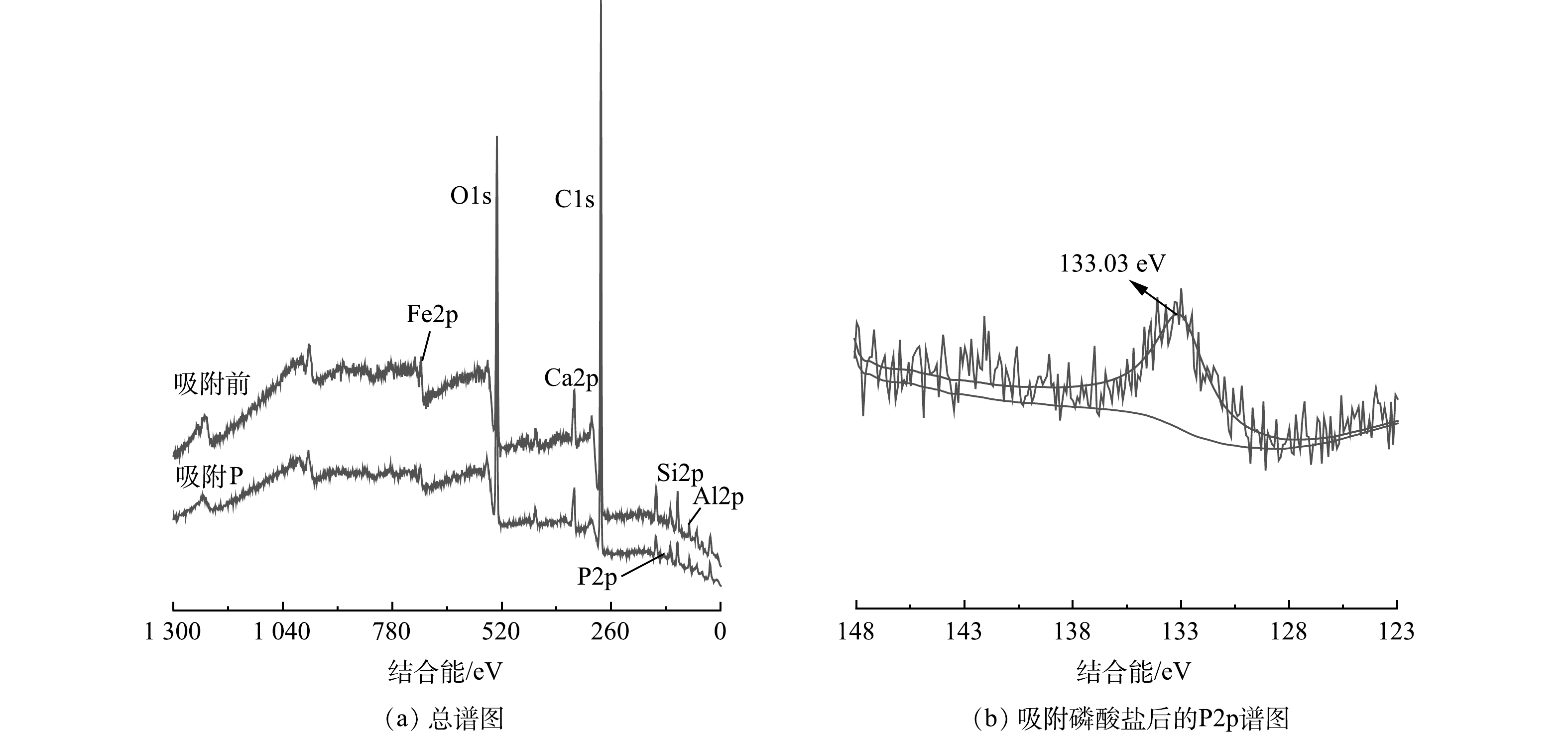
3)反应前后陶粒表面元素的XPS谱图分析。图8和表3分别为吸附反应前后陶粒表面元素的XPS谱图和元素组成。图8(a)为XPS总图谱,可以看出陶粒表面主要元素包括Fe、Si、O、C、Ca、Al等。在吸附水中磷酸盐后,陶粒表面检测出了较为显著的磷元素信号,并具有清晰的P2p精细谱(图8(b)),说明磷酸盐被有效吸附于陶粒表面。
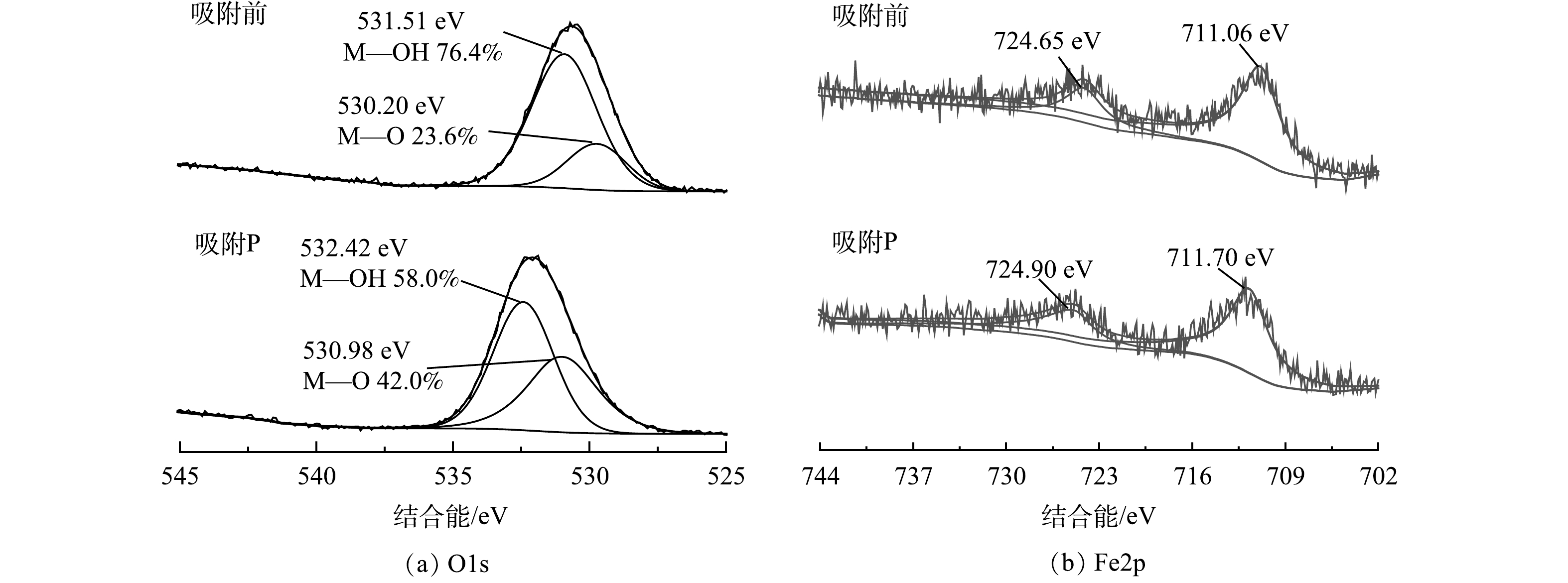
图9为吸附反应前后陶粒表面O和Fe的XPS谱图。由图9(a)可知,吸附反应前O的XPS谱图可拟合为2个峰,其中位于530.20 eV的峰可归因于M—O中的O(M表示Fe、Si、Ca、Al等元素),位于531.51 eV的可归属于M—OH中的O[22, 40-41]。
吸附磷酸盐后,M-OH结合能上升至532.42 eV,同时其含量由吸附前的76.4%下降至58.0%。在金属氧化表面吸附磷酸盐后将同时引入—OH基团[41],且P—OH、P—O−和M—OH的结合能十分接近,难以区分[22],因此,理论上吸附水中磷酸盐后,氧化物表面M-OH含量将会上升。而本研究中,吸附磷酸盐后,陶粒表面M—OH数量反而减少,说明磷吸附过程大量消耗了陶粒自身的M—OH,M—OH在磷吸附过程中起重要作用。由图9(b)可见,吸附水中磷酸盐后,陶粒中Fe元素结合能显著升高,这与相关研究中揭示的铁氧化物吸附磷酸盐后的表现一致[40],说明陶粒中的铁锰污泥材料在磷吸附中起到重要作用。
-
本研究以高岭土、铁锰污泥、生物质、氧化钙为基本原料,成功制备出可有效去除水中磷的生态陶粒,并对其结构特征以及磷吸附特性进行了研究,主要结论如下。
1)添加铁锰污泥可有效提升陶粒的磷去除效果,铁锰污泥添加量、焙烧温度可对陶粒吸附性能产生显著影响,当高岭土、铁锰污泥、生物质和氧化钙的质量比为5:3:1:1、焙烧温度为900 ℃时所制备的陶粒综合性能最佳。
2)铁锰污泥基生态陶粒可高效去除水中的磷,该陶粒对磷的吸附过程符合准二级动力学模型,Freundlich模型能更好地描述磷酸盐的吸附过程,颗粒内扩散模型显示,磷酸盐的吸附速率同时受表面扩散和颗粒内扩散的影响。
3) SEM和BET分析结果表明,该陶粒表面粗糙,为介孔吸附材料,FTIR、XPS表征发现所添加的铁锰污泥材料,主要是通过其表面羟基将水中磷酸盐有效吸附去除。
铁锰污泥基生态陶粒的制备及其对水中磷酸盐的去除性能
The preparation of the ecological ceramsite based on iron-manganese sludge and its performance on phosphate removal from water
-
摘要: 采用高岭土、除铁锰滤池反冲洗污泥、生物质、氧化钙等材料成功制备出铁锰污泥基生态陶粒,并探究了该陶粒的结构特征以及对水中磷的吸附性能。结果表明,铁锰污泥的添加量为30%,焙烧温度为900 ℃时所制备的陶粒综合性能最佳。当初始磷的质量浓度为3.0 mg·L−1,陶粒投加量为7.45 g·L−1,陶粒对磷酸盐的去除率达96.79%。吸附动力学结果表明,该陶粒对水中磷的去除过程符合准二级动力学;颗粒内扩散模型显示,磷酸盐的吸附速率同时受表面扩散和颗粒内扩散的影响;吸附等温实验表明Freundlich模型能更好地描述磷酸盐吸附过程。FTIR、XPS等表征发现铁锰污泥基陶粒,主要通过其表面羟基将水中磷有效去除。Abstract: The ecological ceramsite based on iron-manganese sludge was successfully prepared using the sludge from the filter for removing Fe and Mn, kaolin, biomass, and calcium oxide etc.. Its structural characteristics and performance on phosphorus adsorption from water were investigated. The results show that the ceramsite prepared with a 30% addition of iron-manganese sludge at sintering temperature of 900 ℃ had the best performance. When the initial concentration was 3.0 mg·L−1 and the dosage of ceramsite was 7.45 g·L−1, the removal rate of phosphorus could reach 96.79%. The results of adsorption kinetics indicate that the removal process of phosphorus from water by the ceramsite fitted with the pseudo-second-order model; the simulation of the intra particle diffusion model shows that the adsorption rate of phosphorus was depended on both surface and intra particle diffusion; the adsorption isotherm experiments show that Freundlich model could better describe the adsorption process of phosphorus. FTIR, XPS and other characterizations suggest that the surface hydroxyl groups of the ceramsite based on iron-manganese sludge mainly contributed to effective phosphate adsorption from water.
-
Key words:
- ceramsite /
- phosphorus /
- adsorption /
- iron-manganese sludge
-

-
表 1 陶粒对水中磷的吸附等温模型拟合结果
Table 1. Fitting results of adsorption isotherm model of phosphorus from water by ceramsite
Langmuir Freundlich qmax
(mg·g−1)KL
(L·mg−1)R2 1/n KF
(mg·g−1·(L·mg−1)1/n)R2 5.005 0.110 6 0.851 0 0.643 1 0.608 1 0.900 8 表 2 不同基质对磷酸盐的吸附效果
Table 2. The phosphate adsorption performance of different substrates
基质类型 制备材料 实验质量浓度/(mg·L−1) 最大吸附量/(mg·g−1) 参考文献 铁锰污泥基生态陶粒 高岭土、铁锰污泥、生物质、氧化钙 3~30 5.005 本研究 固废基陶粒 脱水污泥、粉煤灰、河道底泥、CaCO3、Na2SiO3 2~17 1.013 [13] 改性陶粒 普通陶粒、HCl、FeSO4、KMnO4 10~100 普通陶粒:1.182
改性陶粒:2.751[26] 复合陶粒 磷矿粉、膨润土尾矿、竹粉 1~4 0.352 [27] 给水厂污泥免烧陶粒 给水厂污泥、胶凝材料、粉煤灰、激发剂 100 5.297 [14] 多孔陶粒 磷尾矿、蒙脱石、硬脂酸颗粒 5~200 4.749 [28] 铁尾矿陶粒 铁尾矿、粉煤灰 10 1.68 [29] 其他材料 红泥、粉煤灰、高炉矿渣 — 红 泥:0.909
粉 煤 灰:0.556
高炉矿渣:0.345[30-31] 表 3 反应前后陶粒表面元素组成
Table 3. Composition of the elements on the surface of ceramsite before and after the reaction %
样品 C O Si Ca Fe Al P 吸附P前 65.42 21.17 6.67 2.17 1.64 2.93 / 吸附P后 52.57 27.68 7.58 3.28 1.84 6.21 0.83 -
[1] SHAO Q, ZHANG Y, LIU Z, et al. Phosphorus and nitrogen recovery from wastewater by ceramsite: Adsorption mechanism, plant cultivation and sustainability analysis[J]. Science of the Total Environment, 2022, 805: 150288. doi: 10.1016/j.scitotenv.2021.150288 [2] 郭训文, 李炳辉, 黄永秋, 等. 执行准Ⅳ类地表水标准的印染废水深度处理实例[J]. 中国给水排水, 2019, 35(4): 89-92. [3] 黎鹏宇, 黄天寅, 沈钒. 生活污水处理厂准四类水质提标改造工程实例[J]. 水处理技术, 2023, 49(8): 141-144. [4] 周合喜, 张金松, 张庆珮. 多级AO工艺在某高排放标准污水厂的优化探讨[J]. 中国给水排水, 2022, 38(20): 8-13. [5] WANG T, ZHU B, ZHOU M. Ecological ditch system for nutrient removal of rural domestic sewage in the hilly area of the central Sichuan Basin, China[J]. Journal of hydrology, 2019, 570: 839-849. doi: 10.1016/j.jhydrol.2019.01.034 [6] 陈思佳, 黄丹, 高彦宁, 等. 人工湿地模块化基质脱氮除磷性能研究[J]. 水处理技术, 2024, 50(2): 44-50. [7] 王荣, 贺锋, 徐栋, 等. 人工湿地基质除磷机理及影响因素研究[J]. 环境科学与技术, 2010, 33(6E): 12-18. [8] 赵东源, 张生, 赵胜男, 等. 基于除磷效果的人工湿地基质组合筛选及影响因素的动力学分析[J]. 环境污染与防治, 2018, 40(10): 1085-1089. [9] 王志超, 王战, 李卫平, 等. 寒旱地区生态沟渠基质去除氨氮和磷最优配比筛选及影响因素[J]. 水土保持学报, 2020, 34(1): 262-267. [10] 何强, 陈博文, 杨雨静, 等. 3种人工湿地基质材料对氨氮的吸附特性[J]. 环境科学, 2024, 45(3): 1577-1585. [11] 王青春, 梁宏, 彭红, 等. PO[J]. 四川轻化工大学学报(自然科学版), 2023, 36(3): 10-19. [12] 郑伍魁, 赵丹, 朱毅, 等. 陶粒工程应用的趋势分析及研究进展[J]. 材料导报, 2023, 37(7): 102-113. [13] 李天鹏, 王正庆, 丁华栋, 等. 固废基陶粒对含磷废水的处理研究[J]. 环境科学与技术, 2023, 46(S2): 108-113. [14] 张烨, 余轶鹏, 汪炎, 等. 给水厂污泥免烧结陶粒强化尾水除磷除氟性能研究[J]. 工业用水与废水, 2023, 54(5): 62-67. [15] 罗书舟, 王东田. 净水污泥柠檬酸钠改性焙烧制备陶粒吸附剂及其对废水中氨氮吸附性能的研究[J]. 安全与环境工程, 2021, 28(5): 230-239. [16] 张瑞峰, 杨世莲, 杨靖, 等. MnOx 同步除锰氨氮滤池的快速启动及污染物去除机制[J]. 中国环境科学, 2023, 43(1): 197-205. [17] 曾辉平, 翟龙雪, 李冬, 等. 基于铁泥的磁性水处理材料制备及应用进展[J]. 环境科学, 2022, 43(1): 26-36. [18] H ZENG, C LIU, F WANG, et al. Disposal of iron-manganese sludge from waterworks and its potential for arsenic removal[J]. Journal of Environmental Chemical Engineering, 2022, 10(5): 108480. doi: 10.1016/j.jece.2022.108480 [19] 曾辉平, 王繁烁, 于亚萍, 等. 壳聚糖海藻酸钠铁锰泥吸附剂制备与除As(V)研究[J]. 中国环境科学, 2020, 40(3): 1146-1155. [20] 江凌欣, 程亚, 黄延林. 地下水厂泥饼的活化及其负载滤料去除水中氨[J]. 中国环境科学, 2023, 43(8): 4024-4031. [21] 蔡德所, 散剑娣, 欧文昌, 等. 底泥陶粒的制备及其性能研究[J]. 金属矿山, 2022, 557: 229-237. [22] ZHANG L, LIU Y, WANG Y, et al. Investigation of phosphate removal mechanisms by a lanthanum hydroxide adsorbent using p-XRD, FTIR and XPS[J]. Applied Surface Science, 2021, 557: 149838. doi: 10.1016/j.apsusc.2021.149838 [23] DU X, HAN Q, LI J, et al. The behavior of phosphate adsorption and its reactions on the surfaces of Fe–Mn oxide adsorbent[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017, 76: 167-175. doi: 10.1016/j.jtice.2017.04.023 [24] ZHANG R, YANG S, DONG C, et al. Synthesized akhtenskites remove ammonium and manganese from aqueous solution: removal mechanism and the effect of structural cations[J]. Rsc Advances, 2021, 11: 33798. doi: 10.1039/D1RA06025B [25] YIN Y, XU G, LI L, et al. Fabrication of ceramsite adsorbent from industrial wastes for the removal of phosphorus from aqueous solutions[J]. Journal of Chemistry, 2020, 2020: 8036961. [26] WU L, LIU C, HU Y, et al. Dephosphorization using ceramsites modified by coprecipitation with FeSo4 and KMnO4 and high-temperature combustion[J]. Journal of Water Process Engineering, 2020, 34: 101162. doi: 10.1016/j.jwpe.2020.101162 [27] 蒋楠, 李彬, 赵明星, 等. 复合陶粒对水中氨氮和磷的吸附研究[J]. 沈阳农业大学学报, 2022, 53(5): 600-610. [28] 邢丽静, 梁欢, 田承涛, 等. 白云石质磷尾矿制备多孔陶粒对含磷废水吸附特性研究[J]. 水处理技术, 2023, 49(12): 101-107. [29] 虞孝德, 王道涵. 铁尾矿陶粒的制备及其除磷性能研究[J]. 工业水处理, 2024: 1053. [30] 高耀文, 段宁, 吴克明. 粉煤灰人工湿地基质对磷吸附性能的研究[J]. 工业安全与环保, 2012, 38(12): 3-6. [31] 陈丽丽, 赵同科, 张成军, 等. 不同人工湿地基质对磷的吸附性能研究[J]. 农业环境科学学报, 2012, 31(3): 587-592. [32] QIN Z, SHOBER A L, SCHECKEL K G, et al. Mechanisms of phosphorus removal by phosphorus sorbing materials[J]. Journal of Environmental Quality, 2018, 47(5): 1232-1241. doi: 10.2134/jeq2018.02.0064 [33] NIU J, DING P, JIA X, et al. Study of the properties and mechanism of deep reduction and efficient adsorption of Cr (VI) by low-cost Fe3O4-modified ceramsite[J]. Science of the Total Environment, 2019, 688: 994-1004. doi: 10.1016/j.scitotenv.2019.06.333 [34] XIAO T, FAN X, WANG H, et al. Removal of phosphorus from water bodies using high-performance ceramsite prepared from solid wastes[J]. Separation Purification Technology, 2024, 342: 126962. doi: 10.1016/j.seppur.2024.126962 [35] CHEN Y, WANG N, AN S, et al. Synthesis of novel hierarchical porous zeolitization ceramsite from industrial waste as efficient adsorbent for separation of ammonia nitrogen[J]. Separation Purification Technology, 2022, 297: 121418. doi: 10.1016/j.seppur.2022.121418 [36] CHENG Y, ZHANG S, HUANG T, et al. Effects of coagulants on the catalytic properties of iron–manganese co-oxide filter films for ammonium and manganese removal from surface water[J]. Journal of cleaner production, 2020, 242: 118494. doi: 10.1016/j.jclepro.2019.118494 [37] LIKUS M, KOMOROWSKA-KAUFMAN M, PRUSS A, et al. Sorption properties of groundwater treatment residuals containing iron oxides[J]. Journal of Environmental Chemical Engineering, 2023, 11(5): 110342. doi: 10.1016/j.jece.2023.110342 [38] LIU X, YANG S, LIU S, et al. Performance and mechanism of phosphorus removal by slag ceramsite filler[J]. Process Safety Environmental Protection, 2021, 148: 858-866. doi: 10.1016/j.psep.2021.02.016 [39] CHENG Y, ZHANG Y, XIONG W, et al. Effects of iron doping on catalytic oxidation activity of Mn-based co-oxide filter media for removal of ammonium and manganese from groundwater[J]. Journal of Cleaner Production, 2022, 332: 130091. doi: 10.1016/j.jclepro.2021.130091 [40] MALLET M, BARTHéLéMY K, RUBY C, et al. Investigation of phosphate adsorption onto ferrihydrite by X-ray photoelectron spectroscopy[J]. Journal of Colloid Interface Science, 2013, 407: 95-101. doi: 10.1016/j.jcis.2013.06.049 [41] LU J, LIU H, ZHAO X, et al. Phosphate removal from water using freshly formed Fe–Mn binary oxide: adsorption behaviors and mechanisms[J]. Colloids Surfaces A: Physicochemical Engineering Aspects, 2014, 455: 11-18. doi: 10.1016/j.colsurfa.2014.04.034 -




 下载:
下载: