-
目前,我国生活垃圾无害化处理主要有3种方式:卫生填埋、焚烧、堆肥,其中卫生填埋技术因其成本低,技术相对成熟成为我国主要垃圾处理方式[1]。垃圾填埋过程中极易产生大量恶臭气体,主要成份分为含硫化合物、含氮化合物、卤素及衍生物等,其中硫化氢 (H2S) 和氨气 (NH3) 为含量最多[2]。二者均为有毒腐蚀性恶臭气体,长期吸入对人体健康产生危害[3]。采用覆盖材料除臭与药剂喷洒的方法结合进行恶臭气体处理,在实际工程中应用较多,但是该方法以恶臭气体高效捕集为前提。在填埋场中对垃圾短途转运,为敞开体系,无法实现对恶臭气体的捕集去除[4]。本研究借鉴医药喷涂成膜 (后面简称“喷膜”) 原理,研发复合型喷膜配方,使之兼具除臭剂和覆盖功能,从而实现垃圾填埋场中途转运恶臭气体阻隔。
阳离子聚合物和阴离子聚合物通过静电作用,经初级聚合、内部重排、疏水聚合形成聚电解质复合物膜,兼具良好的机械强度和稳定性,被广泛应用于做离子交换膜、纳滤和反渗透等薄膜,应用于生物医学、食品工业[5-7]。壳聚糖是阳离子聚电解质,由乙酰基葡萄糖胺 (GlcNAc) 和葡萄糖胺 (GlcN) 通过β-1,4-糖苷键连接的多糖链经脱乙酰化产生,水溶液中含有大量氨基 (-NH2) 基团[8]。海藻酸钠是由β-D-甘露醛酸 (M) 和α-L-古醛酸 (G) 通过1,4-糖苷键连接的线性多糖[9]。在中性或碱性条件下,酸性的羧基 (-COOH) 会与钠离子结合,形成海藻酸钠[10]。当壳聚糖和海藻酸钠混合时,壳聚糖中的氨基与海藻酸钠的羧基通过离子键产生相互作用,生成具有较高的机械强度和生物相容性的聚电解质复合物膜[11]。聚合物膜的机械性质、孔隙度、水通量和选择性受pH影响,pH变化可能会导致膜结构解体[12]。而碳酸氢钠水溶液中的HCO3−可作为pH缓冲剂,不但能够调节壳聚糖-海藻酸钠聚电解质复合物膜在pH变化时稳定性,而且HCO3−还可与H2S、NH3恶臭气体发生化学反应,作为除臭剂增强对恶臭气体的截留[13]。首先,该配方少量药剂溶解于水中,在需要的阻隔时喷洒在存余垃圾界面,使其成为具有阻隔作用的薄膜,具有使用方便的特点。其次,少量药剂喷涂在存余垃圾表面,成本可控。第三,选用的材料环境友好。而传统的聚乙烯 (PE) 、聚丙烯 (PP) 薄膜物理阻隔薄膜,体积大、使用不便,而且上述薄膜会产生塑料垃圾,造成额外的处理成本。
本研究选取壳聚糖和海藻酸钠为成膜基质材料,添加化学除臭剂碳酸氢钠制备喷膜液,喷涂成膜实现对H2S和NH3气体阻隔。喷涂薄膜的主要的溶剂是水,添加的助溶剂、成膜材料和抗菌材料,都是具有生物安全性的,是食品医药用的材料,具有环保、高效的特点。同时对喷膜进行了傅里叶变换红外光谱、扫描电镜、X射线电子衍射等结构表征,并研究了喷膜的气体截留率和抗张力性能分析。通过添加甘油增塑剂、肉桂醛防蝇杀虫剂、茶树精油香料,及苯甲酸钠防腐剂对复合膜进行优化,以期开发出高效能成膜配方,使其适用于实际垃圾填埋场短途垃圾转运过程的恶臭气体阻隔。
-
海藻酸钠 (分析纯,粘度≥0.02,纯度≥99.5%) ,壳聚糖 (分析纯,脱乙酰度80.0~95.0) ,碳酸氢钠 (分析纯,NaHCO3) ,吐温80 (分析纯,C24H4O6) ,甘油 (分析纯,C3H8O3) ,苯甲酸钠 (分析纯,C7H5NaO2) ,茶树精油 (分析纯) ,柠檬烯 (分析纯,C10H16) ,均来自国药集团。
-
手持泵吸式H2S检测仪 (BSQ-BH2S,上海本杉仪器设备有限公司) ,手持泵吸式NH3检测仪 (BSQ-BNH3,上海本杉仪器设备有限公司) ,数显恒温磁力搅拌器 (85-2,上海本杉仪器设备有限公司) ,数显式推拉仪 (HLD+HP-500,乐清艾德堡仪器有限公司) ,电动搅拌器 (D2004W,上海梅颖浦仪器仪表制造有限公司) ,扫描电子显微镜 (ZeissGemini300,上海卡尔蔡司科技管理有限公司) ,傅里叶红外光谱仪 (Nicolet5700,上海赛德威科技有限公司) ,接触角测试仪 (JY-82,承德鼎盛试验机检测设备有限公司) 。
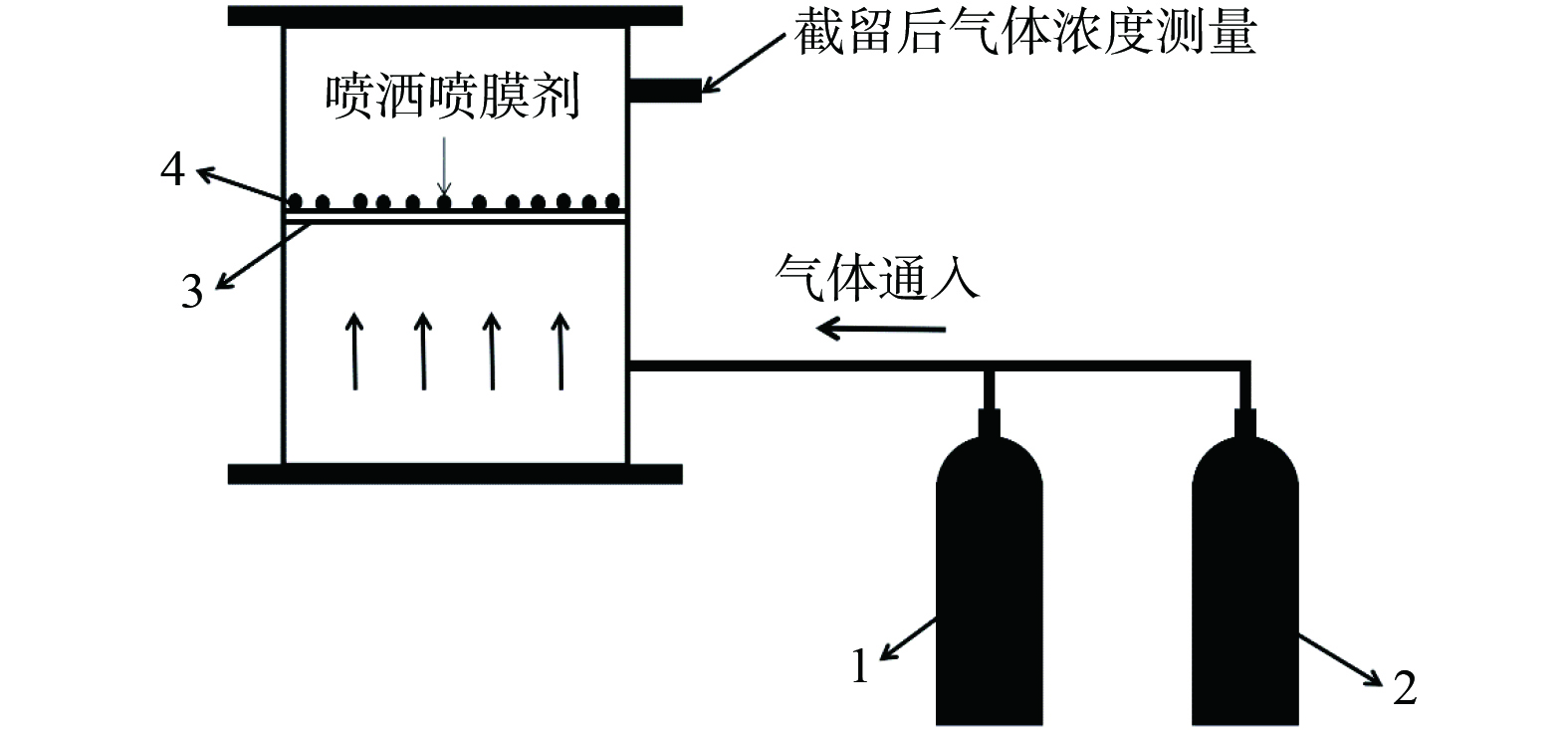
实验装置“升流式实验反应装置”参考生物滴滤塔构造[14-17],反应器构造如图1所示,由直径100 mm,高600 mm的有机玻璃制成。在400 mm处设置孔径为1.5 mm的布气板,橡胶颗粒放置于布气板上,橡胶填料层高度为50 mm。喷淋装置使用50 mL小型塑料喷瓶。
-
1) 复合膜液喷洒。使用50 mL小型喷枪为实验室模拟喷洒装置,每次均匀喷洒10~15 mL成膜药剂于橡胶填料层表面[17]。H2S、NH3气体均由浓度为70 mg∙m−3标准气瓶提供,用转子流量计控制气瓶出口气体流速为0.5 L∙min−1,使用手持泵吸式流量计测量对应出口处H2S、NH3浓度。每组实验运行时间为30 min,每次气体测量时间为1 min,每隔5 min测量1次,每组共计测量6次。每组实验取3组平行样,以平均值计为出口浓度。
2) 复合膜液制备。称取适量壳聚糖、海藻酸钠溶解于100 mL去离子水中,在45 ℃的温度下搅拌20 min,使其成为均匀溶液。为了提高喷膜性能,在喷膜液中添加适量的碳酸氢钠 (NaHCO3) ,在300 r∙min−1的转速下搅拌15 min,使其与高分子溶液充分混合形成均一溶液。选取海藻酸钠和壳聚糖溶液浓度均为2%,为确定海藻酸钠、壳聚糖、碳酸氢钠复合膜的最佳配比条件,单因素实验中设置5个因素水平,进行3次重复实验。以H2S和NH3的气体截留率为评价指标,确定最佳的单因素配比成分。
①海藻酸钠质量与壳聚糖的质量比为10∶0、8∶2、6∶4、4∶6、2∶8;碳酸氢钠浓度为1%。
②碳酸氢钠浓度为0%、1.0%、2.0%、3.0%、4.0%;海藻酸钠与壳聚糖质量为8∶2。
为提升复合膜的工程性能,在单因素实验制备的具有最佳截留率的复合膜溶液中添加不同浓度的增塑剂甘油、表面活性剂吐温80、苯甲酸钠防腐剂以及肉桂醛作为防蝇杀虫剂[18]。以提升海藻酸钠-壳聚糖-碳酸氢钠复合膜的综合性能。
3) 成型膜制备。将制备好的高分子复合膜溶液静置完全消泡后,均匀倾倒于150 mm一次性无菌培养皿表面。培养皿平铺放置于实验操作台上,室温条件下自然干燥3~4 d后,进行揭膜处理[19]。揭除的成型膜放置于干燥器中保存备用。
-
1) 傅里叶变换红外光谱 (FTIR)。选取充分干燥的复合膜,使用红外光谱仪Thermo Scientific Nicoleti S5,在ATR模式下进红外光谱表征,波数范围控制在4 000~500 cm−1,扫描次数32,分辨率4 cm−1[20]。
2) 扫描电镜图谱 (SEM) 。取完全干燥后的复合膜样品,制成2 cm×2 cm样品,用双面胶以水平方向固定于扫描电镜ZEISS MERLIN Compact样品台上。设置实验条件为:扫描电镜电子束加速电压为10 kV,放大倍数为2 500倍[21]。
3) X射线衍射图谱 (XRD) 。X射线衍射能够测试薄膜的结晶程度。其中入射线波长为0.154 18 nm,电压40 KV,电流40 mA,扫描范围为10~80°,扫描步长0.04°,扫描速度38.2秒/步[22]。
4) 热重分析 (TG) 。取完全干燥后的复合膜样品5~8 mg,放置于坩埚中,在氮气保护环境下使用TATGA55仪器进行热重分析。温度从20 ℃升温到600 ℃,热重升温速度为10 ℃∙min−1。根据复合膜热失重的相关曲线,进行相容性判断[23]。
-
1) 膜厚度。将完全干燥后的复合膜裁剪成2 cm×10 cm的长条状,使用精度为0.001 mm的数显式千分测厚仪测量厚度。长条状薄膜均匀取3个点 (标距中心和标距两端) 进行厚度测量,测量结果取中位值。每张复合膜取3组长条,取平均值为最终值。实验中制备的薄膜如图2所示。
2) 机械强度和断裂伸长率。机械强度和断裂伸长率测定均参照国家标准GB/T1040-2006。将完全干燥后的复合膜裁剪成2 cm×10 cm的长条状,两端夹置于HLD数显式推拉力计,滚轮摇动速度为500 mm∙min−1,以薄膜长条断裂为标准,测定薄膜的机械强度和断裂伸长率[24]。每个样品做3个平行样,结果取平均值。
机械强度公式如式(1)所示。
式中:TS为机械强度,KPa;Fm为试样断裂时承受的最大拉为,N;b为膜样品的宽度,mm;d为膜样品的厚度,mm。
断裂伸长率公式如式(2)所示。
式中:
$ E $ 为膜样断裂伸长率,%;$ {L}_{1} $ 为膜样初始长度,mm;$ {L}_{0} $ 为膜样断裂长度,mm。3) 水蒸气透过率 (WVP) 。使用量杯法测量复合膜的水蒸气透过率。将成型膜剪成75 mm
$ \times $ 75 mm见方正方形,放置于盛有11 mL蒸馏水的数量杯口,盖上杯盖后用橡皮筋固定并用凡士林进行密封处理[25]。每隔6 h称重1次,每组实验做3组平行样。水蒸气透过率计算公式如式(3)所示。
式中:WVP为水蒸气透过率,g·m·h−1·m2·Pa;
$ {\mathrm{A}}_{m} $ 为稳定质量的增量,g;A为膜样的面积,m2;$ {\mathrm{A}}_{t} $ 为测定的时间间隔,h;d为膜的平均厚度,mm;$ {\mathrm{A}}_{p} $ 为膜样两侧的水蒸气压差,Pa,25 ℃时为3.168$ \times $ 103 Pa。 -
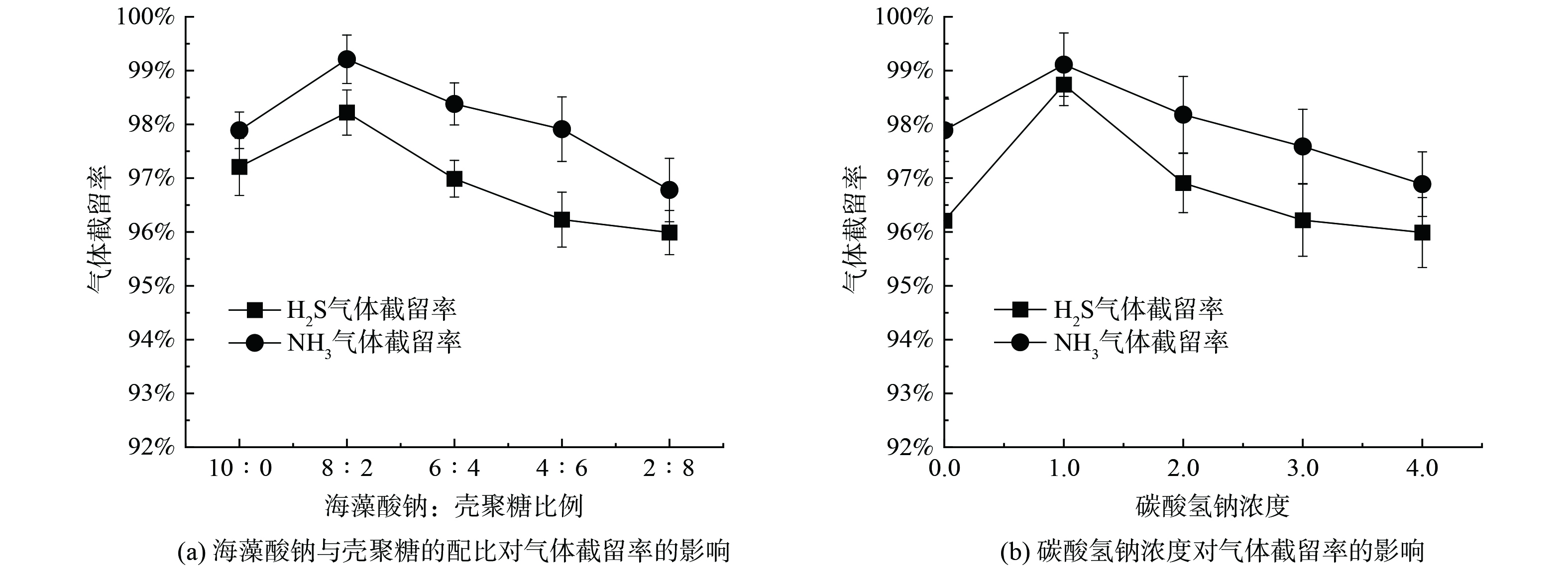
首先筛选海藻酸钠-壳聚糖-碳酸氢钠复合膜,从而使其具备所要求的H2S和NH3的截留率。按照海藻酸钠与壳聚糖的质量比分别为比10∶0、8∶2、6∶4、4∶6和2∶8,其在水中的浓度分别为2%,制备成喷膜配方后制备成喷膜。控制碳酸氢钠浓度为1.0%,由图3(a)可知随着海藻酸钠;壳聚糖比例增加,H2S和NH3气体截留率呈先上升后下降趋势,当海藻酸钠∶壳聚糖配比为8∶2时达到最大的气体截留率。此时复合膜对H2S气体截留率最高可达98.22%,NH3气体截留率最高可达99.21%。与比例为10∶0时,即单组分海藻酸钠行程的喷膜相比,随着壳聚糖分子的添加,截留率增加。这是由于海藻酸钠带负电荷,壳聚糖带正电荷,两者之间通过正负电荷作用,交联,形成的致密网状结构提高了复合膜的阻气效能[11]。但随着壳聚糖配比增加,溶液中聚氧离子含量增加,pH下降,溶液中聚阴离子的解离受到抑制,复合物形成困难[26-28]。进而导致海藻酸钠自身阻气截留优势丧失,新形成的聚电解质无法进行代替性的阻气截留。因此,当海藻酸钠:壳聚糖比例超过8:2峰值后,壳聚糖占比的增加反而是的气体截留率降低。
碳酸氢钠溶解在水中形成的HCO3− 可作为pH调节离子[13],加入到海藻酸钠-壳聚糖水溶液体系中调节pH,调节海藻酸钠-壳聚糖溶液稳定性,避免由于凝聚而产生沉淀。复合膜溶液固定海藻酸钠:壳聚糖配比为8∶2不变,碳酸氢钠浓度梯度为0%、1.0%、2.0%、3.0%、4.0%,制备成薄膜后进行H2S和NH3气体截留率实验。由图3(b)可知,随着NaHCO3浓度增加,海藻酸钠-壳聚糖-碳酸氢钠复合膜对气体截留率呈先上升后下降趋势,并在NaHCO3浓度为1%时达到最大截留率。此时NH3气体截留率为99.11%,H2S气体截留率为98.74%。这可能是NaHCO3提供弱碱性环境,存在的OH− 为带正电荷的壳聚糖提供阴离子,使得海藻酸钠-壳聚糖复合聚电解质溶液保持在最佳pH状态,从而结构稳定。NaHCO3含量增加,海藻酸钠和壳聚糖压缩复合膜微观孔隙,形成致密牢固的聚合物网状膜进而提高气体的截留效果。但当NaHCO3超过一定的pH值,溶液pH过高,多余OH−与带正电荷的壳聚糖分子反应,消耗掉部分壳聚糖以抑制复合膜的形成。同时,随着pH值增加,溶液呈碱性,聚阴离子完全解离,聚合物的溶解度降低,并以沉淀形式析出,复合膜的气体阻隔性能随之降低[9]。
-
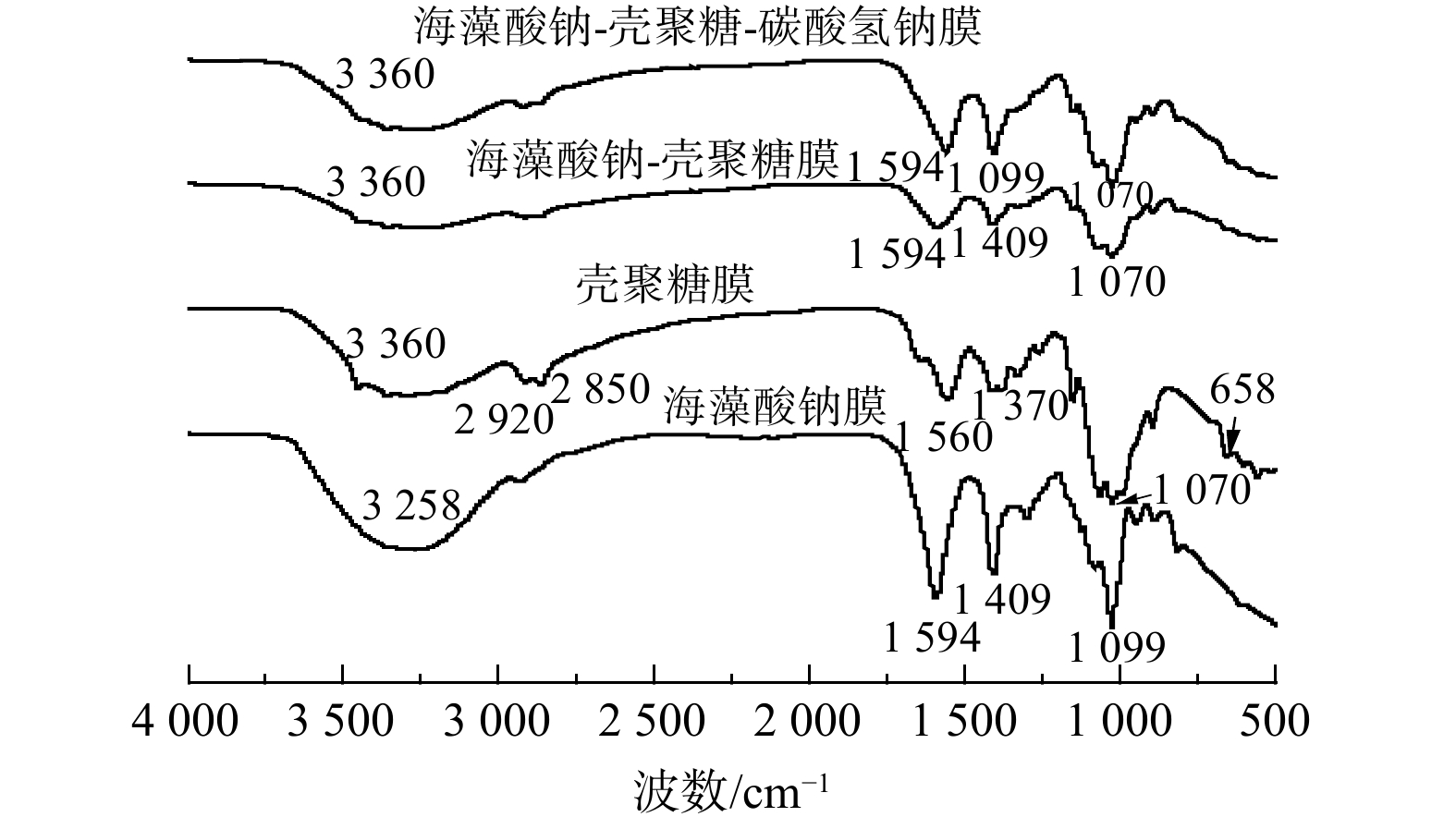
1) 傅里叶红外光谱 (fourier transform infrared spectroscopy,FTIR) 。FTIR鉴定海藻酸钠-壳聚糖-碳酸氢钠复合膜中的特定化学基团,如羟基、酯基、酰胺基等,分析复合膜的气体截留原理。从图4可知,在海藻酸钠红外光谱中,1 099 cm−1处为-C-O伸缩振动峰,3 258 cm−1的吸收带,对应于-OH的伸缩振动峰。1 594和1 409 cm−1处的吸收峰,分别为COO-的反对称伸缩振动和对称伸缩振动吸收峰。壳聚糖红外光谱中,3 360 cm−1处峰为-OH和-NH2伸缩振动缔合峰,2 920 cm−1为-CH3伸缩振动吸收峰和2 850 cm−1处为-CH2伸缩振动吸收峰,证明壳聚糖脱乙酰度较高。1 560 cm−1处出现了为-NH2吸收振动峰,1 370 cm−1处出现了C-CH3乙酰胺氨基吸收峰,说明壳聚糖中仍存在一定数量的乙酰氨基,1 070和658 cm−1为壳聚糖的结晶峰。海藻酸钠-壳聚糖复合膜与海藻酸钠单组分成膜相比,1 594和1 409 cm−1处COO-的反对称伸缩振动和对称伸缩振动吸收峰明显变宽,并向低波数处移动,说明海藻酸钠和壳聚糖混合生成聚电解质[29]。与单组分壳聚糖膜相比,海藻酸钠-壳聚糖复合膜在3 360 cm−1处的峰明显变宽,可能是由于两者之间的静电作用,产生NH4+,而导致的峰[30]。海藻酸钠-壳聚糖-碳酸氢钠复合膜与海藻酸钠-壳聚糖二元复合膜相比,1 594、1 409、3 360 cm−1处吸收峰明显变窄,说明碳酸氢钠可有效抑制海藻酸钠-壳聚糖聚电解质沉淀的生成,提升了海藻酸钠-壳聚糖相容性、稳定性,进而增加了复合膜的网状致密性。
2) 扫描电镜图 (scanning electron microscope,SEM) 。SEM能够从微观尺度上观察复合膜的表面形貌,如纹理、孔洞、裂纹等结构,分析混合膜的致密性和均匀性[31]。根据图5(a),可知海藻酸钠单组分膜有均匀分布的突起,无明显孔径产生,成膜性能良好。从图5(b)可知,壳聚糖单组分膜表面较为光滑平整,呈现片状结构,无明显孔径产生。从图5(c)可知海藻酸钠-壳聚糖复合膜有明显褶皱形成、粗糙度较高,说明海藻酸钠-壳聚糖两者复配,溶解性较差,能够形成聚离子复合物析出而导致的。从图5(d)可知,加入碳酸氢钠后,海藻酸钠-壳聚糖-碳酸氢钠复合膜的褶皱明显减少,说明碳酸氢钠作为pH调节剂,提高了海藻酸钠-壳聚糖聚电解质溶液的稳定性以及复合膜的相容性。
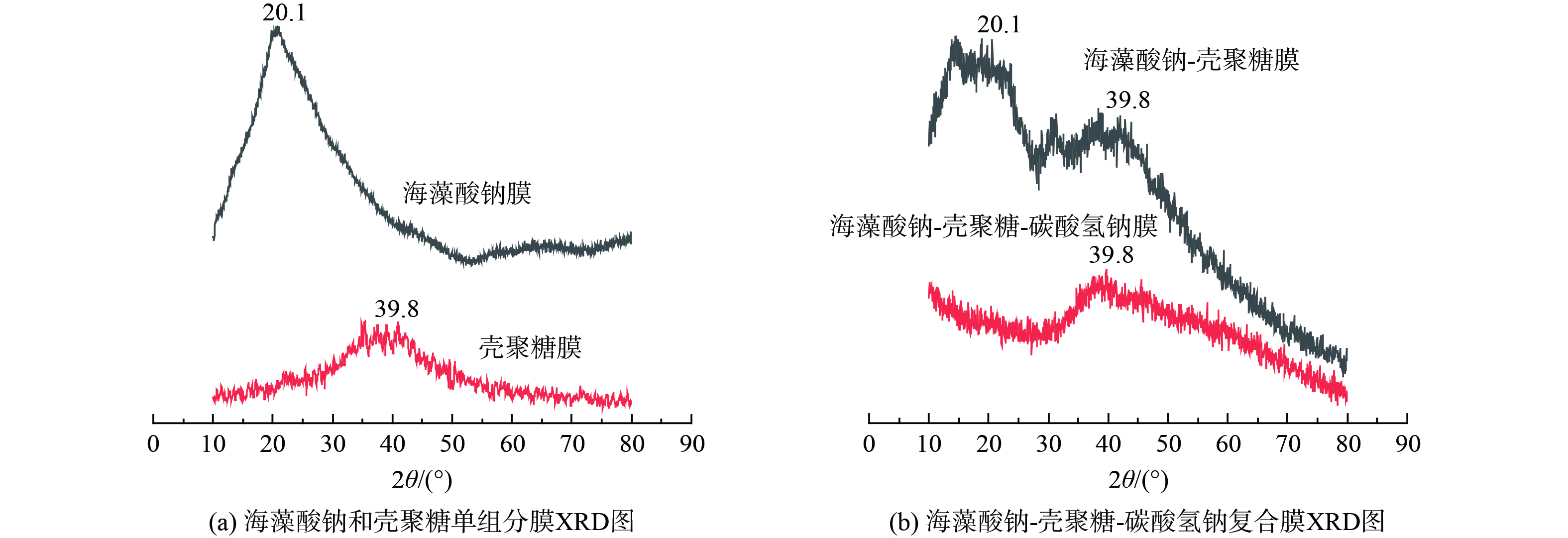
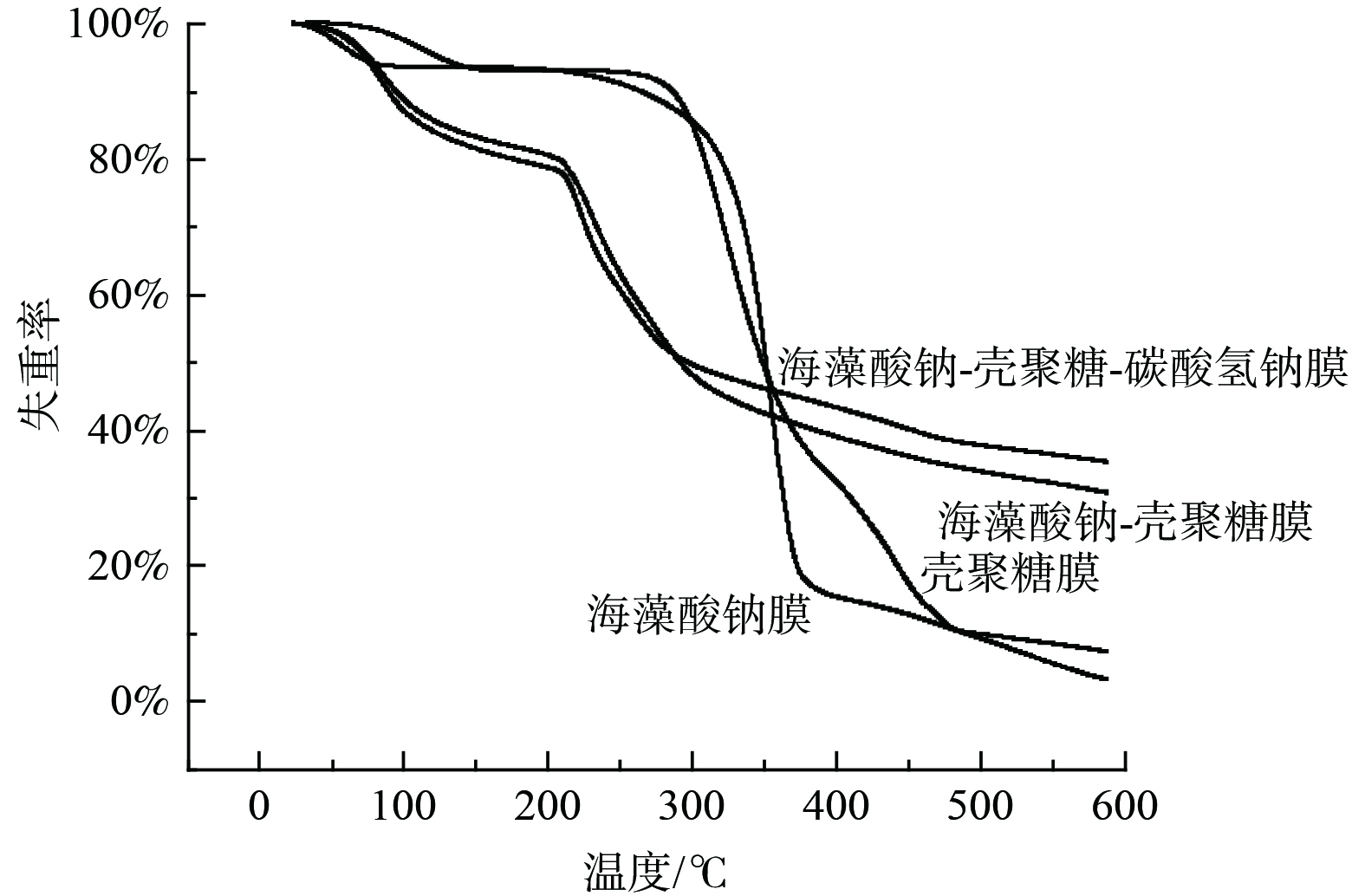
3) X射线衍射分析 (x-ray diffraction analysis,XRD) 。采用XRD图谱,分析海藻酸钠膜、壳聚糖膜及海藻酸钠-壳聚糖复合膜的衍射峰。从图6(a)可知,作为低结晶高分子有机化合物,壳聚糖为在2
$ \theta $ =19.7°和2$ \theta $ =39.8°处有较强的衍射峰,而海藻酸钠在2$ \theta $ =20.1°处有较强的衍射峰。如图6(b)所示,海藻酸钠-壳聚糖二元复合膜在2$ \theta $ =39.8°和2$ \theta $ =20.1°均出现较强衍射峰,即海藻酸钠和壳聚糖衍射峰的简单叠加,可证明两种组织直接混合后,没有形成新的物质[32]。但添加碳酸氢钠后,海藻酸钠在2$ \theta $ =20.1°处衍射图谱的强峰逐渐消失,说明壳聚糖与海藻酸钠进行某种程度相容,产生氢键,影响了混合物的晶形结构,进而说明添加碳酸氢钠提升了海藻酸钠-壳聚糖-碳酸氢钠复合膜的相容性。4) 热重分析 (thermal gravity analysis,TGA) 。使用TGA评估海藻酸钠-壳聚糖-碳酸氢钠复合膜的热稳定性及热降解行为。如图7所示,壳聚糖的热失重主要分为两个阶段,第一阶段从室温到100 ℃,对应于水分蒸发阶段;第二个阶段再250~475 ℃,对应于主链热解阶段,分别为水分蒸发和主链热解。根据键能大小的断裂顺序,首先C-N键,其次C-C键,最后C-O键[28]。海藻酸钠热失重主要分为三个阶段:室温到100 ℃为水分蒸发阶段;100~375 ℃为糖苷键断裂阶段,分子链中的-OH脱去产生中间产物;375~575 ℃为碳化分解阶段,产物脱去羧基,碳化产生CO2,部分产物更高温时产生Na2O。海藻酸钠-壳聚糖复合膜的热失重仍分为三个阶段,热失重的主要阶段发生在175~300 ℃的糖苷键断裂阶段,与纯海藻酸钠膜的热失重相比,该阶段的起始温度变高,温度区间变窄,说明壳聚糖的氨基与海藻酸钠的羧基通过静电吸附作用,形成聚电解质。而形成的聚电解质膜与海藻酸钠单组分膜相比,结构更为紧密\热稳定性提高。在600 ℃时,壳聚糖膜分解率为93%,海藻酸钠膜分解率为97%,海藻酸钠-壳聚糖二元复合膜分解率为70%,海藻酸钠-壳聚糖-碳酸氢钠复合膜分解率为75%。说明海藻酸钠与壳聚糖混合后形成聚电解质复合物后,分子间静电作用力可显著提高单组分的热稳定性。这可能是因为添加碳酸氢钠的复合膜,分子间力增强,同时提升对溶液pH的缓冲能力,进而导致复合膜的热稳定性增强。
-
通过对海藻酸钠、壳聚糖单组分膜和海藻酸钠-壳聚糖-碳酸氢钠复合膜的抗张强度、断裂伸长率、水溶性、水蒸气透过系数进行综合性的机械性能表征 (如表1) ,从而确定薄膜的稳定性。抗张强度反映了材料不断裂条件下能承受的最大拉伸应力,是评估复合膜机械强度的重要指标。根据抗张强度的大小,判断复合膜的机械稳定性[33]。断裂伸长率主要用于评估复合膜韧性和延展性[34]。水溶性代表了复合膜与水的相容性,可影响复合膜的湿润性和涂覆性能[35]。水蒸气透过系数主要衡量复合膜对水蒸气的透过能力,与复合膜的阻隔性能有关[36]。
壳聚糖为亲水性物质,溶解时间仅为35 min,水蒸气透过系数最大。单组分海藻酸钠薄膜机械性能良好,断裂伸长率和抗张强度分别可达12.52%、43.51 MPa。而海藻酸钠-壳聚糖二元复合膜后,在壳聚糖加入后,溶解时间增加,水蒸气透过系数变小。因而与纯海藻酸钠膜相比,代表机械性能的抗张强度变大,断裂伸长率变小。同时,添加碳酸氢钠后海藻酸钠-壳聚糖-碳酸氢钠复合膜,组分之间通过静电作用形成聚电解质,抑制复合膜的溶解性和水蒸气透过系数,而且两组分相容性的增加可进一步形成致密网状结构,提高其机械性能。
-
1) 复合膜性能优化添加剂。丙三醇为三元醇,具有三个羟基,能打断聚合物链间的相互作用,提高材料的柔韧性,降低玻璃化温度,促进复合膜的柔软性和韧性提高,因而被广泛应用于增塑剂[37]。吐温80是一种非离子表面活性剂,具有疏水和亲水两部分,可改善复合膜的润湿性,增强与其他物质黏附性,分散其他添加剂,同时提高复合膜的涂覆性和黏附性,使其在多种应用中更具有竞争力[38]。肉桂醛为有机化合物,具有特殊的芳香气味,具有杀菌和驱蚊蝇、掩盖不良气味的作用,可为复合膜提供一种自然的防腐和驱蚊方法,增强其在特定应用中的吸引力[39]。茶树精油为挥发性的植物油,包含多种有机化合物,能够为复合膜提供一种天然的芳香气味,提升复合膜的感官特性,使其更受消费者欢迎[40]。为此,借鉴工程除臭剂成分及医药喷膜组分,选择质量分数为1.5%的丙三醇为增塑剂,1.0%吐温80为表面活性剂、2.0%的肉桂醛为防蝇除臭剂选择,0.5%的茶树精油为香料添加剂,对海藻酸钠-壳聚糖-碳酸氢钠复合膜进行性能优化。
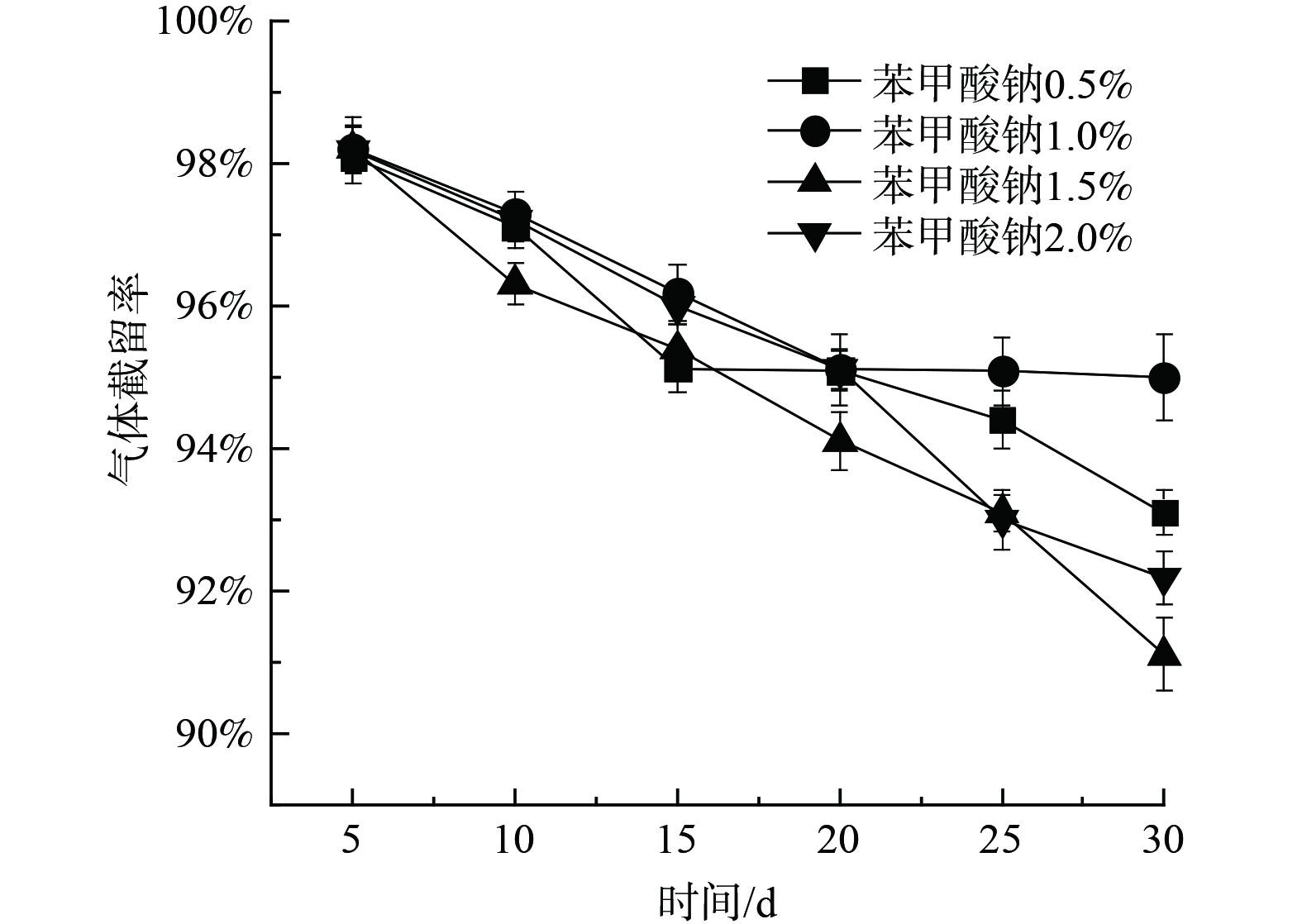
2) 抗菌防腐剂。苯甲酸钠又称安息香酸钠,及其盐类是广谱抗微生物试剂。苯甲酸钠抑菌性能主要有两方面[41],一方面自身亲油性促使其进入细胞体内,抑制细菌对氨基酸等物质的吸收,另一方面可与细菌细胞中呼吸酶反应,抑制细胞的呼吸作用,两者同时作用起到抑菌防腐效果[42]。同时,苯甲酸钠具有对许多酵母和霉菌的抑制作用,被添加到复合膜中时,可为复合膜提供内在的防腐保护。因此,为保证工程运输需求,选取苯甲酸钠作为防腐剂,如图8所示,经实验验证在30 d保质期内,1.0%的苯甲酸钠可提供最佳的防腐保质效果。经过优化后的海藻酸钠-壳聚糖-碳酸氢钠复合膜在中途转运30 min内对H2S和NH3气体截留率仍可保持在95%以上,完全满足工程项目要求。
-
1) 海藻酸钠、壳聚糖作为高分子成膜基材,添加碳酸氢钠作为pH调节物质,制备了海藻酸钠-壳聚糖-碳酸氢钠复合膜,并对垃圾填埋场的H2S和NH3的气体截留效率进行研究。喷膜溶液的各组份的最佳配方为:膜基材海藻酸钠与壳聚糖质量分数比例8∶2,化学除臭剂碳酸氢钠1.0%,该喷膜对H2S和NH3气体截留率在30 min内均可保证在95%以上,添加化学除臭剂NaHCO3后,制成的三元复合膜相容性和稳定性明显提升;相比于海藻酸钠、壳聚糖单组分膜,海藻酸钠-壳聚糖-碳酸氢钠复合膜的抗张强度变大,断裂伸长率变小,机械性能显著提高,更适用于实际应用。
2) 海藻酸钠-壳聚糖- NaHCO3三元复合膜中添加1.5%增塑剂丙三醇、1.0%表面活性剂吐温80、2.0%肉桂醛防蝇杀虫剂、0.5%茶树精油香料、1.0%苯甲酸钠为防腐剂时,制备的海藻酸钠-壳聚糖-碳酸氢钠复合膜适用于实际工程应用。
海藻酸钠-壳聚糖-碳酸氢钠复合膜优化制备及性能表征
Film preparation and performance of sodium alginate-chitosan-sodium bicarbonate membrane
-
摘要: 填埋场垃圾在挖掘和运输过程中常释放大量恶臭气体,持续时间长、影响范围广,其中硫化氢 (H2S) 和氨气 (NH3) 两种气体刺激性较大,产生较为严重的负面影响。开发了适用于垃圾填埋场H2S和NH3阻隔的喷涂薄膜,配方中选择海藻酸钠、壳聚糖作为高分子成膜基材,添加化学除臭剂碳酸氢钠制备薄膜,并添加增塑剂丙三醇、表面活性剂吐温80、防蝇除臭剂肉桂醛、香料添加剂茶树精油、防腐苯甲酸钠剂,对海藻酸钠-壳聚糖-碳酸氢钠复合膜进行性能优化。研究发现,质量分数为2.0%的海藻酸钠与壳聚糖配比为8∶2,碳酸氢钠质量分数1.0%、甘油1.5%、1.0%表面活性剂吐温80、2.0%肉桂醛、0.5%茶树精油香料、苯甲酸钠1.0%,多种成份复配制制备的复合膜对H2S和NH3的气体截留率 (质量浓度为70 mg∙m−3) 在30 min均可达95%。水溶液中多糖海藻酸钠带负电荷,壳聚糖带正电荷,两者能够发生交联形成海藻酸钠-壳聚糖聚电解质复合凝胶,添加化学除臭剂、增塑剂、防腐剂等成分对复合膜进行优化,使其满足垃圾中途转运机械性能要求的,维持高效的气体阻隔性能,实现填埋场垃圾中途转运中恶臭气体的高效阻隔,满足存余垃圾资源化工程项目需求。Abstract: Landfill waste often releases a significant amount of foul-smelling gases during excavation and transportation processes. These gases are characterized by high production, long duration, and wide-ranging impact. Among these foul-smelling gases, hydrogen sulfide (H2S) and ammonia (NH3) are some of the most typical. In this paper, an environmentally friendly spray film formula with barrier functionality was developed. By selecting appropriate ratios and using sodium alginate with a negative charge and chitosan with a positive charge, an alginate-chitosan polyelectrolyte was formed through cross-linking. Chemical deodorants, plasticizers, preservatives, and other ingredients were added to optimize the composite membrane, allowing it to maintain its physical transport effects while exhibiting excellent gas barrier properties. The results showed that a mass fraction of 2.0% of sodium alginate and chitosan membrane substrate, with a mixing ratio of 8∶2, and the addition of 1.0% sodium bicarbonate as a chemical deodorant, 1.5% glycerol as a plasticizer, 1.0% surfactant Tween 80, along with a mass fraction of 2.0% cinnamaldehyde as a fly repellent and insecticide, 0.5% tea tree oil as a fragrance, and 1.0% sodium benzoate as a preservative to inhibit the transformation of sodium alginate during transport. The prepared sodium alginate-chitosan-sodium bicarbonate composite membrane could achieve a gas retention rate of over 95% for hydrogen sulfide(H2S) and ammonia(NH3) with a mass concentration of 70 mg·m−3 for 30 minutes. This meted the requirements of residual waste resource utilization engineering projects and effectively blocks foul-smelling gases during the mid-transfer of landfill waste.
-
Key words:
- deodorizing composite membrane /
- sodium alginate /
- chitosan /
- polyelectrolyte /
- gas retention rate
-

-
图 1 升流式实验反应装置示意图[16]
Figure 1. Schematic diagram of upstream experimental device
表 1 海藻酸钠-壳聚糖-碳酸氢钠复合膜及单组分膜物理表征
Table 1. Physical characterization of sodium alginate-chitosan-sodium bicarbonate composite membrane and single component membranes
组分 抗张强度/MPa 断裂伸长率/% 水蒸气透过系数/ (g·m·h−1·m2·Pa) 海藻酸钠 43.51±0.44 12.52±0.51 43.33±0.64 壳聚糖 52.70±0.21 4.04±0.35 62.10±0.79 海藻酸钠-壳聚糖 45.65±0.53 11.43±0.68 59.31±0.63 海藻酸钠-壳聚糖-碳酸氢钠 37.76±0.47 15.67±0.47 52.77±0.56 -
[1] 赵岩, 陆文静, 王洪涛, 等. 城市固体废物处理处置设施恶臭污染评估指标体系研究[J]. 中国环境科学, 2014, 34(7): 1804-1810. [2] 纪华. 垃圾填埋场恶臭气体产气机制及其动态变化研究[D]. 北京: 中国农业大学, 2004. [3] WILBER C, MURRAY C. Odor source evaluation[J]. BioCycle, 1990, 31(3): 68-72. [4] ALLEN M R, BRAITHWAITE A, HILLS C C. Trace organic compounds in landfill gas at seven U. K. waste disposal sites[J]. Environmental Science and Technology, 1997, 31(4): 1054-1061. doi: 10.1021/es9605634 [5] ZHANG X H, LIU, D H, JIN T Z, et al. Preparation and characterization of gellan gum-chitosan polyelectrolyte complex films with the incorporation of thyme essential oil nanoemulsion[J]. Food Hydrocolloids, 2021, 114: 106570. doi: 10.1016/j.foodhyd.2020.106570 [6] DELGADO J D, SCHLENOFF J B. Polyelectrolyte complex films from blends versus copolymers[J]. Macromolecules, 2019, 52(20): 7812-7820. doi: 10.1021/acs.macromol.9b01834 [7] SISWANTA D, FARIDA F A, ZUNAIM D, et al. Adsorption of HA (humic acid) using sulfuric acid-crosslinked chitosan/pectin polyelectrolyte complex film[J]. Journal of Physics: Conference Series, 2019, 1156(1): 012003. [8] 姜福青. 壳聚糖膜及其共混膜的制备和性能研究[D]. 上海: 东华大学, 2010. [9] 袁柳. 海藻酸钠基水凝胶的制备、性能研究及在组织修复中的应用[D]. 上海: 东华大学, 2018. [10] 袁毅桦. 基于壳聚糖与海藻酸钠的改性聚合物的制备结构与性能研究[D]. 广州: 华南理工大学, 2012. [11] 曾嵘. 壳聚糖/聚乙烯醇共混交联和亲和膜的制备及应用研究[D]. 武汉: 湖北大学, 2018. [12] ČALIJA B, SAVIĆ S, KRAJIŠNIK D, et al. pH‐sensitive polyelectrolyte films derived from submicron chitosan/Eudragitreg L 100‐55 complexes: physicochemical characterization and in vitro drug release[J]. Journal of Applied Polymer Science, 2015, 132(39): 42583. doi: 10.1002/app.42583 [13] LIU K, LIN X X, CHEN L H, et al. Preparation of microfibrillated cellulose/chitosan-benzalkonium chloride biocomposite for enhancing antibacterium and strength of sodium alginate films[J]. Journal of Agricultural and Food Chemistry, 2013, 61(26): 6562-6567. doi: 10.1021/jf4010065 [14] LI L, HAN Y P, YAN X, et al. H2S removal and bacterial structure along a full-scale biofilter bed packed with polyurethane foam in a landfill site[J]. Bioresource Technology, 2013, 147: 52-58. doi: 10.1016/j.biortech.2013.07.143 [15] RYBARCZYK P, SZULCZYŃSKI B, GĘBICKI J, et al. Treatment of malodorous air in biotrickling filters: A review[J]. Biochemical Engineering Journal, 2019, 141: 146-162. doi: 10.1016/j.bej.2018.10.014 [16] 王涵, 李季, 刘爱荣, 等. 普鲁兰多糖基恶臭气体阻隔喷膜的制备及性能[J]. 环境工程学报, 2023, 17(2): 617-624. doi: 10.12030/j.cjee.202211037 [17] 袁晓雨. 疏水/亲油膜的制备及其油水分离性能研究[D]. 天津: 天津工业大学, 2017. [18] 李东光. 小化工产品配方与制作[M]. 1版 北京: 化学工业出版社, 2012: 601-800. [19] SUN X Y, WANG J, DONG M N, et al. Food spoilage, bioactive food fresh-keeping films and functional edible coatings: Research status, existing problems and development trend[J]. Trends in Food Science & Technology, 2022, 119: 122-132. [20] 金顺子, 沈德言. 聚氯乙烯膜在玻璃化转变温度区域的傅里叶变换红外光谱研究[J]. 高分子学报, 1991(6): 667-671. [21] 姜良斌. 壳聚糖/海藻酸钠膜支架-骨髓间充质干细胞修复软骨缺损的研究[D]. 广州: 广州中医药大学, 2019. [22] JUNG J, DENG Z L, SIMONSEN J, et al. Development and preliminary field validation of water-resistant cellulose nanofiber based coatings with high surface adhesion and elasticity for reducing cherry rain-cracking[J]. Scientia Horticulturae, 2016, 200: 161-169. doi: 10.1016/j.scienta.2016.01.016 [23] 陈敬鑫, 杨明亮, 葛永红, 等. 海藻酸钠可食性膜及其食品保鲜应用的研究进展[J]. 渤海大学学报(自然科学版), 2021, 42(2): 102-110. [24] 程东东. 合成锂皂土-海藻酸钠复合屏障膜的制备及研究[D]. 上海: 安徽医科大学, 2021. [25] HOSSEINI S F, REZAEI M, ZANDI M, et al. Preparation and functional properties of fish gelatin-chitosan blend edible film[J]. Food Chemistry, 2013, 136(3-4): 1490-1495. doi: 10.1016/j.foodchem.2012.09.081 [26] 岳艺璇. 大蒜素皮克林乳液-海藻酸钠基抑菌包装膜的制备及抑菌性能研究[D]. 长春: 吉林大学, 2023. [27] 高美玲. 海洋多糖生物可降解膜的制备与应用研究[D]. 青岛: 中国海洋大学, 2011. [28] ZHANG R P, DING M T. Preparation propertie sodium alginatend characterization of the blend film of polyvinyl alcohol and chito sodium alginaten[J]. Functionional Materials, 2007, 38(12): 2004-2007. [29] XING L, MA Y, TAN H P. Alginate membrane dressing toughened by chitosan floccule to load antibacterial drugs for wound healing[J]. Polymer Testing, 2019, 79: 106039. doi: 10.1016/j.polymertesting.2019.106039 [30] CHEN Y, QIU H Y, DONG M H, et al. Preparation of hydroxylated lecithin complexed chitosan/sodium alginate composite membrane by microwave drying and its applications in infected burn wound treatment[J]. Carbohydrate Polymers, 2019, 206: 435-445. doi: 10.1016/j.carbpol.2018.10.068 [31] 王志亮. 壳聚糖-海藻酸钠聚电解质复合膜的制备及性能研究[D]. 北京: 北京化工大学, 2014. [32] 宋慧君. 明胶-壳聚糖基可生物降解膜的制备、结构与性能研究[D]. 郑州: 郑州大学, 2015. [33] 张群利, 崔琳琳, 高雪. 再生纤维素/壳聚糖/银纳米线抗菌复合膜的制备及性能[J]. 精细化工, 2022, 39(5): 892-897. [34] 钟婷, 普涵, 茹素梅, 等. 壳聚糖-生姜精油复合膜的优化制备[J]. 山东化工, 2022, 51(23): 46-50. doi: 10.3969/j.issn.1008-021X.2022.23.012 [35] 李秋莹, 徐瑾秀, 高明君, 等. 普鲁兰/壳聚糖/海藻酸钠双层膜的制备及表征[J]. 包装工程, 2020, 41(15): 96-102. [36] 章琪良. 水溶性壳聚糖合成及其海藻酸复合膜特性评价[D]. 杭州: 浙江工业大学, 2013. [37] NGUYEN T T, PHAN N H T, TRINH C D, et al. Glycerol‐plasticized chitosan film for the preservation of orange[J]. Journal of Food Safety, 2021, 42(1): 1-13. [38] LIU T, WANG J F, CHI F M, et al. Development and characterization of novel active chitosan films containing fennel and peppermint essential oils[J]. Coatings, 2020, 10(10): 936. doi: 10.3390/coatings10100936 [39] LIAN H, PENG Y, SHI J Y, et al. Effect of emulsifier hydropHilic-lipopHilic balance(HLB) on the release of thyme essential oil from chitosan films[J]. Food Hydrocolloids, 2019, 97: 105213. doi: 10.1016/j.foodhyd.2019.105213 [40] CHEN H L, HU X R, CHEN E M, et al. Preparation, characterization, and properties of chitosan films with cinnamaldehyde nanoemulsions[J]. Food Hydrocolloids, 2016, 61: 662-671. doi: 10.1016/j.foodhyd.2016.06.034 [41] 徐文峰. 苯甲酸钠对多糖共混膜吸湿性和抗菌性的影响研究[J]. 中国食品添加, 2020(3): 158-161. [42] 王思文, 巩江, 高昂, 等. 防腐剂苯甲酸钠的药理及毒理学研究[J]. 安徽农业科学, 2010(30): 16724+16846. -



 下载:
下载: