-
铅(Pb)是一种普遍存在且具有生理毒性和生物蓄积性的重金属[1],低浓度暴露也会对人体和生活环境造成永久性损害[2-3],被公认为最具毒性的金属之一[4]。铅离子主要来源于铅冶炼、电池制造、印刷和采矿等行业。根据地表水环境质量标准,Ⅴ类水中Pb2+的含量为不高于0.1 mg·L−1[5]。目前,重金属检测方法包括原子光谱法、色谱法、电化学法、表面增强拉曼光谱法等[6-8]。这些方法灵敏度高、重现性好,但存在预处理复杂、耗时、设备昂贵等缺点[9]。与之相比,荧光检测法具有速度快、操作简单、价格低廉等优点[10],适用于偏远分散水源的检测以及突发环境事件的应急检测。因此,开发一种便捷原位检测铅离子的方法势在必行。
金属-有机框架(MOFs)是一种新型的微孔材料,它通过金属离子或金属簇与有机配体之间的配位进行组装,在吸附和分离[11-12]、催化[13]、光电及电化学[14]等方面被广泛使用。MOFs不仅具有表面积大、可结合位点多、设计性强等特点[15],而且具有良好的荧光性能。已有研究[15-16]表明,基于MOFs的荧光传感器可以与重金属离子选择性结合,与Fe3+、Cu2+、Pb2+、Cr2O72+和CrO42+等结合后具有敏感的荧光淬灭响应。近年来,有研究者利用这种效应,开展了铅离子荧光法检测相关研究。LIU等[17]通过合成碱土金属有机框架[Ca2(µ10-L)(EtOH)]n,利用荧光淬灭机制检测Pb2+,检测限达69.4 µmol·L−1。LI等[18]合成的基于氟烯基的镧系元素金属-有机框架([Eu2(FDC)3DMA(H2O)3]·DMA·4.5H2O),作为荧光探针可以快速选择性检测水相中的铅离子,检测限为8.22 µmol·L−1。现已报道的荧光探针存在灵敏度较低的问题,故制备灵敏高效的荧光探针具有十分重要的现实意义。
碳点(CDs)是一种新型的量子点,大量研究[19-21]表明,CDs@MOFs复合材料是可调可设计的荧光探针,对各种目标分析物具有高灵敏度和选择性,是一种很有前途的荧光材料。HAO等[19]通过合成花球状CDs@Eu-DPA MOFs,开发了一种检测Cu2+的荧光探针,CDs发射的荧光可以降低激发源不稳定性等系统误差,从而提高荧光探针的精度。XU等[20]设计了一种CD@Eu3+-MOF-253复合材料用于检测Hg2+,并发现Hg2+通过与CDs的表面官能团协调,可以显著淬灭CDs的荧光,而不影响Eu-MOF的荧光强度。到目前为止,已有许多关于MOFs的荧光探针研究[19-21],然而,CDs@MOFs荧光材料用于重金属铅离子检测的研究鲜有报道。
本研究通过碳点(N,S,I-CDs)修饰MIL-101-NH2, 制备了CDs@MIL-101-NH2复合材料,通过TEM、XRD、FT-IR、XPS等对材料进行表征,研究碳点修饰对MOFs结构的影响以及材料浓度、pH值、时间对CDs@MOFs复合材料荧光强度的影响,在将复合材料作为荧光探针用于水中Pb2+的荧光检测过程中,考察其检测范围、检出限以及离子选择性等,探讨CDs@MIL-101-NH2复合材料发生荧光淬灭的可能机理,以期为荧光法检测重金属离子的MOF材料设计提供参考。
-
实验所用试剂均为分析纯。六水合氯化铁(FeCl3·6H2O)和乙二胺购自国药集团;N,N-二甲基甲酰胺和无水乙醇购自麦克林有限公司;2-氨基对苯二甲酸购自毕得医药有限公司;三聚硫氰酸(C3H3N3S3)购自贤鼎生物有限公司;碘酸钾(KIO3)购自迈瑞尔有限公司;实验用水为去离子水,电阻率为18.2 MΩ·cm−1。
-
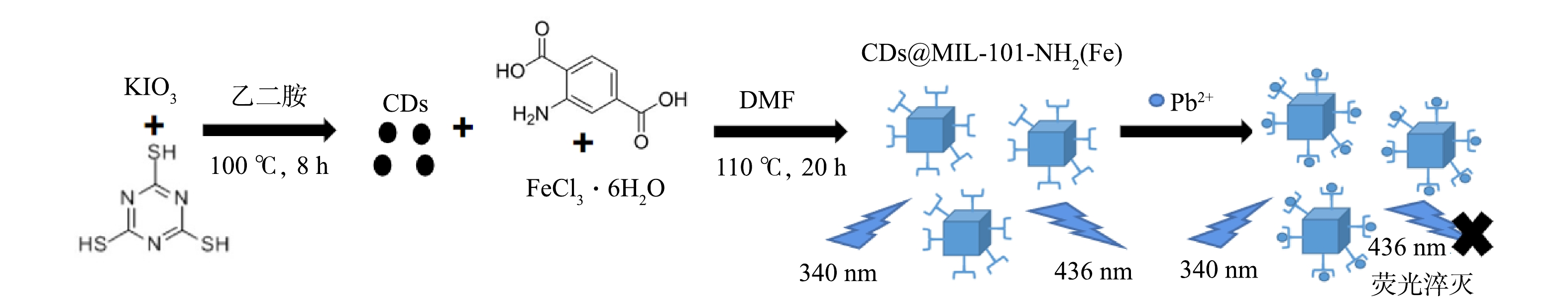
在碳点(N,S,I-CDs)制备过程中,室温下,将250 mg碘酸钾和25 mg三聚硫氰酸混合于25 mL去离子水中,加入1.5 mL乙二胺,超声振荡至完全溶解。将混合液置于50 mL聚四氟乙烯反应釜中,设定温度为180 °C,反应8 h,反应结束后,取出,自然冷却至室温。反应后的混合液经0.22 μm亲水PTFE滤膜过滤,取澄清溶液于4 °C保存待用。
采用水热法,在室温下,将0.67 g FeCl3·6H2O(5 mmol)和0.45 g NH2-H2BDC(2.5 mmol)分散于30 mL于DMF中,超声10 min,待完全溶解后,再加入体积为200 μL的CDs溶液。将混合液转移至50 mL的聚四氟乙烯反应釜,置于110 °C的烘箱中,反应20 h。反应结束后,自然冷至室温,离心出产物,用乙醇反复离心洗涤3次以上去除多余的杂质,于80 °C真空条件下烘干,得到CDs@MIL-101-NH2(Fe)复合材料。
-
针对实验室制备的CDs@MIL-101-NH2(Fe)材料,采用材料型场发射透射电镜(Talos F200X G2,USA)表征样品的形貌;采用MAXima 7000型X射线衍射分析仪(Shimadzu,Japan)表征材料的晶体结构;采用Nicolet 670光谱仪(Thermo Fisher,USA)记录傅里叶变换红外光谱并分析有机配体官能团的存在形态;采用X射线光电子能谱仪(Kratos,Japan)分析材料的元素及价态;采用Autosorb IQ3分析仪(Quantachrome,USA)测定材料的比表面积、介孔孔径分布;通过Brunauer-Emmett-Teller (BET)法和Barrett-Joyner-Halenda (BJH)法分别计算比表面积和孔径。
-
在室温下,采用荧光光谱仪FLS1000 (Edinburgh,UK)进行测量;使用450 W的氙灯和光电倍增管(PMT900)作为测试光源。待测液的容器为石英比色皿(1 cm×1 cm),激发波长和狭缝宽度的选取须同时考虑样品特征与仪器最大接受荧光强度。将1.0 g的CDs@MIL-101-NH2(Fe)粉末溶于1 000 mL的去离子水中,超声10 min,使其完全分散均匀,得到初始质量浓度为1 000 mg·L−1的悬浮液荧光探针。然后将其质量浓度分别稀释至5、10、25、50、100、200、300、500 mg·L−1,测量上述质量浓度材料的荧光强度。制备最佳质量浓度的CDs@MOFs溶液,然后利用1 mol ·L−1的硫酸和氢氧化钠溶液将其pH分别调至5~13,测量上述pH下的CDs@MIL-101-NH2荧光探针的荧光强度。在最佳浓度和最佳pH值下,将响应时间设置为1、20、60、90、120、150、180、240和300 min,检测各个响应时间下溶液的荧光强度。
检测不同Pb2+浓度(0、10、20、40、60、80、100、120、150、180、200、240、280、320、360、400、450、500 μmol·L−1) CDs@MIL-101-NH2(Fe)溶液的荧光强度。CDs@MOFs荧光探针效率的定量计算采用Stern-Volmer计算方法[21] (式(1))。
式中:I0和I分别为CDs@MOFs加入被分析物前后的荧光强度;c为被分析物的浓度;Ksv为Stern-Volmer常数,Ksv值越高,说明荧光探针的效率越高。
在CDs@MIL-101-NH2(Fe)溶液溶液中,加入阴离子Cl−、CO32−、PO43−、SO42−以及阳离子K+、Mg2+、Ba2+、Fe3+、Co2+、Ni2+、Cu2+、Cd2+、Cr3+(离子浓度= 0.5 mmol·L−1),混合均匀并检测CDs@MOFs溶液的荧光强度。
-
利用自来水和湖水来验证CDs@MIL-101-NH2(Fe)荧光探针在水基质中检测铅离子的实用性。湖水水样取自思源湖(上海交通大学),自来水水样取自实验室(上海交通大学)。水样均通过0.45 μm孔径的滤膜过滤,去除悬浮颗粒物,分别加入Pb2+标准溶液,制备出不同浓度的加标水样。将1 mg CDs@MIL-101-NH2分散于100 mL加标水样中,孵育90 min后,测其荧光强度。
-
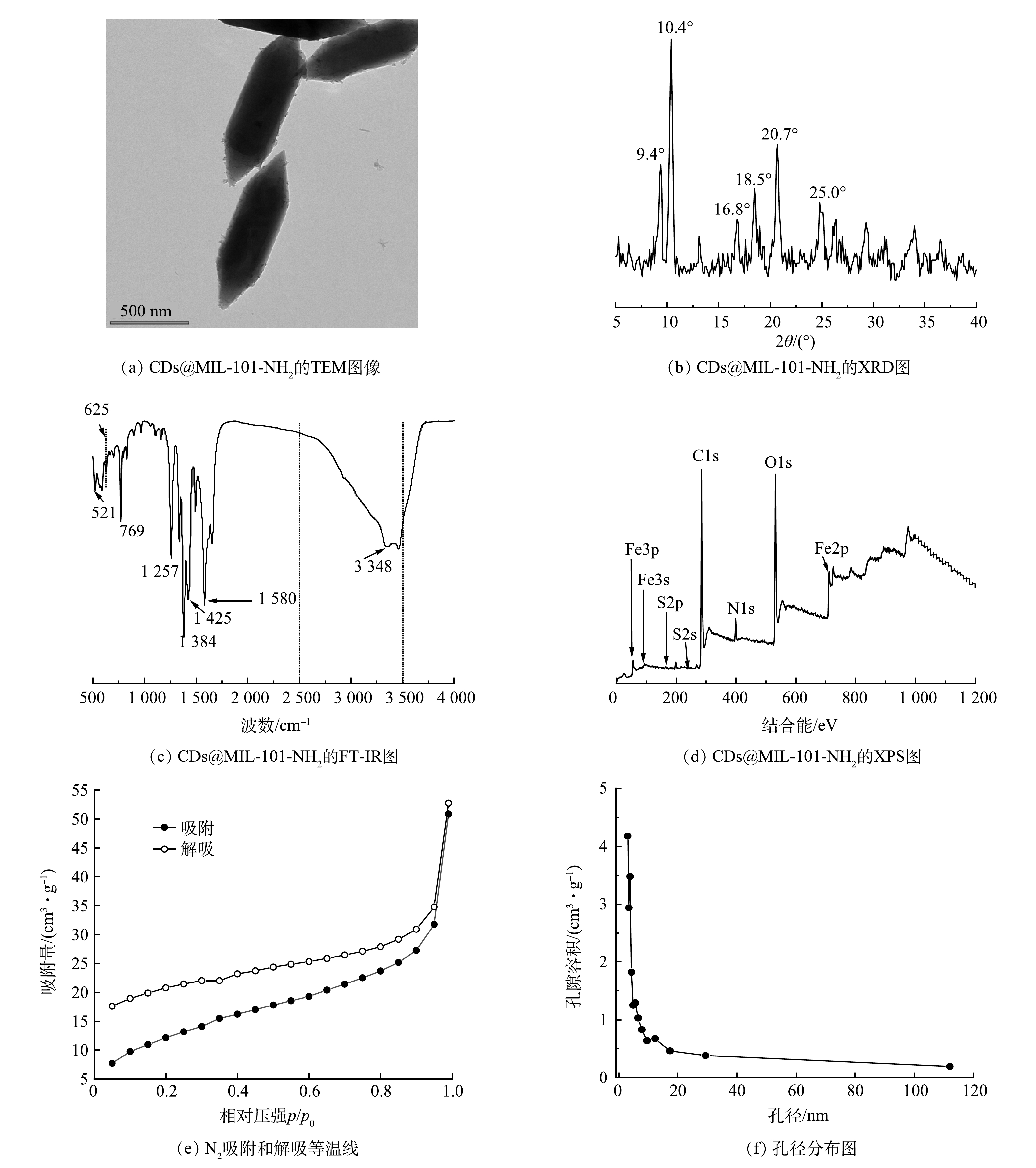
通过场发射透镜研究CDs@MIL-101-NH2(Fe)的微观形貌。如图1(a)所示,材料为纺锤形晶体,与已有研究[22]中的MIL-101-NH2晶体形状一致。显然,MIL-101-NH2在引入碳点后,晶体形貌仍呈纺锤形,说明碳点修饰不改变晶体形貌。XRD对样品的组成和晶体形态表征结果如图1(b)所示。可以看出:CDs@MIL-101-NH2的XRD谱图在9.4°、10.4°、16.8°、18.5°、20.7°和25.0°处有明显的特征峰;10.4°和16.8°处的特征峰与MIL-101-NH2(Fe)的特征峰[22-23]符合,在25.0°处的特征峰与碳点(N,S,I-CDs)的特征峰[24]相符。这说明CDs@MIL-101-NH2复合材料的构建是成功的,且碳点(N,S,I-CDs)的引入未对晶体MIL-101-NH2结构造成很大影响。
为研究CDs@MIL-101-NH2(Fe)的结构,采用傅里叶变换红外光谱仪分析有机配体官能团的存在形态,红外光谱如图1(c)所示。吸附谱带在625 cm−1处分配给Fe—O键[23],1 400~1 600 cm−1处对应芳香环上的C=C伸缩振动吸收峰,1 384 cm−1处的强波段对应C—C键、—COO—的反对称伸缩振动峰和对称伸缩振动峰,说明CDs@MIL-101-NH2中存在二羧酸结构[25]。769 cm−1和3 348 cm−1处的吸收峰分别是N—H键的摇摆带和C—N键的拉伸带[24],说明氨基已成功修饰于框架上。这些吸收振动峰与已有研究[24]中报道的MIL-101-NH2的特征峰相似。复合材料CDs@MIL-101-NH2中还出现了一些新的峰,其中包括在2 500~3 500 cm−1处属于O—H键的伸缩振动峰[26],在1 656 cm−1处对应于C=O键的伸缩振动吸收峰以及1 257 cm−1、521 cm−1对应的C—S键、C—I键的伸缩振动峰[27]。这些新的特征峰进一步证实了碳点(N,S,I-CDs)在复合材料中的存在。本研究针对CDs@MIL-101-NH2进行了XPS分析,结果如图1(d)所示。CDs@MIL-101-NH2探测到的元素有C、N、O、Fe、S,碳点修饰的材料探测到的S元素进一步说明碳点(N,S,I-CDs)修饰过程的成功。I元素由于含量少而未被检测到,表明碳点在复合材料CDs@MIL-101-NH2中的占比较少。
CDs@MIL-101-NH2(Fe)的N2吸附-解吸等温线如图1(e)所示。可以看出,曲线形状符合IV型等温线。CDs@MIL-101-NH2材料的孔径分布如图1(f)所示,其比表面积为45.374 m2·g−1,孔径为3.054 nm,这表明CDs@MIL-101-NH2具有介孔结构。
-
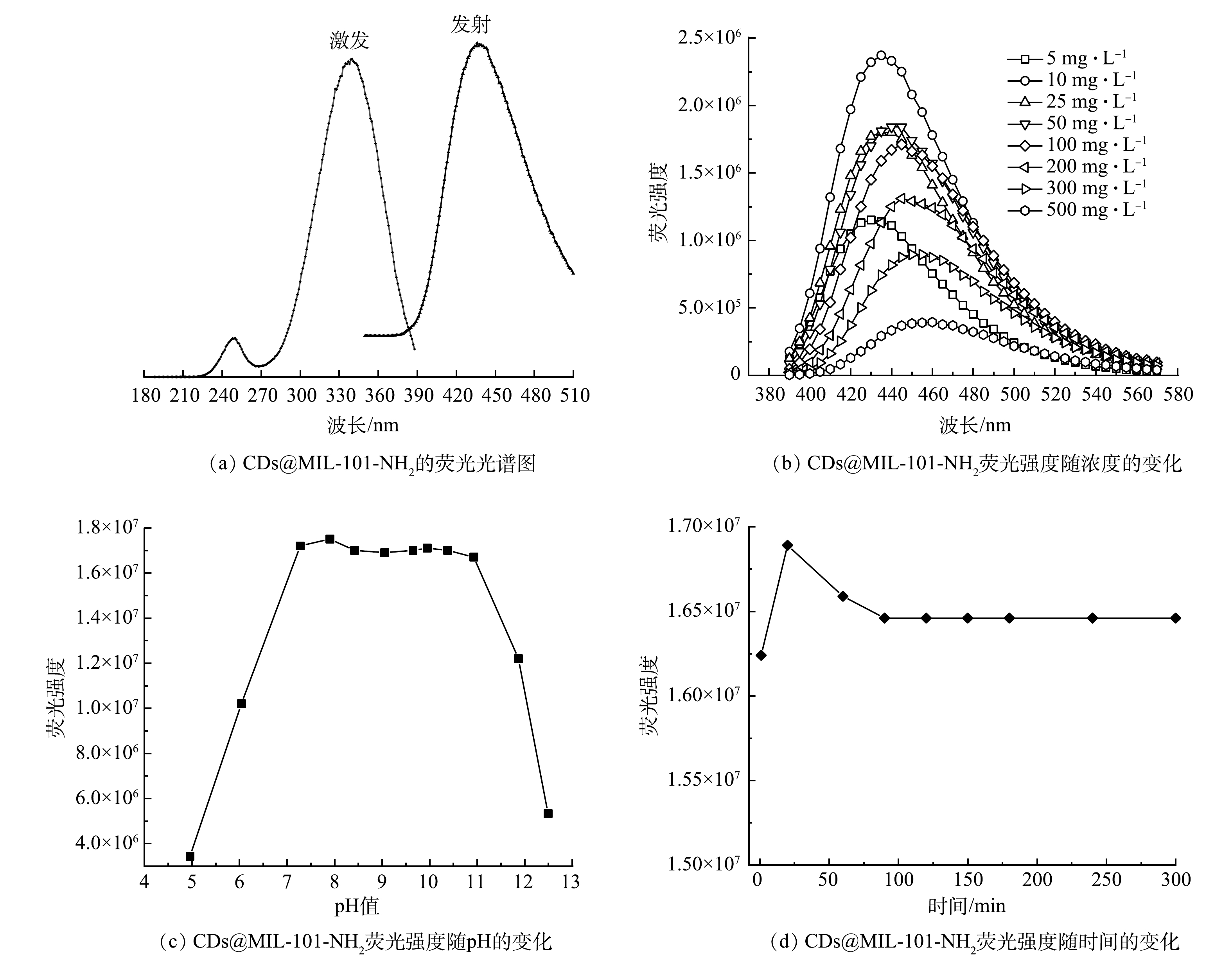
图2(a)为CDs@MIL-101-NH2(Fe)的荧光激发和发射光谱图。在检测过程中,使用荧光光谱仪FLS1000在室温下进行测量,使用 450 W的氙灯和光电倍增管(PMT900)作为测试光源,激发狭缝宽度和发射狭缝宽度均为1.5 nm。确定CDs@MIL-101-NH2材料的最佳激发波长为340 nm,最佳发射波长为436 nm。
发光CDs@MOFs的质量浓度和pH对荧光性质有重要影响[26,28]。如图2(b)所示,随着CDs@MIL-101-NH2(Fe)质量浓度的降低,荧光强度逐渐增大。当质量浓度达到10 mg·L−1时,荧光强度达到最大值。随着材料质量浓度的升高,荧光强度也呈现下降趋势,这可能与CDs@MIL-101-NH2的自淬灭行为有关。为达到最佳的荧光强度,以上实验确定材料的最佳质量浓度为10 mg·L−1。如图2(c)所示,MOFs材料荧光强度会受到pH的影响。pH值在5~7时,复合材料的荧光强度显著增大;pH为7~11时,荧光强度的变化不大;pH>11时,荧光强度锐减。由此可见,材料对酸性环境的变化十分敏感,在碱性环境中则相对稳定。这可能是由于CDs@MIL-101-NH2表面的氨基在酸性环境中容易质子化,从而对荧光信号产生了不良影响,在碱性环境中则不受影响。为获得最佳荧光强度,材料溶液的pH需要控制为7。
响应时间会影响荧光强度的变化。如图2(d)所示,CDs@MIL-101-NH2(Fe)的响应时间大于90 min时,其荧光强度没有显著变化,趋于稳定状态。因此,90 min为CDs@MIL-101-NH2材料的最佳响应时间。
-
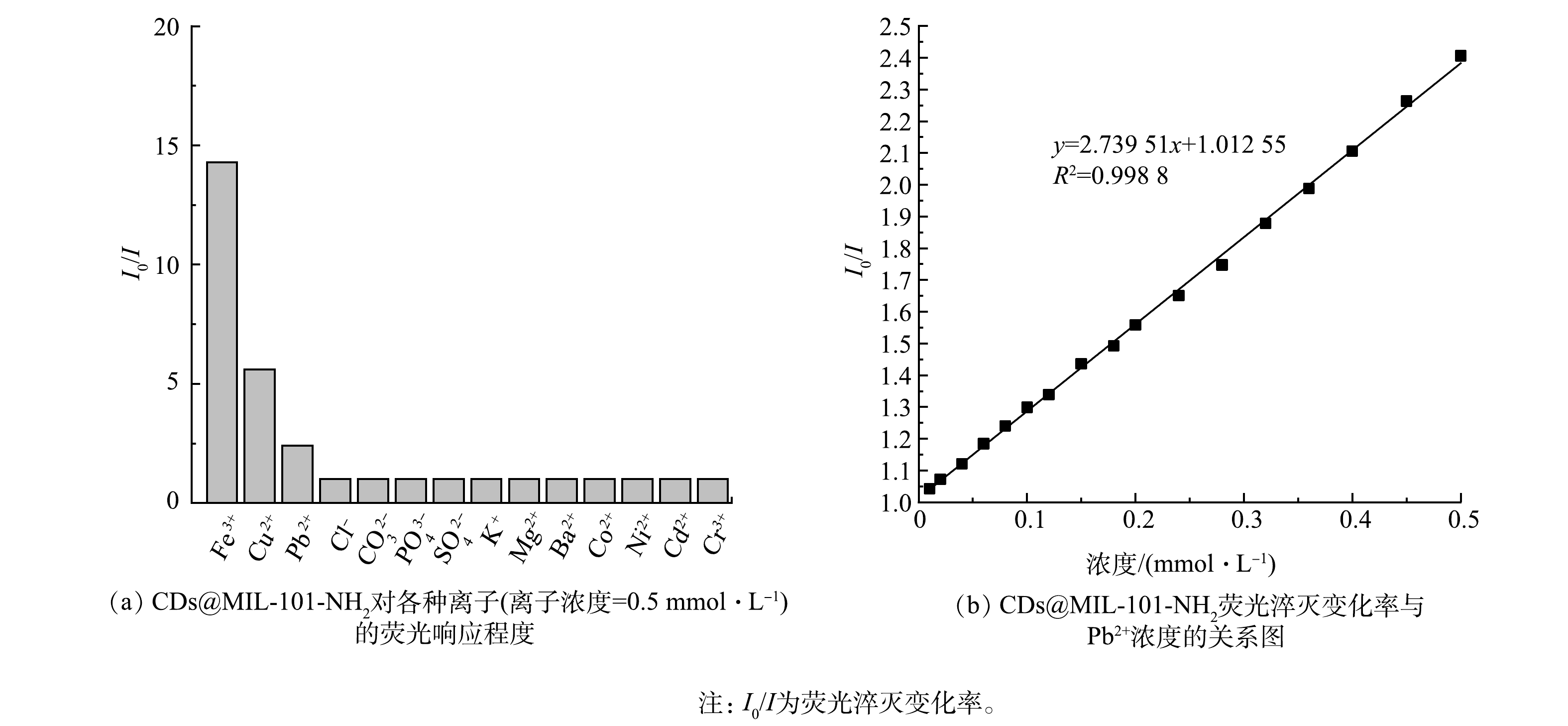
为探讨CDs@MIL-101-NH2(Fe)作为荧光探针对金属离子的荧光响应的应用前景,研究了不同阴阳离子对CDs@MIL-101-NH2荧光强度的影响。由图3(a)可以看出,阴离子Cl−、CO32−、PO43−、SO42−加入前后对复合材料荧光强度几乎没有影响(I0/I=1),而不同的金属离子对复合材料的荧光强度变化有不同的影响,如Fe3+、Cu2+和Pb2+与CDs@MIL-101-NH2(Fe)的相互作用可以显著淬灭荧光。上述结果表明,CDs@MIL-101-NH2在水介质中具有较高的选择性和灵敏度,用来检测水体中Pb2+的荧光探针会受到Fe3+和Cu2+的干扰。实验结果表明,过量的Na+和F−对CDs@MIL-101-NH2溶液的荧光强度没有影响,故可采用NaF溶液消除Fe3+和Cu2+的干扰。对照实验表明,含100 μmol·L−1 Pb2+的CDs@MIL-101-NH2溶液在加入过量NaF后,荧光强度没有显著变化,变化率为2%~3%。同时,含100 μmol·L−1 Fe3+、100 μmol·L−1 Cu2+、100 μmol·L−1 Pb2+和过量NaF的CDs@MIL-101-NH2溶液产生的荧光淬灭,是含100 μmol·L−1 Pb2+和过量NaF的CDs@MIL-101-NH2溶液产生的荧光淬灭的98%~102%。实验结果证明,当NaF消除了Fe3+和Cu2+的干扰后,Pb2+的检测不受影响。因此,CDs@MIL-101-NH2对水中的Pb(Ⅱ)有较好的选择性,对实际水体中Pb(Ⅱ) 的检测具有较高的可行性。
本研究进一步探讨了0~500 µmol·L−1的Pb2+浓度对CDs@MIL-101-NH2(Fe)荧光强度的影响,结果如图3(b)所示。采用上述方法制备的复合材料溶液,荧光淬灭效率由式(1)计算得出。CDs@MIL-101-NH2溶液I0/I与Pb2+质量浓度之间可决系数R2为0.998 8,Ksv为2 739.5 mol·L−1。这表明复合材料作为荧光探针检测水中的铅离子有较好的灵敏度。Pb2+的检出限为1.22 µmol·L−1 (3σ水平),检测区间为1.22~500 µmol·L−1。
-
为探究碳点修饰对MOF材料检测Pb2+的性能影响,比较了未经碳点修饰和碳点修饰的2种材料检测重金属Pb2+的效果差异。碳点(N,S,I-CDs)修饰获得的CDs@MIL-101-NH2(Fe)复合材料与未经碳点修饰的材料相比,检测区间由5.72~100 µmol·L−1变为1.22~500 µmol·L−1。可决系数R2从0.974 2提高至0.998 8,Pb2+的检出限从5.72 µmol·L−1降至1.22 µmol·L−1,Ksv从831.2 mol·L−1增至2 739.5 mol·L−1。由此可证明碳点的修饰明显地提高了MIL-101-NH2对Pb2+的荧光淬灭传感效率。与其他报道结果(表1)相比,本研究所制备的复合材料用于荧光法检测铅离子具有更大的检测区间(1.22~500 µmol·L−1)和优异的荧光传感效率(Ksv)。这是因为,与传统的MOFs材料比较,碳点修饰可以弥补MOFs材料自身存在的一些缺陷,增强复合材料的光学性能。
本研究通过CDs@MIL-101-NH2(Fe)的表征分析,探讨了CDs@MIL-101-NH2荧光淬灭的可能机制。如图2(c)所示,随着pH的升高,复合材料的荧光强度先增大后减小,pH为7~11时,荧光强度的变化不大,且氨基为MIL-101-NH2荧光产生的关键[24],可推测氨基在CDs@MIL-101-NH2荧光探针检测铅离子的荧光淬灭现象中起着重要作用。WU等[29]在制备NH2-UiO-66荧光探针用于铜离子的荧光检测研究中,发现铜离子具有顺磁性,d轨道对氨基有较高的亲和力,荧光淬灭的发生可能与Cu2+-NH2配合物的形成有关。已有研究者[24]在基于MIL-101-NH2材料荧光检测金属离子的研究中,提出氨基与金属离子的之间的螯合作用可以诱导主-客体电子转移,从而导致荧光淬灭的发生。由此可以看出,碳点的引入没有改变MIL-101-NH2的晶相,且CDs@MIL-101-NH2复合材料发生荧光淬灭的主要原因为氨基与铅离子的作用(图4)。
已有研究[19,30]表明,荧光碳点的修饰增强了铅离子与激发态π电子的接触。荧光碳点的尺寸通常远小于MOFs材料,本研究所制备的MIL-101-NH2晶体粒径为800 nm~1 µm,制备的荧光碳点的粒径为4~5 nm。样品形貌与结构表征结果表明,荧光碳点的加入并未改变配位网络的结构。因此,推测荧光碳点的存在形式是分布于配位网络之间的极富电子的纳米结构。在铅离子荧光响应过程中,碳点的富电子基团具有远强于氨基的供电子能力,能够有效吸引铅离子的空轨道,使铅离子能够为附近的π*电子供弛豫途径[31],因此,荧光碳点的加入未改变MOFs配位网络本身的结构,但有效提高了铅离子的荧光响应效率。
根据靶受体的不同,CDs@MOFs复合材料的传感途径一般可分为3类:1) CDs为受体; 2) MOFs为受体;3)CDs和MOFs为共同受体[32]。在本研究中,MIL-101-NH2作为受体,Pb2+可以通过与配体官能团氨基的相互作用改变荧光探针的荧光强度。因此,CDs和MOFs的荧光可以相互对照,从而提高了荧光检测的精确度。
-
在实验过程中,配置不同浓度梯度的铅离子浓度标准液(0、10、20、40、60、80、100、120、150、180、200 μmol·L−1),获得了CDs@MIL-101-NH2(Fe)荧光探针结合后混合液的荧光强度。以铅离子的质量浓度为横坐标,荧光淬灭变化率为纵坐标,绘制标准曲线。基于标准曲线,根据实际样品中的荧光淬灭率,计算得出实际样品的铅离子质量浓度。实际样品主要为自来水和思源湖湖水,在进行实验前,对实际样品进行预处理过滤并对添加铅离子的自来水和思源湖湖水进行加标回收实验,结果如表2所示。由表2可以看出,加标回收率分别为98.74%~106.16%和97.24%~103.63%,相对标准偏差RSD<4%(n=3),检测可靠性和准确性较高。这说明基于CDs@MIL-101-NH2复合材料的荧光检测法应用于水体中的铅离子检测具有可行性。
-
1) CDs@MIL-101-NH2(Fe)复合材料在质量浓度为10 mg·L−1,pH为7,反应时间为90 min的条件下,荧光强度最佳。
2)碳点(N,S,I-CDs)修饰提高了MIL-101-NH2(Fe)检测Pb2+的性能,检测区间由5.72~100 µmol·L−1变为1.22~500 µmol·L−1,可决系数R2从0.974 2提至0.998 8,Pb2+的检出限从5.72 µmol·L−1降至1.22 µmol·L−1,Ksv从831.2 mol·L−1增至2 739.5 mol·L−1。
3) Pb2+的荧光淬灭效应可归因于CDs@MIL-101-NH2(Fe)复合材料上的氨基与铅离子的相互作用。荧光碳点(N,S,I-CDs)的加入不改变MIL-101-NH2(Fe)配位网络本身的结构,但有效提高了铅离子的荧光响应效率(Ksv)。
基于CDs@MIL-101-NH2复合材料的水体铅离子荧光检测方法及效果分析
Fluorescence detection of lead ions in water and its effect analysis based on CDs@MIL-101-NH2 composite
-
摘要: 为探究CDs@MIL-101-NH2对铅离子的荧光法检测性能及荧光淬灭机理,采用水热法制备了碳点(N, S, I-CDs)修饰MIL-101-NH2(Fe)的复合材料,使用TEM、XRD、FT-IR、XPS对复合材料进行了表征。结果表明:采用水热法成功构建了CDs@MIL-101-NH2复合材料,碳点的引入未对MIL-101-NH2结构造成很大影响,且氨基修饰于MOF框架上;CDs@MIL-101-NH2复合材料在激发波长为340 nm、发射波长为436 nm、材料的质量浓度为10 mg·L−1、pH为7的条件下具有最佳荧光强度;CDs@MIL-101-NH2荧光探针可对水体铅离子做出荧光响应,有较好的选择性,在1.22~500 µmol·L−1内具有良好的拟合度(R2=0.998 8),检出限为1.22 µmol·L−1;荧光探针与铅离子结合后发生荧光淬灭现象,可能是由于复合材料上的氨基与铅离子发生相互作用引起的,且荧光碳点修饰提高了MIL-101-NH2检测水体铅离子的性能;在实际水样的铅离子检测中,样品回收率为97.24%~106.16%,相对标准偏差RSD<4%,说明这一新型的CDs@MIL-101-NH2复合材料可用于荧光法检测水体中的铅离子。本研究结果可为灵敏高效的荧光探针的设计与制备提供一种新思路,亦可为便捷的原位检测铅离子荧光方法的进一步开发和应用提供参考。
-
关键词:
- CDs@MIL-101-NH2复合材料 /
- 荧光探针 /
- 水体铅离子 /
- 荧光淬灭
Abstract: To investigate the performance of fluorometric detection for lead ions by CDs@MIL-101-NH2(Fe) and fluorescence quenching mechanism, carbon dots (N, S, I-CDs)-modified MIL-101-NH2(Fe) composite was prepared by hydrothermal method and was characterized by TEM, XRD, FT-IR and XPS. The results show that: CDs@MIL-101-NH2 composite was successfully prepared by hydrothermal method , and the introduction of carbon dots did not have a large effect on the MIL-101-NH2 structure, and the amino group modified the MOF framework; CDs@MIL-101-NH2 composite presented the highest fluorescence intensity at an excitation wavelength of 340 nm, an emission wavelength of 436 nm, dosage of 10 mg·L−1, and pH 7; CDs@MIL-101-NH2 fluorescent probe could fluorescently respond to lead ions in water with good selectivity and good fitting (R2=0.9988) within 1.22~500 µmol·L−1, the detection limit was 1.22 µmol·L−1. The fluorescence quenching occurred when the fluorescent probe combined with lead ions through the interaction between the amino group on the composite and lead ions, and the fluorescent carbon dot modification improved the performance of MIL-101-NH2 on detecting lead ions in water. During the detection of lead ions in the actual water samples, the sample recovery rates ranged from 97.24% to 106.16% with the relative standard deviations of RSD<4%, indicating that this novel CDs@MIL-101-NH2 composite can be used to test lead ions in water through fluorometric method. The results of this study can provide a new idea for the design and preparation of sensitive and efficient fluorescent probes, and also provide a reference for the further development and application of convenient in situ fluorescence methods for lead ions detection. -
基于污水源分离技术,生活污水按其来源和水质的不同可被分为灰水(grey water)和黑水(black water),灰水由厨房和卫生间的洗涤、洗浴水组成;黑水包括大小便和冲厕水等,约占生活污水总量的30%,化学需氧量(chemical oxygen demand, COD)、总氮(total nitrogen, TN)、悬浮固体(suspended solid, SS)、总磷(total phosphorus, TP)等污染物质量浓度高,处理难度大,同时具备资源化条件[1-3]。另外,黑水的高效处理与资源化对“厕所革命”的推进、农村人居卫生条件的改善等也至关重要[4]。黑水经化学强化高负荷活性污泥法(chemical enhance high-rate activated sludge, CEHRAS)捕获碳源后,虽然NH4+-N质量浓度可达100~300 mg·L−1,但各种氮回收技术仍不具有经济性[5],且碳氮比较低(COD/NH4+-N< 3)[6],传统硝化/反硝化工艺无法实现有效脱氮[7]。近年来,基于NO2−-N的高效低耗脱氮工艺如短程硝化-反硝化(partial nitrification-denitrification, PN/D)、短程硝化-厌氧氨氧化(partial nitrification-anammox, PN/A)等新型脱氮技术受到了广泛关注[8]。
长期稳定的短程硝化是实现PN/A等新型脱氮技术的前提与难点,其关键在于富集并促进氨氧化菌(ammonia-oxidizing bacteria, AOB)的同时有效抑制和淘汰亚硝酸盐氧化菌(nitrite-oxidizing bacteria, NOB)。目前已报道的短程硝化控制策略包括游离氨(free ammonia, FA)[9]、游离亚硝酸(free nitrous acid, FNA)[10]、碳氮比(C/N)[11]、温度[12]、进水氨氮负荷[13]、溶解氧(dissolved oxygen, DO)[14]、间歇曝气[15]、不同停曝比[16]等。采用单一的控制手段难以实现稳定的短程硝化,将多种控制策略组合应用能进一步提高短程硝化效果[17]。XU等[18]在移动床生物膜反应器(moving bed biofilm reactor, MBBR)中,通过控制DO、FA和FNA的质量浓度,实现了高效、稳定的短程硝化。WEN等[19]利用序批式反应器(sequential batch reactor, SBR),通过实时控制进水温度、pH、DO、FA等参数,在反应器运行的第16个周期成功启动短程硝化,并稳定运行了32 d。
在实际应用中,进水中的FA、FNA、C/N等参数难以实现灵活控制,而曝气模式和DO值较容易控制[20]。曝气控制相对于其它控制策略而言,具有操作简单、成本低廉等优点,有研究[21]认为,曝气控制是黑水实现短程硝化较为合适的策略。高氧持续曝气、间歇曝气和低氧持续曝气是3种常见的曝气方式,当前国内外研究中,有关3种曝气方式实现碳捕获预处理黑水部分亚硝化及其稳定性的文献报道较少。为此,本文采用SBR,对比研究了高氧持续曝气、间歇曝气和低氧持续曝气3种曝气方式实现碳捕获预处理黑水短程硝化的效果差异,剖析了不同曝气方式对微生物种群结构的影响,提出了实现长期稳定短程硝化的调控策略,以期为后续短程硝化与Anammox工艺的耦合奠定基础。
1. 材料与方法
1.1 实验装置
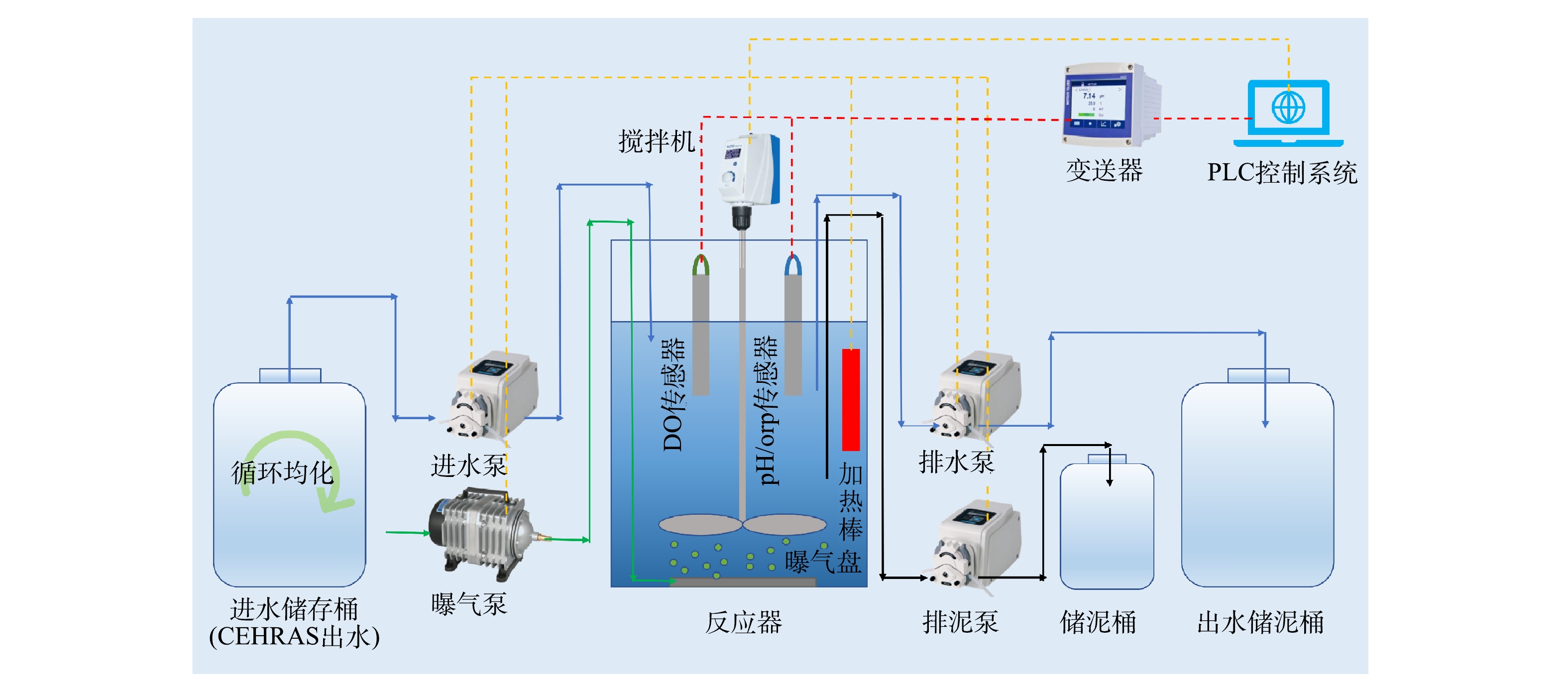
如图1所示,实验所用的SBR由反应器主体、进水泵、曝气泵与曝气盘、排泥泵、排水泵、搅拌器、加热棒以及控制系统组成。反应器主体为圆柱形,有机玻璃材质,内径为160 mm,有效体积为8 L。控制系统由DO传感器(Oxymax COS22D,Endress + Hauser)、pH/氧化还原电位(oxidation-reduction potential, ORP)复合传感器(Memosens CPS16D,Endress + Hauser)、变送器(Liquidline CM44,Endress + Hauser)和可编程逻辑控制器(programmable logic controller, PLC,7-200 Smart CPU,Siemens)等模块组成。通过编程,PLC可灵活控制各设备的工作状态。SBR周期可分为进水、反应、排泥、沉淀、排水和闲置6个阶段。
1.2 实验用污水及接种污泥
实验所用污水为CEHRAS小试装置的出水,该碳源捕获装置以黑水作为进水,所用黑水为校园图书馆及教学楼的厕所污水。SBR装置各工况的进水水质特征如表1所示。实验所用接种污泥来自于上海某生活污水处理厂(厌氧-缺氧-好氧工艺)的内回流活性污泥。
表 1 各工况的进水水质特征Table 1. Wastewater quality characteristics of influent at different phases工况 pH 质量浓度/(mg·L−1) COD NH4+-N NO2−-N NO3−-N 碱度(以CaCO3计) Ⅰ 8.2±0.1 352±129 194±38 <0.5 0.9±0.6 792±173 Ⅱ 8.0±0.2 162±118 146±49 ND 1.1±0.9 550±270 Ⅲ 8.1±0.1 213±90 187±48 ND 0.3±0.2 628±192 注:ND表示未检出。 1.3 运行工况条件
工况Ⅰ、Ⅱ、Ⅲ分别采用高氧持续曝气、间歇曝气和低氧持续曝气的曝气方式。3种曝气方式的控制策略如下:高氧持续曝气工况期间,固定曝气量和曝气时间,DO未控制,DO值可达2~7 mg·L−1;间歇曝气工况采用曝气20 min,停止曝气10 min交替进行的曝气策略,当反应器内pH<6.2时停止曝气(在预实验和前期研究[21]的基础上选择了pH<6.2作为控制点),DO未控制,曝气阶段反应器的DO值可达到4~6 mg·L−1,反应阶段反应器内DO均值为(0.8±0.6) mg·L−1;低氧持续曝气工况则控制DO为0.3 mg·L−1,持续曝气,当反应器内pH<6.2时停止曝气。各工况运行期间温度控制在25~30 ℃,具体运行条件如表2所示。
表 2 3种曝气控制策略的具体工况条件Table 2. Specific operational conditions of three aeration control strategies工况 SRT/d SBR程序 曝气策略 Ⅰ 10 总周期12 h;VER=50%;进水15 min;反应600 min;排泥5 min;沉淀60 min;排水15 min;闲置25 min DO=2~7 mg·L-1 曝气时长固定 Ⅱ 40 总周期12 h;VER=50%;进水15 min;反应600 min;排泥5 min;沉淀60 min;排水15 min;闲置25 min 交替曝气20 min/不曝气10 min pH<6.2停止曝气 Ⅲ 40 总周期12 h;VER=50%;进水15 min;反应600 min;排泥5 min;沉淀60 min;排水15 min;闲置25 min DO=0.3 mg·L−1 pH<6.2停止曝气 注:VER表示SBR体积交换比(volume exchange rate);尽管高氧持续曝气未采用pH实时判别曝气终点,但由于污泥龄(sluge retention time, SRT)短、生物量低,在固定曝气时长反应末期(600 min)pH接近6.2,与间歇曝气和低氧持续曝气终点pH判定功能相差不大。 1.4 分析方法
采用HACH-COD试剂盒测定COD;采用纳氏试剂分光光度法测定氨氮;采用N-1-(奈基)-乙二胺光度法测定亚硝态氮;采用紫外分光光度法测定硝态氮;采用HACH HQ40d测定仪测定DO和pH;采用重量法测定混合液悬浮固体浓度(mixed liquor suspended solids, MLSS)和混合液挥发性悬浮固体浓度(mixed liquor volatile suspended solids, MLVSS);采用电位滴定法测定碱度;每个工况运行结束后,提取反应器内的污泥样品,由上海美吉生物测序分析微生物群落组成。
1.5 亚硝态氮累积率的计算
亚硝态氮累积率(nitrite accumulation ratio, NAR)按式(1)进行计算。
NAR = CNO2−-NCNO2−-N+CNO−3-N×100% (1) 式中:NAR为亚硝态氮累积率;
CNO2−-N CNO3−-N 2. 结果与讨论
2.1 SBR短程硝化反应器进水、出水氮素质量浓度
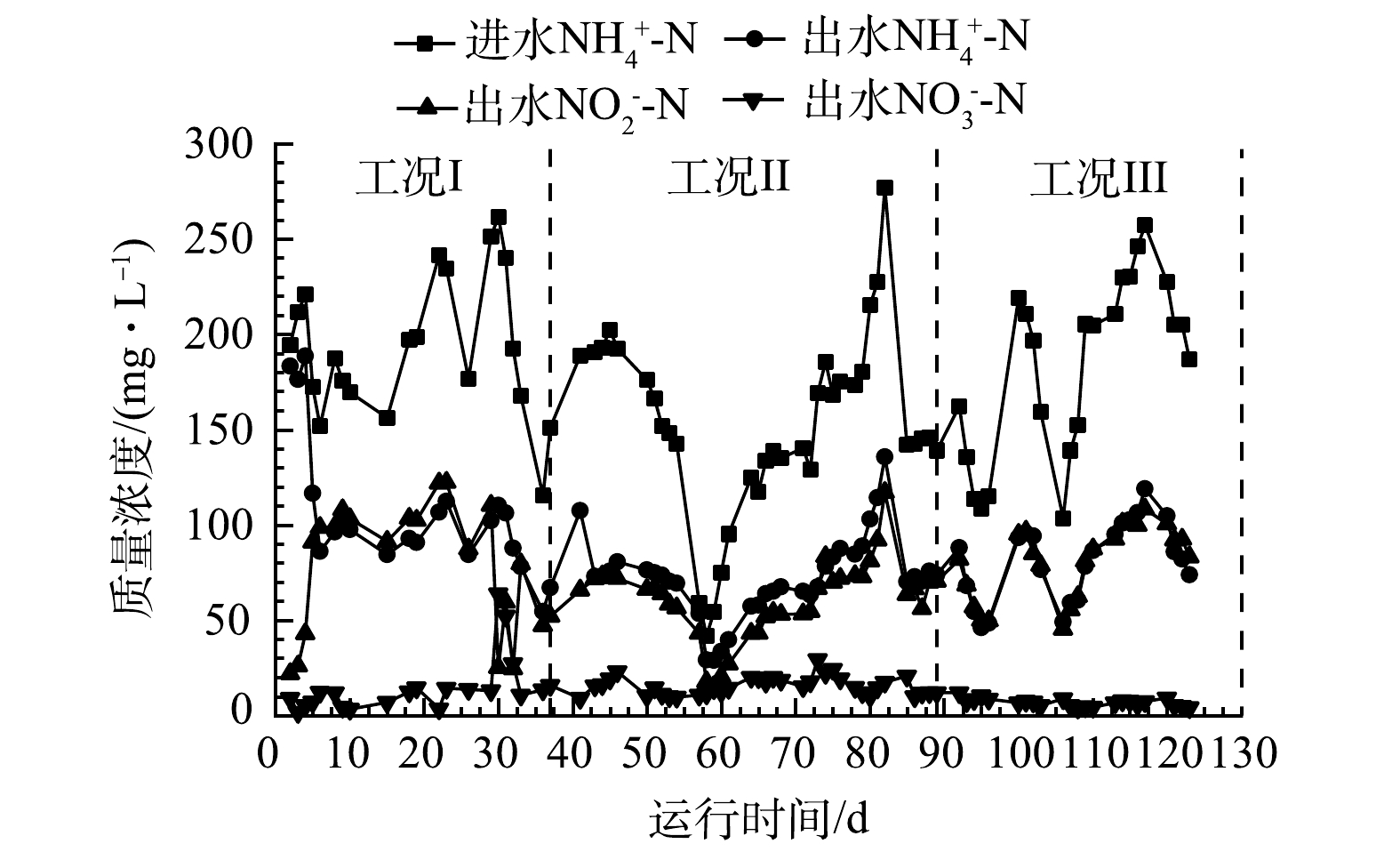
图2为3种工况的进出水氮素质量浓度随运行时间的变化。对于工况Ⅰ,0~4 d内反应器处于启动阶段,NH4+-N去除率(ammonium removal efficiency, ARE)仅为12.4%,出水NO2−-N和NO3−-N质量浓度较低;第5~29天,进水NH4+-N质量浓度为(193±33) mg·L−1,出水NH4+-N、NO2−-N和NO3−-N质量浓度均维持在较稳定的水平,分别为(97.7±10.6)、(103±11)和(9.9±4.4) mg·L−1;第30天,在进水NH4+-N质量浓度变化不大的情况下,出水NO2−-N质量浓度急剧下降,由110 mg·L−1下降到25.3 mg·L−1,出水NO3−-N质量浓度由13.2 mg·L−1增加到63.9 mg·L−1。结果表明,在运行的第5~29天,反应阶段反应器内积累了较高质量浓度的NO2−-N,同时DO维持在较高值,这些环境因素有利于NOB表现出较高活性。然而,由于在SBR每个运行周期中都存在进水过程、沉淀过程等缺氧阶段,且每个周期进水后反应器内的NO2−-N质量浓度会大幅下降,从而使得NOB不能一直保持较高的活性。第30~37天出水NO2−-N质量浓度较第5~29天有所下降,且呈现波动性变化,而出水NO3−-N质量浓度呈现交错式的波动变化。故高氧持续曝气虽然能在反应器成功启动后的一定时间段内维持较好的短程硝化效果,但NOB的活性得不到有效抑制,进而影响了短程硝化的稳定性。
在工况Ⅱ,除第57~60天,由于进水NH4+-N质量浓度过低而导致出水氮素质量浓度变化失常(4 d的总氮去除率均值为负值,这与SBR的体积交换比为50%有关),该工况其余运行时间内,虽然进水NH4+-N质量浓度波动较大,但出水NH4+-N和NO2−-N质量浓度随进水NH4+-N质量浓度同步稳定变化,分别为(77.0±18.0) mg·L−1和(65.7±15.8) mg·L−1,出水NO3−-N质量浓度为(16.1±5.0) mg·L−1。该工况反应器内的溶解氧环境在缺氧和好氧之间交替变化,这在一定程度上可抑制NOB的活性,从而未出现工况Ⅰ中出水NO2−-N质量浓度急剧下降的情况。
在低氧持续曝气阶段(工况Ⅲ),在整个运行期间(92~123 d),出水NH4+-N和NO2−-N质量浓度随进水NH4+-N浓度稳定变化,分别为(81.6±21.5) mg·L−1和(81.6±19.9) mg·L−1,且相对于前2个工况,出水NO3−-N质量浓度稳定维持在较低水平,为(6.7±1.9) mg·L−1。
2.2 ARE、NAR及出水NO2−-N/NH4+-N
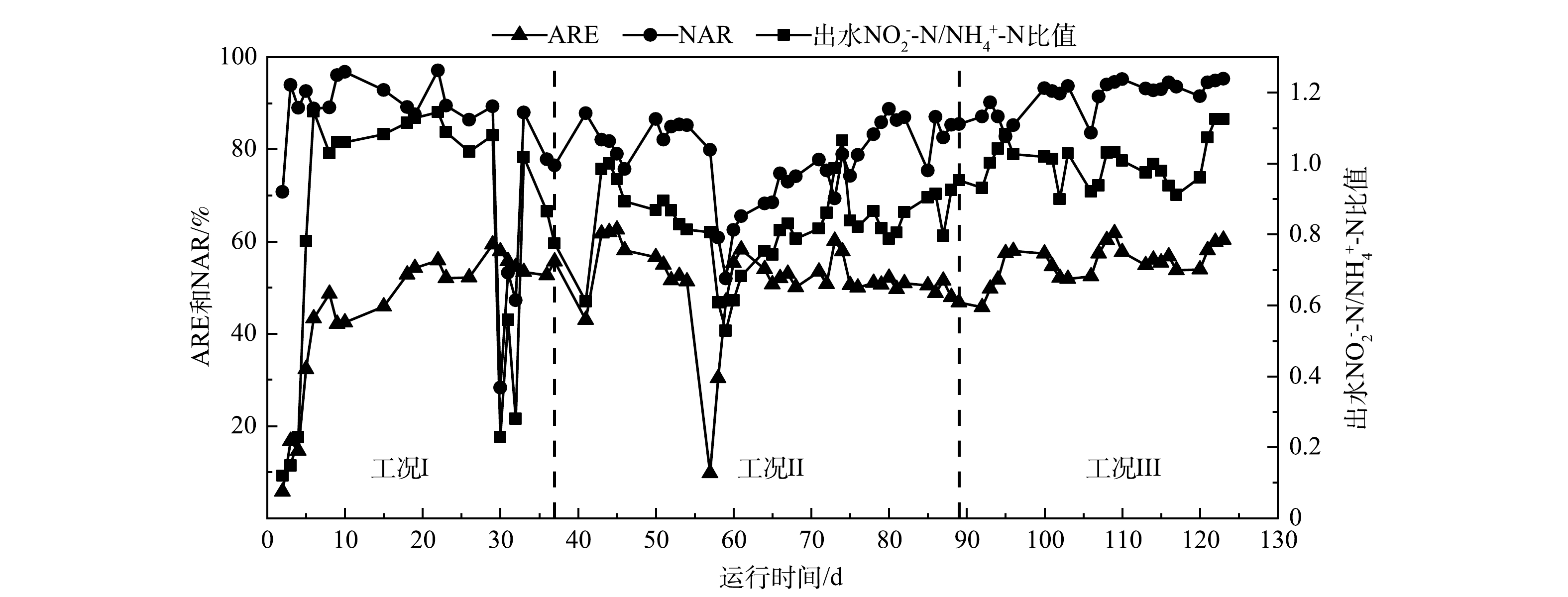
3种工况的ARE、NAR及出水NO2−-N/NH4+-N随运行时间的变化情况如图3所示。对于高氧持续曝气工况,从装置成功启动直至该工况结束,ARE一直维持在较稳定的水平,为(47.1±12.6)%;对于NAR和出水NO2−-N/NH4+-N,在短程硝化反应器启动后的一定时间段内能维持较稳定的水平,但随着运行时间的增加,NOB逐渐适应了反应器内的环境并表现出较高的活性,使得NAR和出水NO2−-N/NH4+-N急剧下降,并进一步影响后续运行效果,短程硝化效果不稳定。
在间歇曝气阶段,由于在57~60 d内反应器进出水氮素质量浓度变化失常而导致ARE大幅度下降,该工况其余运行时间的ARE、NAR及出水NO2−-N/NH4+-N分别为(53.0±4.6)%、(79.9±6.5)%和(0.90±0.09),维持在较稳定的水平。对于低氧持续曝气工况,尽管运行期间进水NH4+-N质量浓度波动较大,但该工况的ARE、NAR以及出水NO2−-N/NH4+-N均较为稳定,分别为(56.3±3.0)%、(91.8±3.8)%和(1.01±0.06)。
ARE主要受进水碱度/NH4+-N以及好氧水力停留时间(hydraulic retention time, HRT)的影响。3种曝气策略均可保证足够长的好氧HRT,因此,ARE主要受进水碱度/NH4+-N的影响。3种工况中,进水碱度/NH4+-N分别为(4.19±0.19)、(3.55±0.20)和(3.71±0.22),其中间歇曝气工况去除了57~60 d的数据。有研究[22]表明,当碱度小于50 mg·L−1时氨氮氧化停止,3种工况出水的碱度分别为(26.6±4.5)、(24.0±9.3)和(23.1±4.9) mg·L−1,出水碱度几乎被消耗殆尽。由于氧化1 g的NH4+-N需要消耗碱度7.14 g,假定碱度完全消耗时停止硝化反应,且不存在其它碱度产生与消耗过程,理论上3种工况的ARE分别为58.7%、49.8%和52.1%。间歇曝气和低氧持续曝气工况的实际ARE略高于理论值。这可能是因为在2种工况下反应器内存在同步反硝化过程,从而补充了部分碱度。高氧持续曝气工况的实际运行ARE均值低于理论值。这是由于SBR处于启动阶段时,AOB丰度和活性较低,ARE维持在较低水平,同时,AOB和NOB的繁殖也会消耗部分碱度[23];当反应器进入稳定运行阶段后,实际运行的ARE与理论值相近。
NAR主要受AOB和NOB活性的影响,AOB与NOB的活性比值越大,NAR值越大。故在3种曝气策略中,低氧持续曝气工况中AOB与NOB的活性比值最大。高氧持续曝气的NAR出现大幅度波动,难以实现稳定短程硝化。间歇曝气是一种抑制NOB活性的有效手段,这是因为在经过缺氧阶段后当反应器重新开始曝气时,NOB活性恢复比AOB慢[24-25]。但是,如果重新开始曝气时反应器内NO2−-N质量浓度较高,NOB活性恢复速度将加快,从而导致短程硝化效果不佳[25]。在间歇曝气工况的曝气阶段,反应器内积累了较高浓度的NO2−-N,由于反应器进水碳氮比较低(COD/NH4+-N<2),反硝化菌无法获得足够的电子供体,在停曝阶段NO2−-N并不会被大量还原,重新开始曝气时反应器内具有较高质量浓度的NO2−-N,NOB活性恢复较快,故间歇曝气并未获得比高氧持续曝气更高的NAR。出水NO2−-N/NH4+-N由ARE和NAR共同决定,低氧持续曝气工况的出水NO2−-N/NH4+-N最高,但3种工况的出水NO2−-N/NH4+-N均低于Anammox过程的化学计量学比。
2.3 微生物群落分析
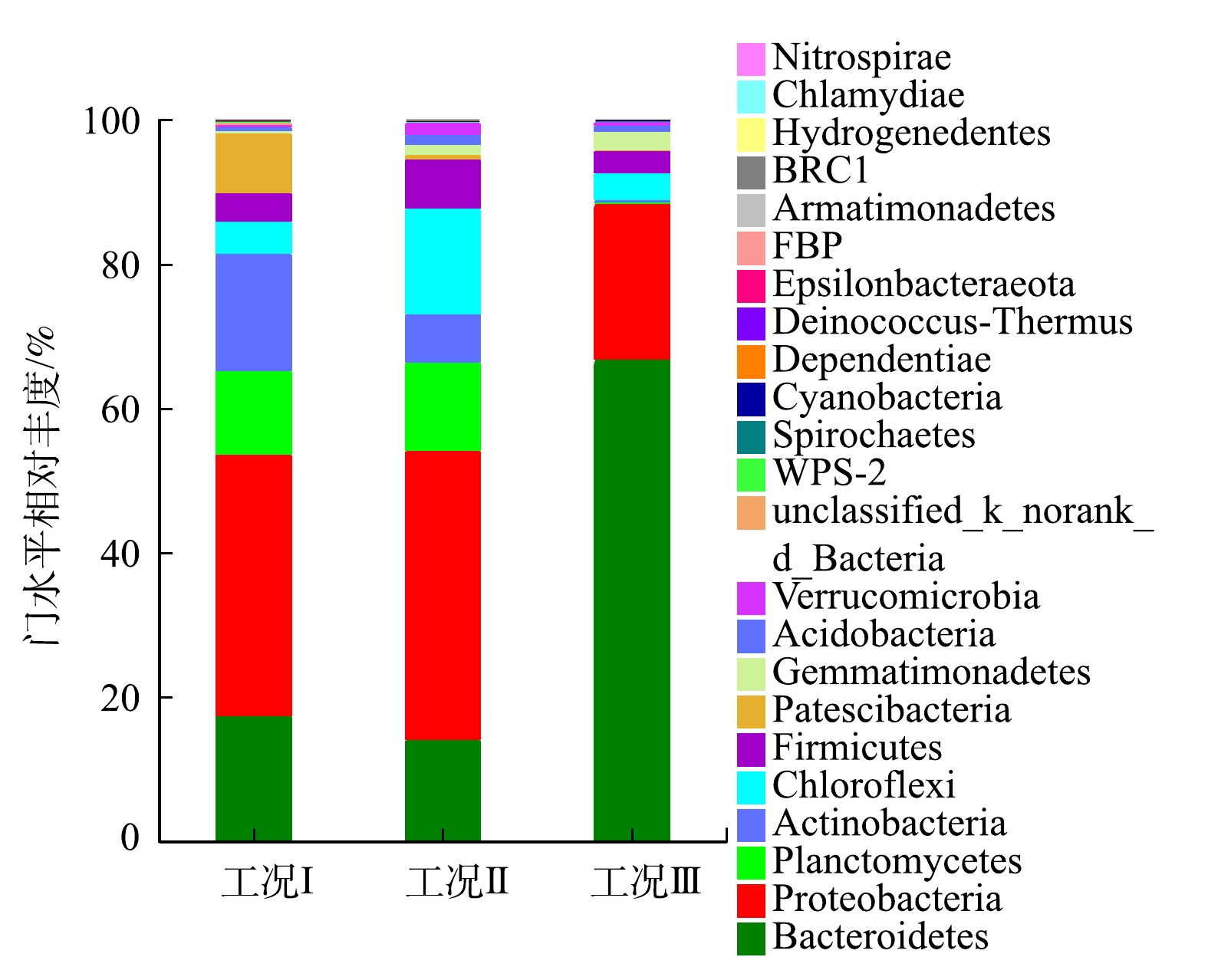
表3为接种污泥和不同工况污泥中AOB和NOB菌群的相对丰度,各工况污泥样品在菌门水平上的微生物组成结构如图4所示。AOB属于变形菌门(Proteobacteria),分为Nitrosomonas、Nitrosospira、Nitrosovibiro、Nitrosolobus和Nitrosococcus 5个属。污水处理厂中以Nitrosomonas最为常见[26]。Nitrospira和Nitrobacter是污水处理厂污泥中2种常见的NOB,前者属于硝化螺旋菌门(Nitrospirae),后者属于变形菌门[26]。接种污泥中检测到的AOB只有Nitrosomonas,NOB有Nitrospira和Nitrobacter 2个属,Nitrosomonas和Nitrospira分别是占主导地位的AOB和NOB。
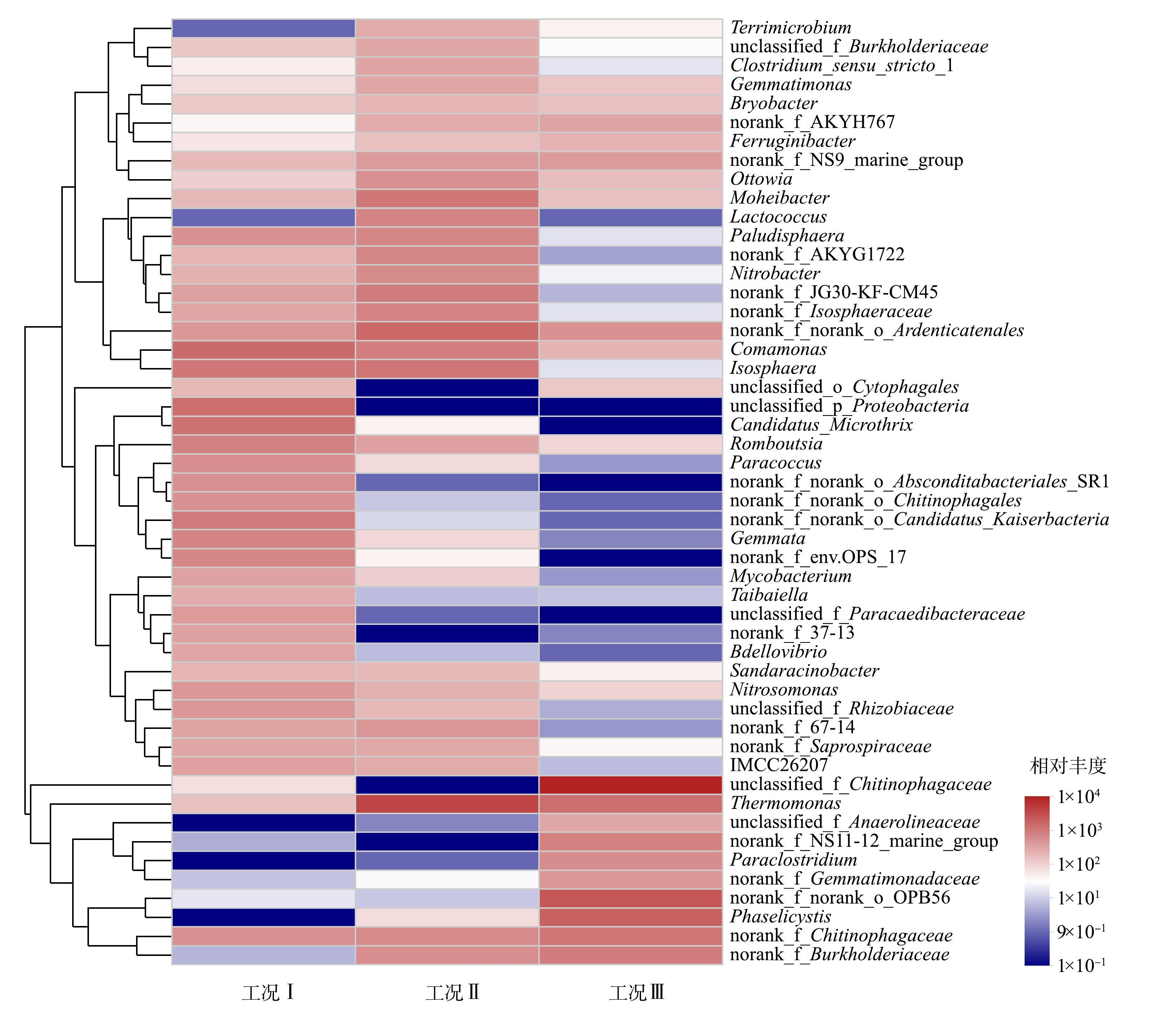
表 3 接种污泥和不同工况污泥中AOB和NOB的相对丰度Table 3. Relative abundances of AOB and NOB in inoculum sludge and sludge at different phases污泥样品来源 AOB/% NOB/% AOB/NOB相对丰度比 Nitrosomonas Nitrospira Nitrobacter 接种污泥[27] 0.089 0.39 0.15 0.16 工况Ⅰ 1.99 — 1.02 1.95 工况Ⅱ 1.02 — 2.42 0.42 工况Ⅲ 0.38 0.01 0.07 4.75 注:“—”表示无法检出或相对丰度低于0.01%。 如图4所示,在高氧持续曝气工况后,污泥中排名前5的菌门为变形菌门(36.2%)、拟杆菌门(17.5%)、放线菌门(16.2%)、浮霉状菌门(11.6%)和髌骨细菌门(8.2%)。相对于接种污泥,Nitrospira属被洗脱出系统,Nitrobacter成为唯一的NOB。AOB和Nitrobacter的相对丰度均有所提高,Nitrosomonas的相对丰度由0.089%显著增加至1.99%,同时Nitrobacter的相对丰度由0.15%增至1.02%。间歇曝气工况后,污泥中排名前5的微生物菌门为变形菌门(40.1%)、绿屈绕菌门(14.6%)、拟杆菌门(14.1%)、浮霉状菌门(12.2%)和厚壁菌门(6.9%)。除变形菌门保持丰度最高位置,第2~5名顺序均发生变化。Nitrosomonas相对丰度降至1.02%,Nitrobacter则增至2.42%,同时AOB/NOB相对丰度比降至0.42。切换至低氧持续曝气工况并运行30 d后,排名前5的微生物菌门变为拟杆菌门(66.8%)、变形菌门(21.6%)、绿屈绕菌门(3.8%)、厚壁菌门(3.1%)和芽单胞菌门(2.5%)。微生物群落结构变化较大,拟杆菌门替代变形菌门成为相对丰度最高的微生物菌门。变形菌门的相对丰度降低了约50%,这归属于该菌门的Nitrosomonas和Nitrobacter相对丰度分别降至0.38%和0.07%,Nitrobacter得到了有效抑制并正在逐渐洗脱出系统。虽然在低氧条件下AOB的相对丰度也有所下降,但AOB/NOB丰度比显著增至4.75。同时,值得注意的是,反应器中出现了对氧亲和能力更高的Nitrospira,但相对丰度仅为0.01%。
Nitrospira的生存方式为K-选择型,即比生长速率低而底物亲和能力强,而Nitrobacter与之相反,属于r-选择型[28]。在城市污水处理厂生化池内,氨氮质量浓度低且碱度充足,不容易发生NO2−-N的积累,NO2−-N质量浓度较低,主导型NOB为Nitrospira。重力式污水源分离收集系统中的黑水中NH4+-N质量浓度在100~300 mg·L−1,显著高于市政污水的25~75 mg·L−1[29]。在本研究中,高氧持续曝气、间歇曝气和低氧持续曝气3个工况稳定运行时的NO2−-N出水质量浓度分别为(79.8±32.9)、(59.5±21.4)和(81.6±19.9) mg·L−1,远高于市政污水生化池中的NO2−-N质量浓度。因此,不同于接种污泥,3种工况中主导NOB均为Nitrobacter。
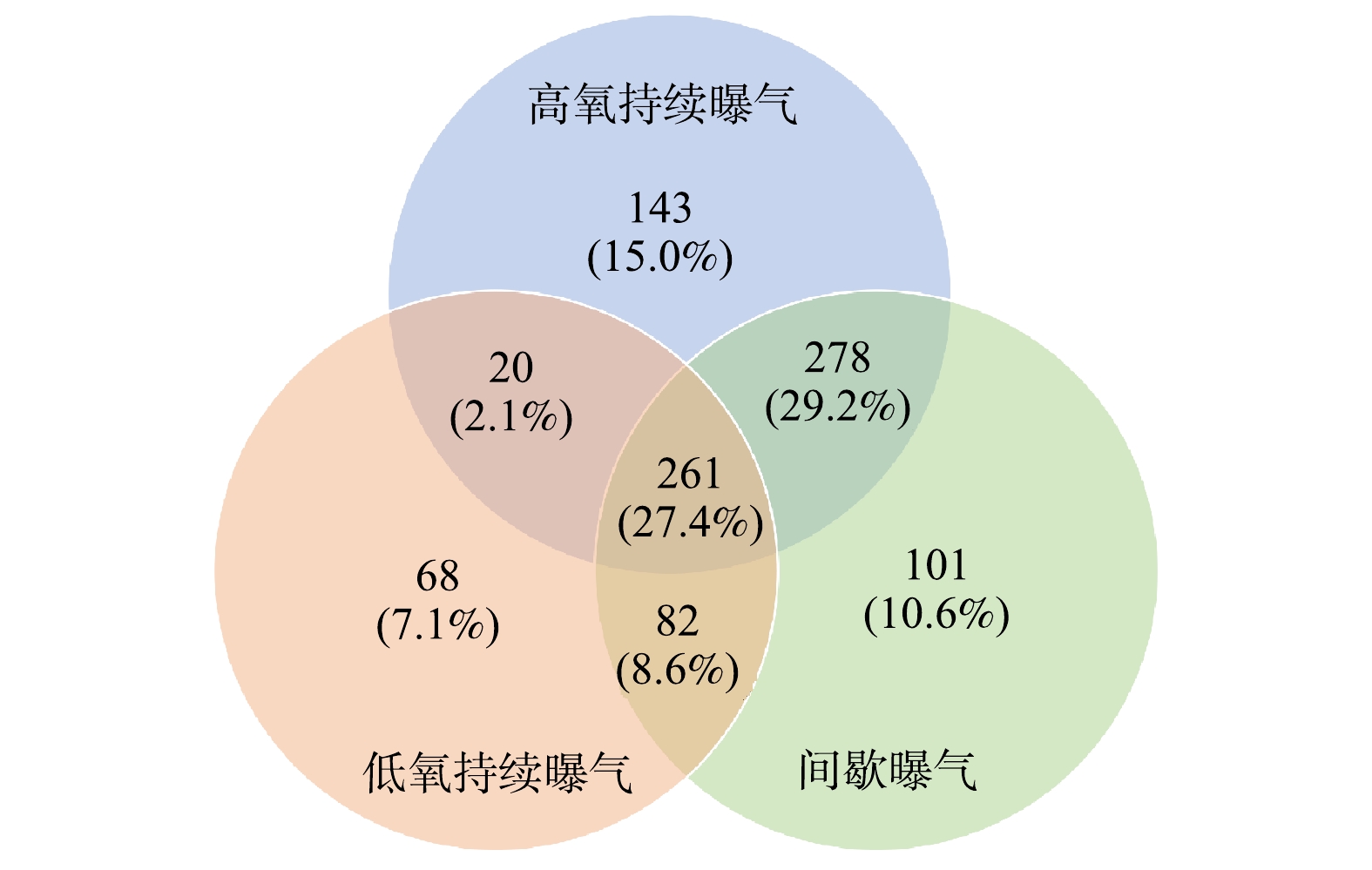
基于高通量测序结果,对不同工况污泥样品绘制的物种Venn图如图5所示。高氧持续曝气和间歇曝气污泥样品的操作分类单元(operational taxonomic units, OTU)数量基本一致,而低氧持续曝气污泥样品的OTU数量低于前两者。高氧持续曝气、间歇曝气和低氧持续曝气工况中污泥所特有的OTU数量占比分别为15.0%、10.6%和7.1%,呈现逐渐下降的趋势,这表明不同曝气策略对微生物菌落结构的改变有一定的影响。为了进一步比较不同工况污泥中物种组成差异,使用热图进行物种组成分析。使用平均丰度前50位属的丰度数据绘制聚类热图。由图6可见,红色区域代表该样品中相对丰度较高的物种,3个样品中红色区域分布差异明显。这表明在不同的曝气策略下,富集到的微生物菌落在种类和相对丰度上存在一定的差异。
2.4 实现长期稳定短程硝化的曝气策略分析
高氨氮质量浓度(500~1 500 mg·L−1)废水实现短程硝化较为容易,通常采用低氧曝气策略[30]。对于碳源捕获后黑水的短程硝化,低氧持续曝气的优势在于短程硝化效果更好,而高氧持续曝气的优势在于HRT更短;间歇曝气控制策略虽然能在一定程度上抑制NOB的活性,但并未表现出明显优势。工况Ⅲ的结果表明,碳捕获预处理黑水若长时间采用低氧持续曝气,可能导致Nitrospira丰度增加,进而影响短程硝化效果。因此,可考虑运行一段时间低氧持续曝气后切换为高氧持续曝气,抑制和洗脱Nitrospira,然后再切换回低氧持续曝气。
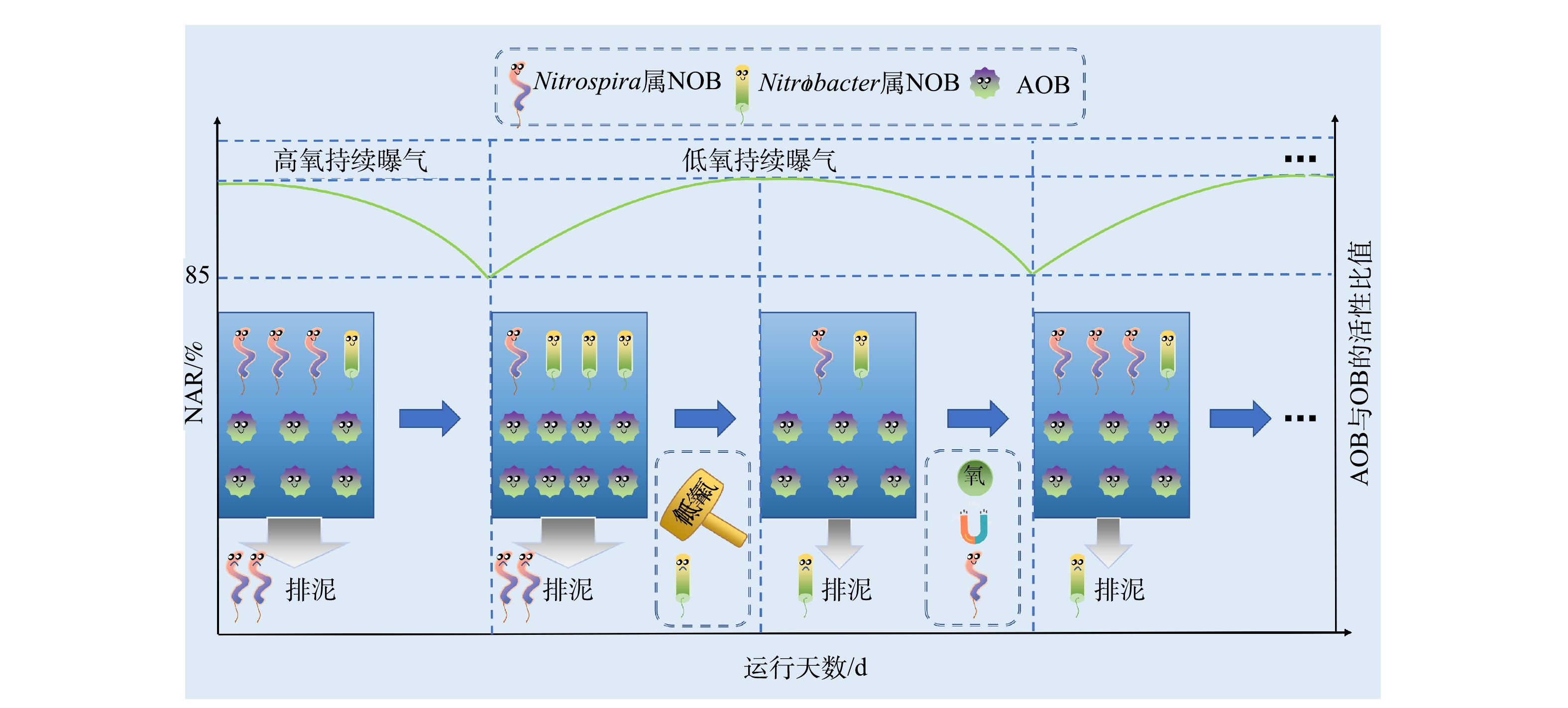
如图7所示,在高氧持续曝气工况下,AOB和Nitrobacter属NOB相对丰度增加。采用较短的污泥龄(本研究中采用10 d)有利于将Nitrospira属NOB从系统中洗脱,然而Nitrobacter相对丰度的增加会逐渐影响短程硝化效果。当反应器的NAR下降至85%左右时,将曝气模式切换至低氧持续曝气。低氧持续曝气工况下,由于DO的限制作用,AOB的相对丰度有所下降,同时Nitrobacter的比增长速率μ变小,即使采用较长的污泥龄(本研究中的40 d)也能将其从反应器中逐渐洗脱;而Nitrospira属对氧亲和能力更高,其相对丰度可能会逐渐增加并影响系统的短程硝化效果。当反应器的NAR下降至85%左右时,将曝气方式切换为高氧持续曝气,对Nitrospira进行抑制和洗脱的同时提高AOB的相对丰度。如此交替运行2种曝气策略,分别实现对Nitrospira和Nitrobacter的抑制和洗脱,有助于形成长期稳定的短程硝化效果。
3. 结论
1) 3种曝气控制策略均能实现碳捕获预处理黑水的部分亚硝化。相对于高氧持续曝气和间歇曝气工况,低氧持续曝气工况的NAR更高,出水NO2−-N/NH4+-N更接近厌氧氨氧化进水的水质要求。
2) 3种曝气控制策略中AOB优势菌属均为Nitrosomonas,NOB优势菌属均为Nitrobacter。高氧持续曝气工况能逐步洗脱Nitrospira,同时提高AOB和Nitrobacter的相对丰度;低氧持续曝气工况能显著降低Nitrobacter的相对丰度,但低DO条件下AOB相对丰度降低并出现了对氧亲和能力更高的Nitrospira。
3)经碳源回收后的黑水,建议使用高氧持续曝气与低氧持续曝气交替组合运行的控制策略,分别实现对Nitrospira和Nitrobacter的抑制和洗脱,从而有利于实现较好稳定的短程硝化效果。
-
表 1 各种MOFs材料对Pb2+的荧光检测性能
Table 1. Parameters of lead ion fluorescence detection performance of various modified MOFs
表 2 自来水和思源湖湖水水样中Pb2+加标回收率和相对标准偏差结果
Table 2. Pb2+ spiked recovery rates and relative standard deviations in water samples from tap water and Siyuan Lake
样品 加标溶液/(µmol·L−1) 检测值/(µmol·L−1) 加标回收率/% 相对标准偏差/% 自来水-1 25 26.54 106.16 3.51 自来水-2 50 49.37 98.74 1.87 自来水-3 100 105.3 105.3 2.33 思源湖湖水-1 25 24.31 97.24 1.74 思源湖湖水-2 50 50.69 101.38 0.97 思源湖湖水-3 100 103.63 103.63 2.16 -
[1] NAG R, CUMMINS E. Human health risk assessment of lead (Pb) through the environmental-food pathway[J]. Science of the Total Environment, 2021, 15: 1168-1182. [2] LOU J, JIN L, WU N, et al. DNA damage and oxidative stress in human B lymphoblastoid cells after combined exposure to hexavalent chromium and nickel compounds[J]. Food and Chemical Toxicology, 2013, 55: 535-540. [3] LI X, ZHANG B, LI N, et al. Zebrafish neurobehavioral phenomics applied as the behavioral warning methods for fingerprinting endocrine disrupting effect by lead exposure at environmentally relevant level[J]. Chemosphere, 2019, 231: 315-325. doi: 10.1016/j.chemosphere.2019.05.146 [4] CLEMENS S, MA J F. Toxic heavy metal and metalloid accumulation in crop plants and foods[J]. Annual Review of Plant Biology, 2016, 67: 489-512. doi: 10.1146/annurev-arplant-043015-112301 [5] 中华人民共和国国家环境保护总局, 国家质量监督检验检疫总局. 地表水环境质量标准: GB 3838-2002[S]. 北京: 中国环境科学出版社, 2003. [6] 蔡良圣, 林君, 辛青, 等. 电化学传感器监测水中痕量铜离子[J]. 中国环境科学, 2020, 40(8): 3394-3400. doi: 10.3969/j.issn.1000-6923.2020.08.017 [7] YAN S R, FOROUGHI M M, SAFAEI M, et al. A review: Recent advances in ultrasensitive and highly specific recognition aptasensors with various detection strategies[J]. International Journal of Biological Macromolecules, 2020, 155: 184-207. doi: 10.1016/j.ijbiomac.2020.03.173 [8] SARFO D K, IZAKE E L, OʹMULLANE A P, et al. Molecular recognition and detection of Pb(II) ions in water by aminobenzo-18-crown-6 immobilised onto a nanostructured SERS substrate[J]. Sensors and Actuators B:Chemical, 2018, 255: 1945-1952. doi: 10.1016/j.snb.2017.08.223 [9] OZDEMIR M. A novel chromogenic molecular sensing platform for highly sensitive and selective detection of Cu2+ ions in aqueous environment[J]. Journal of Photochemistry & Photobiology A:Chemistry, 2019, 369: 54-69. [10] NAIK L, MARIDEVARMATH C V, THIPPESWAMY M S, et al. A highly selective and sensitive thiophene substituted 1, 3, 4-oxadiazole based turn-off fluorescence chemosensor for Fe2+ and turn on fluorescence chemosensor for Ni2+ and Cu2+ detection[J]. Materials Chemistry and Physics, 2021, 260: 63-75. [11] HE Y B, ZHOU W, QIAN G D, et al. Methane storage in metal-organic frameworks[J]. Chemical Society Reviews, 2014, 43: 5657-5679. doi: 10.1039/C4CS00032C [12] RAZAVI S A A, MASOOMI M Y, ISLAMOGLU T, et al. Improvement of methane-framework interaction by controlling pore size and functionality of pillared MOFs[J]. Inorganic Chemistry, 2017, 56: 2581-2588. doi: 10.1021/acs.inorgchem.6b02758 [13] RAZAVI S A A, MASOOMI A. Function-structure relationship in metal-organic frameworks for mild, green, and fast catalytic C-C bond formation[J]. Inorganic Chemistry, 2019, 58: 14429-14439. doi: 10.1021/acs.inorgchem.9b01819 [14] MOROZAN A, JAOUEN F. Metal organic frameworks for electrochemical applications[J]. Energy & Environmental Science, 2012, 5: 9269-9290. [15] RAZAVI S A A, MORSALI A. Metal ion detection using luminescent-MOFs: Principles, strategies and roadmap[J]. Coordination Chemistry Reviews, 2020, 415: 213299-213342. doi: 10.1016/j.ccr.2020.213299 [16] 李孜旋. 荧光功能NH2-MIL-53(Al)纳米片及其复合材料用于水中离子检测研究[D]. 合肥: 中国科学技术大学, 2021. [17] LIU Y, MA L N, SHI W J, et al. Four alkaline earth metal (Mg, Ca, Sr, Ba)-based MOFs as multiresponsive fluorescent sensors for Fe3+, Pb2+ and Cu2+ ions in aqueous solution[J]. Journal of Solid State Chemistry, 2019, 227: 636-647. [18] LI L, CHEN Q, NIU Z G, et al. Lanthanide metal-organic frameworks assembled from a fluorene-based ligand: selective sensing of Pb2+ and Fe3+ ions[J]. Journal of Materials Chemistry C, 2016, 4: 1900-1905. doi: 10.1039/C5TC04320D [19] HAO J, LIU F, LIU N, et al. Ratiometric fluorescent detection of Cu2+ with carbon dots chelated Eu-based metal-organic frameworks[J]. Sensor and Actuators B:Chemical, 2017, 245: 641-647. doi: 10.1016/j.snb.2017.02.029 [20] XU X, YAN B. Fabrication and application of a ratiometric and colorimetric fluorescent probe for Hg2+ based on dual-emissive metaleorganic framework hybrids with carbon dots and Eu3+[J]. Journal of Materials Chemistry C, 2016, 4: 1543-1549. doi: 10.1039/C5TC04002G [21] WANG H, YAN B. N-GQDs and Eu3+ co-encapsulated anionic MOFs: Two-dimensional luminescent platform for decoding benzene homologues[J]. Dalton Transactions, 2017, 46(21): 7098-7105. doi: 10.1039/C7DT01352C [22] YAO C, XU Y, XIA Z. A carbon dot-encapsulated UiO-type metal organic framework as a multifunctional fluorescent sensor for temperature, metal ion and pH detection[J]. Journal of Materials Chemistry C, 2018, 6(16): 4396-4399. doi: 10.1039/C8TC01018H [23] BANERJEE D, HU Z C, LI J. Luminescent metal-organic frameworks as explosive sensors[J]. Dalton Transactions, 2014, 43: 10668-10685. doi: 10.1039/C4DT01196A [24] LV S W, LIU J M, LI C Y, et al. A novel and universal metal-organic frameworks sensing platform for selective detection and efficient removal of heavy metal ions[J]. Chemical Engineering Journal, 2019, 375: 122111-122121. doi: 10.1016/j.cej.2019.122111 [25] DUAN M, GUAN Z, MA Y J, et al. A novel catalyst of MIL-101(Fe) doped with Co and Cu as persulfate activator: Synthesis, characterization, and catalytic performance[J]. Chemical Papers, 2018, 72: 235-250. doi: 10.1007/s11696-017-0276-7 [26] FAZAELI R, ALIYAN H, MOGHADAM, et al. Nano-rod catalysts: Building MOF bottles (MIL-101 family as heterogeneous single-site catalysts) around vanadium oxide ships[J]. Journal of Molecular Catalysis A:Chemical, 2013, 374-375: 46-52. doi: 10.1016/j.molcata.2013.03.020 [27] MU Z, HUA J H, YANG Y L. N, S, I co-doped carbon dots for folic acid and temperature sensing and applied to cellular imaging[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2020, 224: 117444-117453. doi: 10.1016/j.saa.2019.117444 [28] HASAN Z, KHAN N A, JHUNG S H. Adsorptive removal of diclofenac sodium from water with Zr-based metal-organic frameworks[J]. Chemical Engineering Journal, 2016, 284: 1406-1413. doi: 10.1016/j.cej.2015.08.087 [29] WU L, ZHANG X F, LI Z Q, et al. A new sensor based on amino-functionalized zirconium metal-organic framework for detection of Cu2+ in aqueous solution[J]. Inorganic Chemistry Communications, 2016, 74: 22-25. doi: 10.1016/j.inoche.2016.10.031 [30] 王雨霏. 碳点@ZIF-8复合材料的制备与性能研究[D]. 长春: 吉林大学, 2021. [31] 胥静. 镧系金属有机框架材料的合成及其在荧光传感中的应用[D]. 南充: 西华师范大学, 2020. [32] LI B Z, SUO T Y, XIE S Y, et al. Rational design, synthesis, and applications of carbon dots@metal-organic frameworks (CD@MOF) based sensors[J]. Trends in Analytical Chemistry, 2021, 135: 116163. doi: 10.1016/j.trac.2020.116163 -





 下载:
下载: