-
漆酶是一类含铜多酚氧化酶,广泛存在于真菌、细菌和部分植物中,其特征在于铜氧还原蛋白结构中含有4个铜离子[1]。依据电磁学特征,T1和T2型2个铜均为单电子受体,呈现顺磁性;而T3型铜含有2个铜离子,为双电子受体,呈现反磁性。T2和T3铜位点构成三核铜簇中心,与T1铜相互连通,参与漆酶的催化氧化过程。漆酶可以利用分子氧为唯一的电子受体,氧化各种酚类、芳香族化合物及其胺类化合物[2-3]。因此,漆酶是一种优良的绿色生物催化剂,广泛应用于生物传感、医药加工、有机合成、及废水处理等工程应用领域[4]。然而,游离漆酶对环境条件表现出极高的敏感性,这意味着漆酶在自然条件下(pH、温度等)的稳定性相对较差[5-6]。漆酶的低稳定性和高生产成本导致漆酶在实际工业应用中受到限制。而且,游离漆酶在复杂环境中极易变性,回收十分困难。提高漆酶的稳定性和可重复使用性是漆酶相关研究的一个重要方向[7],因此,酶的固定化是备受关注的一项关键技术。
漆酶的固定化是将游离漆酶嫁接到不溶性载体基质上[8-10]。吸附法是指漆酶通过分子间作用力(离子键、氢键和范德华力等)吸附到载体的表面和孔隙内部[11]。吸附法制备条件相对简单,但吸附力相对较弱,易于漆酶脱落渗漏,从而降低固定化酶活性。吸附载体多样易得,如生物炭[6]、金属有机骨架材料[12]或蒙脱石[13]等。包埋法是指将漆酶固定在半透性聚合物膜或多面体结构中。常见的包埋材料包括天然凝胶(如明胶、壳聚糖珠等)以及合成凝胶(如聚丙烯酰胺和海藻酸盐珠等),其中海藻酸盐珠由于其无毒温和的凝胶特性[14]最为常见。包埋法的特殊固定方式是漆酶被包裹在高聚物基质中,因此可以有效地防止漆酶的流失和机械损伤,使得包埋后的酶不易漏出,也不会引起酶结构的变化。提高了固定化酶的稳定性。包埋法形成的固定化酶颗粒较小,底物和产物容易扩散到颗粒内部,有利于酶促反应的进行。但可能会造成漆酶与底物的接触效率低和孔扩散受到限制。
碳基材料因其物理强度高和热稳定性优良等特点,被视为一种有前途的固定化载体。生物炭是通过限氧裂解生物质废弃物而来的一类富碳颗粒,被视为廉价的、且环境友好的炭质材料[15]。由于生物质的可再生性,大量低廉的生物质废弃物可为生物炭的规模化生产提供原料。LIU 等[16]针对生物炭的经济性进行了分析,指出水稻秸秆炭和甘蔗渣炭的价格分别为0.79美元·kg−1和0.93 美元·kg−1。据国际生物炭协会(International Biochar Initiative, IBI)调查,全球生物炭价格在0.08~13.48美元·kg−1[17]。碳纳米管(CNT)是同轴圆管状的石墨烯材料,具有超轻重量、高机械强度以及化学稳定性等独特的性质。它因能应用在高性能材料和电化学传感器等领域而备受关注[19]。只是CNT生产成本高,其价格从5美元·g−1到75美元·g−1不等[18],这限制了CNT的技术应用。生物炭和CNT均具有较强的机械强度、可观的比表面积、以及易于功能化等优点,可作为固定化漆酶的碳基载体[20-22]。ZHANG 等[21]利用CNT固定化漆酶去除刚果红,研究发现漆酶-碳纳米管可在前30 min内快速吸附和降解刚果红。在漆酶-碳纳米管体系下,75%刚果红被去除时所需时间仅仅是CNT体系下的50%。
雌二醇(E2)属于典型的环境激素、广泛分布在水体环境中。它能通过干扰或破坏生物体内原生激素的合成、转运、分解等过程,使生物体无法正常代谢。据报道,E2在0.1ng·L−1 的质量浓度水平内就能表现出生物学效应[23]。E2在食物链中的积累可能会导致对人和动物的生长问题、生殖健康问题、低出生率及高肿瘤率等不良影响[23-24]。因此,利用固定化漆酶高效处理水体中E2的研究具有重要实际应用意义。本研究旨在比较性研究生物炭和CNT固定化漆酶的性能及去除水体E2的效果及机制,本研究选用木炭(WB)、竹炭(BB)和CNT作为碳基载体,通过吸附法和包埋法固定游离漆酶,对比游离漆酶和固定化漆酶的活性、稳定性、和可重复使用性;研究WB、BB和CNT固定化漆酶去除E2的效果,以及循环利用率;同时,探究金属离子浓度效应对于吸附法和包埋法固定化漆酶去除水体E2的影响。
-
实验选取来源于杂色栓菌(Trametes versicolor)的真菌漆酶(Laccase, 500 U·g−1)、E2(17β-estradiol, >98%)、一水柠檬酸、二水柠檬酸钠、2,2'-叠氮基-双(3-乙基苯并噻唑啉-6-磺酸)(ABTS)、WB(粒径<300目)、BB(粒径<300目)、CNT等购置于阿拉丁试剂(上海)有限公司。
-
通过吸附法固定漆酶,以柠檬酸-柠檬酸钠为缓冲对作为背景液,配制50 mg·L−1漆酶溶液,分别将100 mL漆酶溶液与100 mg WB、BB、CNT进行充分混合,25 °C下于摇床中振荡12 h。待吸附固定后,进行固液分离,通过0.22 μm滤膜得到的三种固定化漆酶材料,放置于4 °C冰箱中待用。利用吸附法固载漆酶于WB上,简写为AWB-L(Adsorption Wood Biochar-Laccase)。其他依次简写为ABB-L和ACNT-L。
通过包埋法固定漆酶,将100 mL的3%氯化钙溶液与100 mg的WB、BB、CNT进行充分混合,超声30 min后,在25 °C保存24 h,使3种炭质材料与Ca2+充分进行接触。待炭质材料表面充分吸附Ca2+后,进行固液分离,通过0.22 μm滤膜得到3种炭质材料,在60 °C下烘干。其次将100 mL漆酶溶液(50 mg·L−1)与100 mg富Ca2+离子的3种炭质材料充分混合。在摇床中振荡8 h后,取20 mL质量分数0.5%的海藻酸钠溶液缓慢滴入漆酶-炭质材料的混合体系,置于摇床中继续振荡4 h。最后,当转化的海藻酸钙包埋住游离漆酶固载于3种炭质材料上,进行固液分离,通过0.22 μm滤膜获得3种包埋法固定化漆酶材料。放置于4 °C冰箱中待用。利用包埋法固载漆酶于WB简写为EWB-L(Embedding Wood Biochar-Laccase),其他依次简写为EBB-L和ECNT-L。
-
使用扫描电子显微镜(SEM, S-4800, Hitachi, Japan)表征固定化前后WB、BB、CNT的微观尺度形貌结构。通过傅里叶红外光谱(FTIR, Varian 640-IR, USA)在400~4000 cm−1内分析固定化前后WB、BB、CNT的官能团。
-
ABTS向ABTS+自由基的转化用于测定漆酶的活性。一个游离酶活性单位定义为每分钟催化 1 μmol ABTS 所需的游离酶量。具体而言,取0.3 mL 1 mmol·L−1 ABTS与2.7 mL漆酶溶液充分混合,使用紫外-可见分光光度计(Ultraviolet spectrophotometer, UV-Vis)于420 nm 处测量其吸光度的增加量,2 min内的吸光度变化,每隔15 s记录1次。根据测定的吸光度,计算漆酶的酶活,计算公式如式(1)所示。
其中:K代表酶活,U·g−1;∆A为ABTS+在一段时间内的吸光度变化值;Vt为反应体系的总体积,L;ε为表ABTS+的摩尔消光系数,36 000 L·(mol·cm)−1;∆T 为反应时间,min;m 为酶的质量,g。
-
在25 °C下,将50 mg·L−1游离漆酶和40 mg固定化漆酶分别放入40 mL柠檬酸-柠檬酸钠溶液(pH=5)中,并分别在24、48、72、96、120 h时,测定其剩余活性。研究了固定化漆酶在25 °C下长达25 d的储存稳定性,并以120 h为间隔测定剩余活性。通过ABTS作为底物,研究了固定化漆酶的重复使用性,进行了5个重复循环。
-
在pH=5条件下,将40 mg WB、BB、CNT以及固定化材料加入至40 mL的E2(50 mg·L−1)溶液中,利用0.22 μm过滤器分别在20、40、60、90、120、240、480 min从反应体系中取出0.5 mL液体置于2 mL玻璃小瓶,并加入0.5 mL甲醇溶液淬灭漆酶反应活性。所有样品均一式三份,利用高效液相色谱仪(HPLC, 安捷伦1260),定量液相剩余E2的质量浓度。反应480 min后,进行固液分离,重新加入40 mL E2(50 mg·L−1)溶液。该步骤循环重复5次,每次所取出的液体经过0.22 μm的过滤器制样、保存。所有样品均一式三份,利用HPLC定定液相剩余E2的质量浓度。
-
以柠檬酸-柠檬酸钠缓冲背景液(pH=5),分别配制0.5、1.0、5.0 mmol·L−1的硝酸钾(KNO3)和一水硝酸锰(MnNO3()2·H2O)。在K+和Mn2+离子存在条件下,分别利用40 mg吸附和包埋法固定化漆酶降解 40 mL质量浓度为 50 mg·L−1 E2溶液。分别在20、40、60、90、120、240、480 min进行取样。所有样品均一式三份,利用HPLC测定液相剩余E2的质量浓度。
-
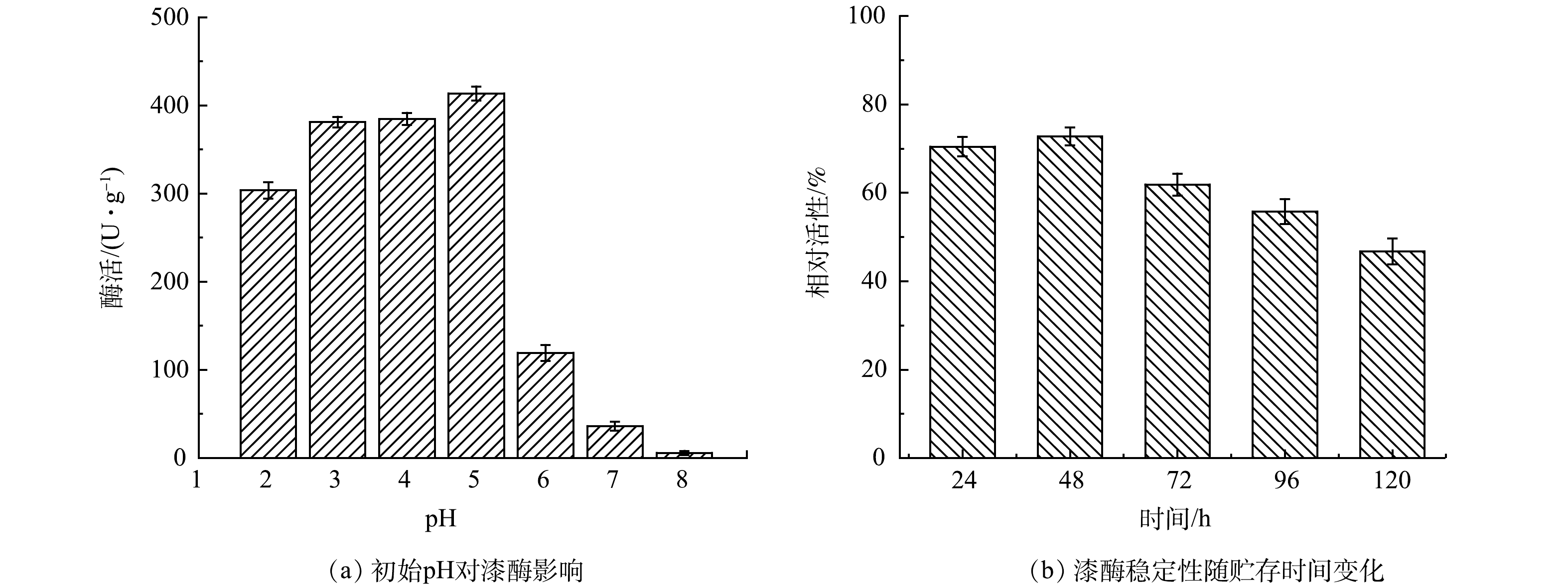
由于游离漆酶的活性受pH影响极大,因此测定了不同pH条件下的漆酶活性。如图1(a)所示,在pH=2~8的条件下,游离漆酶的活性分别为303.75、381.05、384.65、413.58、119.31、36.24、5.80 U·g−1。pH的变化可以决定漆酶中氨基酸的电离状态,从而影响其结构和活性[4]。游离漆酶的活性随着pH的提高,逐渐增加。在pH=5时游离漆酶活性最佳。随着pH继续升高,漆酶的活性出现急剧下降现象。当pH=7时,游离漆酶的活性降低至36.24 U·g−1,仅为最高酶活的8.76%。在碱性水体环境中漆酶完全丧失了其活性。这可能是由于氢氧根阴离子与漆酶活性位点的 T2/T3 铜结合而引起的抑制,从而中断了从 T1 到 T2/T3 铜位点的内部电子转移[25-26]。漆酶的 T1/T2 和T3活性位点协同作用,通过传递电子来促进漆酶催化氧化反应的进行。这些活性位点在固定化漆酶结构中保持了其原有的生物活性,使得固定化的漆酶可以有效地催化氧化反应。此外,在pH =5时游离漆酶储存的稳定性。结果表明:24、48、72、96、120 h时,游离漆酶剩余的相对活性分别为70.40%、72.78%、61.92%、55.85%、46.78%(图1(b))。可以发现,随着时间的增加,游离漆酶的活性逐渐下降。这可能是因为在长时间静置的游离漆酶中,酶活性位点的构象变化导致酶活性降低[27-28]。游离漆酶作为一种水溶性蛋白,难以在有机废水处理过程中进行回收,造成浪费。而且,漆酶的稳定性弱和成本高限制了其在环境修复领域的应用。因此,研究适当的固定化方法将游离漆酶固载,提高漆酶的循环利用率以及固定化漆酶的功能效应非常必要。
-
通过吸附和包埋方式将漆酶固定在WB、BB和CNT上,利用扫描电镜观察固定前后的微观形态结构。如图2(a)~(c)所示,WB、BB结构表面存有排列有序的孔状结构,这是由于木质纤维素在炭化过程中炭相的转化所致。而CNT有着细长的管状结构并容易团聚成不规则的球体。图2(d)~(i)是固化漆酶后的扫描电镜图,在图中没有观察到表面形貌的显着变化。这可能是由于漆酶蛋白(60~90 kDa)的小尺寸相当于小于 5 nm 的粒径。这个尺寸很难被放大 10 μm 的显微照片捕捉到[21,29]。 然而,在酶固定化后,AWB-L、EWB-L等表面似乎更光滑,这可能是由于WB、BB、和CNT表面有酶涂层所致[22]。有研究表明,利用磁性生物炭固定漆酶后,生物炭的表面因有酶涂层变得更为光滑[30]。
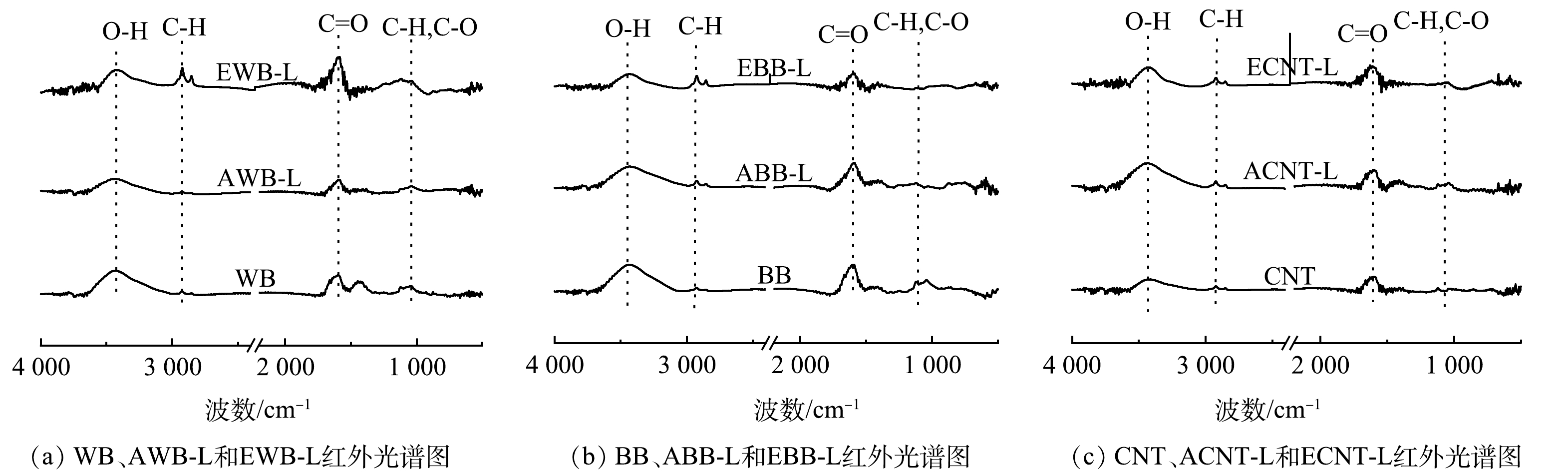
本研究利用FTIR分析了漆酶固定化前后WB、BB和CNT的结构变化。如图3所示,在3 420~3 450 cm−1处观察到的峰为—OH 伸缩振动[29]。2 924 cm−1处的峰归因于烷基引起的不对称 C—H 和对称 C—H 振动[31]。1 626~1 641 cm−1处的吸收峰可能与生物炭中羧基的C=O键和漆酶蛋白中存在的酰胺键的伸缩振动有关[32]。1 148 cm−1处的峰对应于二级酰胺结构的C—O—C伸缩振动[33]。1 050 cm−1和1 071 cm−1处的峰代表生物炭中芳环的 C—H 键[34]。而 1 026 cm−1处则代表着 C—O 基团的伸缩振动[22,34]。与WB和BB相比,CNT固载漆酶后的以上官能团的振动峰均有所增强,这是由于漆酶负载后增加了官能团的在CNT上的量。例如, WB和BB负载漆酶后,—OH峰强有所降低;而CNT负载漆酶后—OH峰则增强,CNT固载漆酶的峰强增加。包埋法负载在WB上的C=O和C—H官能团有明显增加。另外,780 cm−1附近的峰变多,进一步证明漆酶成功固定在WB和BB和CNT上[35]。
-
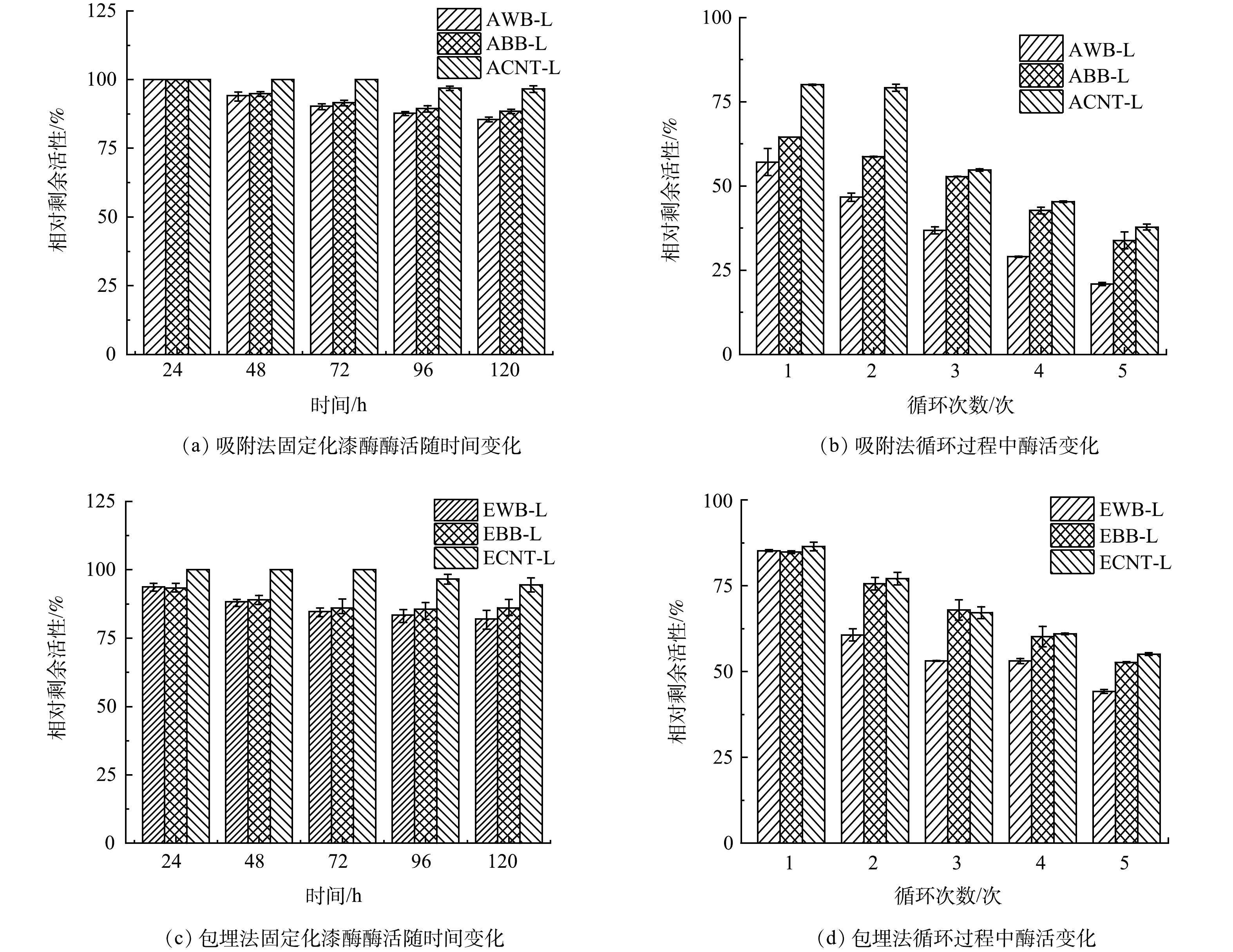
漆酶的稳定性是决定生物催化剂稳健性的重要因素,可通过探究固漆酶固定化后酶活性的时间变化,探究不同固定方式的漆酶的稳定性。本研究在25 °C下储存120 h来评估固定化漆酶的稳定性,每24 h测定其相对剩余活性。吸附法固定化漆酶的稳定性如图4(a)所示。可见,120 h后AWB-L和ABB-L的活性仍分别保留了85.82%和88.51%剩余活性,而ACNT-L更加表现出其优越的固载性能,可保留96.60%固载的漆酶。此前研究报道固定在磁性纳米颗粒上的漆酶能保存71.2%的活性[36],而固定在氨基功能化纳米颗粒上的漆酶仅表现出64.7%的活性[37]。经过包埋法固定化后(图4(c)),EWB-L、EBB-L和ECNT-L的相对剩余活性在120 h后分别为82.02%、85.07%和94.54%。这表现出在WB、BB和CNT上包埋法极大提高了游离漆酶的稳定性,防止了漆酶在水相中流失。碳基材料固定化漆酶的优越性可能关乎其刚性多孔结构,能起到高效贮存漆酶作用。
另一方面,漆酶固定后,它的重复使用性也是决定生物催化系统在工业规模上的潜在应用的重要参数。本研究以ABTS作为底物,在5次循环过程中检查固定化漆酶的可重复使用性。研究结果表明,吸附法固定化漆酶经历 5次循环后(图4(b)),AWB-L和ABB-L的剩余酶活 仅剩初始酶活的27.81%和26.62%;而ACNT-L也仅存37.99%的剩余活性。这可能是由于吸附负载过程漆酶与载体活性位点之间的结合力不强。经过多次反应和水洗后,大量漆酶从固定载体表面脱落,导致相对酶活性下降[38]。相比于吸附法,包埋法的损失率要小于吸附法的损失率。因为包埋法固定化漆酶主要利用了聚合物和载体共同包裹住漆酶,而不是利用吸附的弱作用力固定化漆酶[39],此结果与其他研究研究结果类似。WANG 等[6]利用十六烷基三甲基溴化铵-氢氧化钾(CTAB-KOH)改性生物炭,并通过吸附法固定漆酶,他们发现固定化漆酶在6次循环后失去了约 55% 的活性。而另一项研究中,将漆酶吸附固定在稻草生物炭上,其固定化率达到66%,而且固定化酶在经过6次循环的稳定性操作,能够保留40%的初始活性[40]。ZHANG 等[22]通过吸附、沉淀和交联将漆酶稳定地固定在纳米磁性生物炭(L-MBC)上,固定量达到2.25 U·mg−1,经过30 d储存,L-MBC活性还保持在64.40%。由此可知,吸附法虽然操作方法易行,但其固定化漆酶的稳定性和可重复使用性相对较弱。包埋法固定化漆酶不仅更有利于酶的稳定性,而且提高了固定化漆酶的重复利用率,从而有效降低漆酶在污水处理中的应用成本。
-
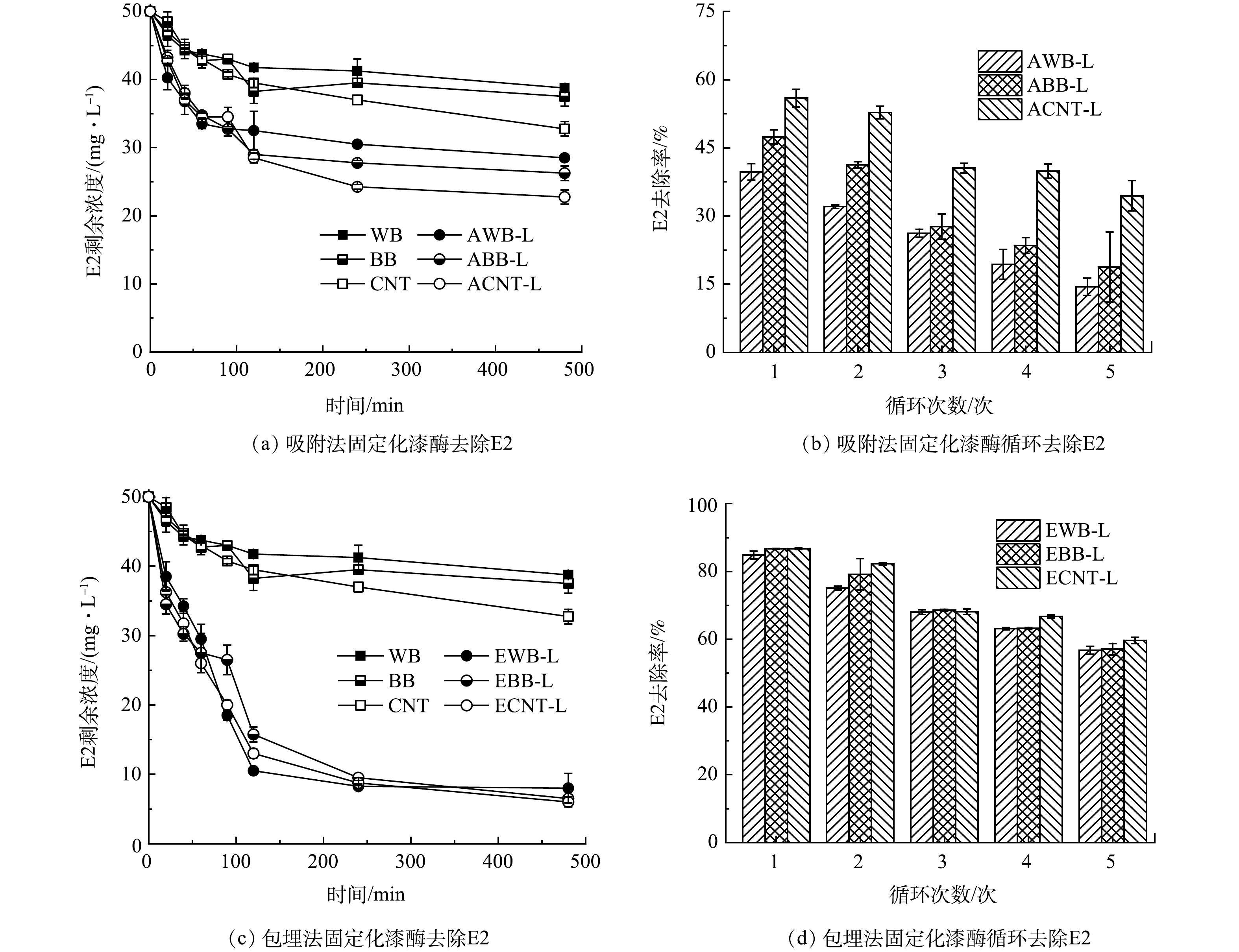
通过吸附法和包埋法使漆酶固定在WB、BB和CNT上,从而研究固定化漆酶对E2的去除。经过8 h反应,3种碳基材料对E2的吸附量遵循CNT>BB>WB,其吸附量分别达到17.23、13.01和11.32 mg·L−1。这可能是由于CNT的比表面积大所致[41]。如图5(a)所示,AWB-L的E2去除量增加到21.46 mg·L−1;ABB-L的E2去除量增加到23.83 mg·L−1。ACNT-L对E2去除最高,在8 h内对于E2去除量为27.38 mg·L−1。另外,包埋法固定化漆酶对于E2的去除效果如图5c。在8 h内,EWB-L对E2去除量增加到42.04 mg·L−1;EBB-L对E2去除量增加到43.60 mg·L−1;ECNT-L对于E2去除量达到43.93 mg·L−1。固定化漆酶对水中E2的去除效果更好,是因为固定化漆酶不仅可以吸附水体E2,而且可以通过漆酶的催化氧化降解E2[42]。另外,有研究表明,包埋法固定化漆酶去除E2的效果显著高于吸附法,可能由于漆酶吸附于载体的作用力较弱,循环利用过程中漆酶也易于再次脱落,漆酶的负载率会不断降低。对于包埋法而言,由于酶蛋白分子相对较大,漆酶易于被限制在包埋空间内,且漆酶的分子结构也不会发生改变[43-44]。而分子质量较小的污染物则可以畅通进入漆酶空间内, 当污染物分子接近该空间时, 被固定化的漆酶将参与污染物的催化氧化过程[14]。SHAO等[45]通过空心介孔碳纳米球(HMCs)固定了游离的漆酶, 发现漆酶的固定化效果极为稳定, HMCs材料上漆酶的最大载量达到835 mg·g−1。固定化漆酶对盐酸四环素和盐酸环丙沙星的去除率分别为99.40%和96.90%。
对比5个连续批次(每批次8 h)循环对E2(50 mg·L−1)的去除量的变化。如图5(b)所示, 经过5次循环后,吸附法制备的3种固定化漆酶对E2的去除率逐渐降低。AWB-L对E2的去除率由39.66%降低至15.38%;对于ABB-L,5次循环后E2的去除率也由47.44%降至19.76%;5次循环后ACNT-L对E2的去除率由54.50%降低至34.84%。这是因为固定在载体上的漆酶发生脱落,或漆酶结构发生变化导致酶活性下降,进而影响了E2的去除效率[46]。包埋法固定化漆酶去除E2的循环实验结果如图5(d)所示,对于EWB-L,5次循环后E2的去除率由88.84%降低至56.06%;EBB-L对E2的去除率由86.66%降低至57.08%;对于ECNT-L,5次循环后E2的去除率由86.76%降低至59.66%。经过多次循环后,利用包埋法固定化漆酶的去除能力也会随着循环次数的增加而逐渐减弱,因为经过多次使用,导致包埋结构遭到破坏,从而导漆酶脱落所致[47]。在5次循环后,利用包埋法固定化漆酶去除E2效果高于吸附法,可能归因于藻酸盐基质提供的保护性微环境[48]。相对于吸附法,包埋法固定漆酶对E2的效果更好,循环使用的去除率也较高。其中,吸附法WB和BB固定漆酶对E2的去除率要低于CNT固定漆酶的去除率。然而,包埋法CNT与生物炭固载漆酶对E2的去除率和循环效率都很相似,因此,包埋法生物炭固载漆酶可以代替高成本的CNT固载漆酶,也能达到相同的去除E2的效果。
-
漆酶的活性通常会受到废水或者其他环境中存在的金属离子的影响,随金属离子和酶的不同而变化。例如,Mn2+可刺激肉孢子丝菌中的漆酶但抑制来自Leptographium qinlingensis的漆酶[49,50]。所以为了进一步了解固定化漆酶的实际应用效果,考察2种金属离子(K+和Mn2+)对固定化漆酶去除E2的影响。
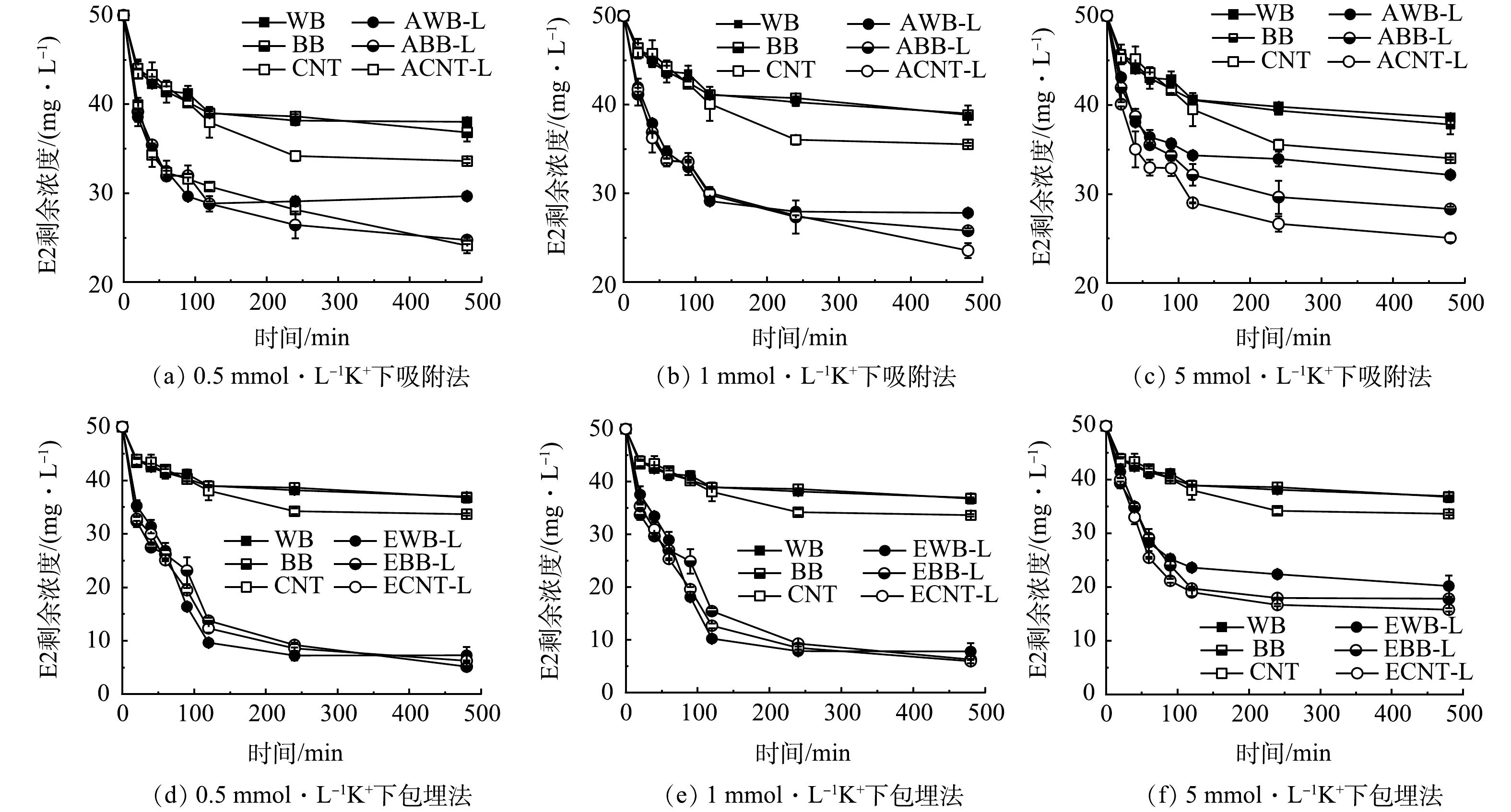
1) K+离子的影响。图6描述在0.5、1和5 mmol·L−1 K+浓度下,漆酶固定化前后炭质材料去除E2随时间变化的关系曲线。研究发现在前100 min内E2的质量浓度迅速下降,随后保持一定平衡。随着K+浓度由0.5 mmol·L−1增加到1 mmol·L−1时,固定化漆酶对于E2的去除无太大的变化现象。但是当K+浓度达到5 mmol·L−1时,E2的去除率明显降低。金属离子的抑制作用主要是通过干扰漆酶催化反应过程中电子传递以及可能影响漆酶的活性,从而导致固定化漆酶对E2的去除量降低。同样冯义平等[51]发现Na+、K+、Cd2+、Hg2+、Fe2+、Fe3+ 在10.0 mmol·L−1浓度水平下显著抑制漆酶活性。这些金属离子能够与漆酶结构中游离的半胱氨酸结合,形成失活的蛋白加合物,并因此导致漆酶失活。从而影响漆酶催化去除溴代阻燃剂四溴双酚 A。另外发现在K+离子影响下,包埋法固定化漆酶去除E2受到抑制的效果低于吸附法。一方面可能由于漆酶对载体的吸附亲和力差,导致容易脱落[52];另一方面可能由于藻酸盐包埋保护漆酶一定程度上免受溶液中金属离子的影响[53]。
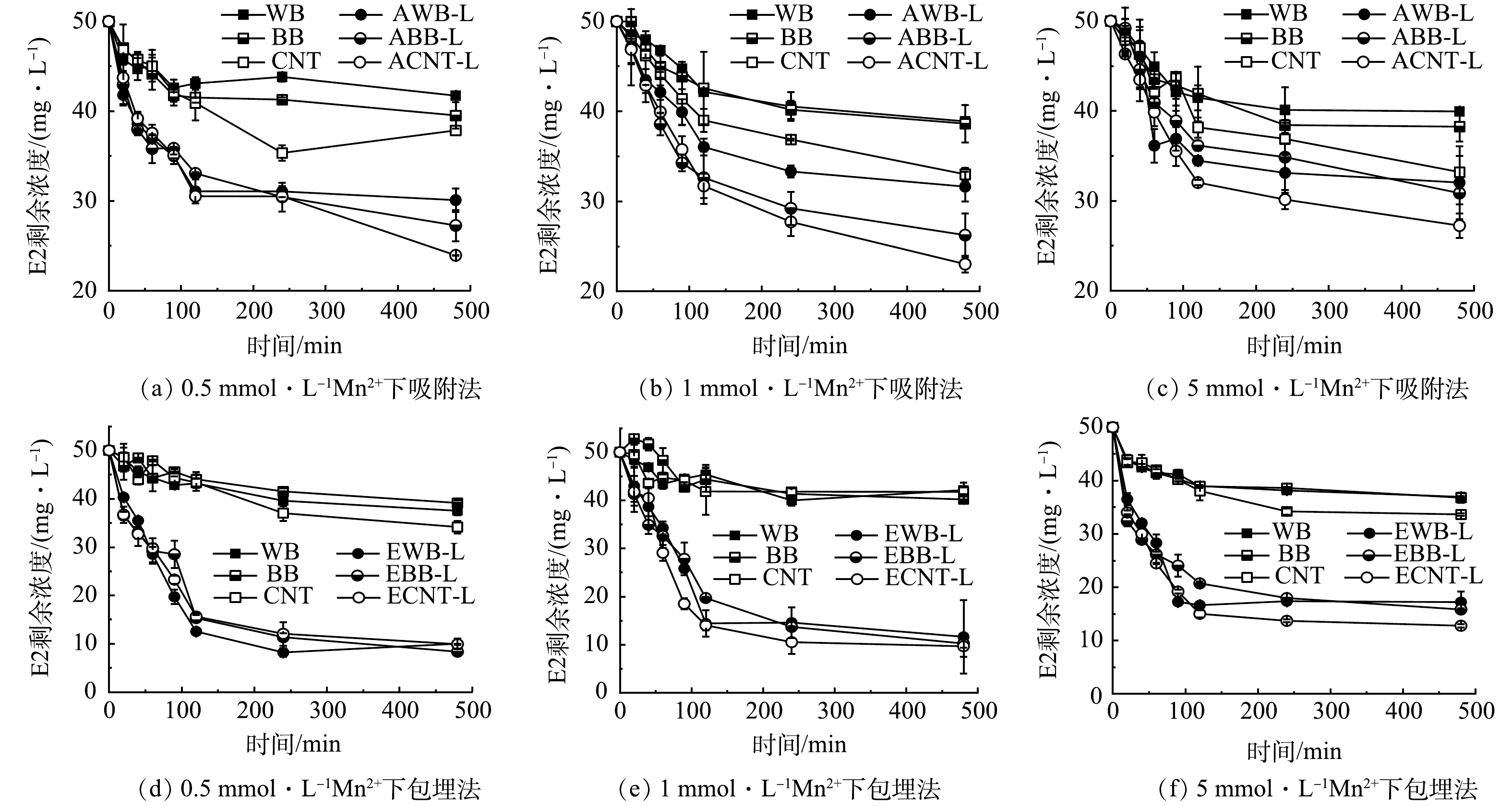
2) Mn2+的影响。将Mn2+与固定化后的漆酶在E2溶液中共同反应8 h后(图7)。当Mn2+浓度由0.5 mmol·L−1增加到1 mmol·L−1时,对于E2的去除几乎没有影响。使用吸附法和包埋法固定化漆酶后,E2的剩余质量浓度分别为28 mg·L−1和10 mg·L−1。然而当Mn2+浓度达到5 mmol·L−1时,对E2的去除出现抑制作用。这可能是由于水溶液中的漆酶带负电荷,与金属阳离子之间由于静电引力而吸附在一起,而且金属阳离子价态越高,相互之间静电力作用越强,从而导致漆酶的活性降低[54]。WAGNER 等[55]研究在pH=5.0、Mn2+浓度高达1.0 mmol·L−1的情况下,对苯酚的去除有明显抑制效果。有研究[56]表明,包括Mn(II)在内的某些金属离子与含氧配体相互作用,例如存在于酶上的羧基。这些相互作用可能会改变酶对底物的亲和力。
-
通过吸附法和包埋法制备WB、BB和CNT的固定化漆酶,系统地探究了固定化漆酶的活性和稳定性,固定化漆酶去除E2效果以及金属离子对去除效果的影响,为固定化漆酶技术在绿色化学应用研究提供了新的视角。得出如下结论。
1)对比WB、BB、CNT 3种炭质载体吸附法固定漆酶,发现CNT固定漆酶的稳定性、可重复使用性以及对E2的去除效果都高于WB和BB,这可能是因为CNT具有丰富的纳米孔隙结构所致。
2)包埋法固定的漆酶的稳定性、可重复使用性和E2的去除效果均高于吸附法固定化漆酶。WB、BB、CNT 3种炭质载体包埋法固定漆酶的稳定性、可重复使用性、及对E2去除效率差别不大。因此,生物炭可以作为替代CNT的炭质载体通过包埋法固定游离漆酶,减少固定化成本。
3)固定化漆酶的活性和去除E2的效率受金属离子种类的影响,K+和Mn2+离子的抑制固定化漆酶的活性和E2的去除效率。
生物炭和碳纳米管固定化漆酶去除水体雌二醇
Removal of β-estradiol in wastewater using laccase immobilized by biochar and carbon nano tube
-
摘要: 漆酶是一类具有高效的催化氧化能力的含铜多酚的氧化酶,而固定化漆酶技术在有机废水处理领域受到了越来越多的关注。通过比较吸附法和包埋法利用木炭(WB)、竹炭(BB)和碳纳米管(CNT)固定游离漆酶去除水体雌二醇(E2)。在25 °C 、pH=5条件下,固定化漆酶经120 h 贮存仍保留80%的活性。经过5次循环研究,固载的漆酶仍保留了27%~58%的剩余活性。结合扫描电子显微镜和傅里叶变换红外光谱,证实了漆酶成功地负载在碳基材料上。仅在 8 h内,50 mg·L−1 E2通过吸附法制备的WB、BB、CNT固定化漆酶去除了42.92%、47.66%、43.92%,而包埋法制备的WB、BB、CNT固定化漆酶分别去除84.08%、87.20%、87.86%。结果表明,包埋法固定化漆酶对E2的去除效率更优,这是由于包埋固载在生物炭和CNT的漆酶更为稳定。此外,K+和Mn2+离子可能通过干扰漆酶的电子传递过程影响漆酶的活性,从而抑制E2的去除。本研究旨在为固定化漆酶在有机废水处理的实际应用提供指导。Abstract: Laccase is a class of Cu-containing polyphenol oxidase with high catalytic oxidation ability. The immobilized laccase technique has attracted an increasing attention in organic wastewater treatment. In this study, wood- and bamboo-derived biochars (WB and BB) or carbon nano tube (CNT) were used to immobilize laccase by the adsorption and embedding methods for the removal of β-estradiol (E2) in aqueous environment. At 25 °C and pH=5, 80% activity of the immobilized laccase on WB, BB, and CNT was preserved after 120 h storage. After 5 cycles, the residual activity of the immobilized laccase was 27%~58%. Combined with scanning electron microscopy and Fourier transform infrared spectroscopy, it was confirmed that laccase was successfully loaded on carbon-based materials. Within only 8 h, 42.92%, 47.66%, and 43.92% of 50 mg·L−1 E2 were removed by WB-, BB-, and CNT-immobilized laccases using the adsorption method, while 84.08%, 87.2%, and 87.86% of 50 mg·L−1 E2 were removed by WB-, BB-, and CNT-immobilized laccases using the embedding method. The results showed that the immobilized laccase using the embedding method had a better removal efficiency for E2 due to its stronger stability onto biochars and CNT. In addition, K+ and Mn2+ ions could interfere with electron transfer of laccases, then affect the activity of laccases, diminish E2 removal. The aim of this work can provide a guidance for designing immobilized laccase for organic wastewater treatment.
-
Key words:
- biochars /
- CNT /
- immobilized laccase /
- β-estradiol /
- metal ions
-

-
-
[1] LIU J, SUN K, ZHU R, et al. Biotransformation of bisphenol A in vivo and in vitro by laccase-producing Trametes hirsuta La-7: Kinetics, products, and mechanisms[J]. Environmental Pollution, 2023, 321: 121155-121166. doi: 10.1016/j.envpol.2023.121155 [2] GUPTA V, BALDA S, GUPTA N, et al. Functional substitution of domain 3 (T1 copper center) of a novel laccase with Cu ions[J]. International journal of biological macromolecules, 2019, 123: 1052-1061. doi: 10.1016/j.ijbiomac.2018.11.174 [3] DATTA S, VEENA R, SAMUEL M S, et al. Immobilization of laccases and applications for the detection and remediation of pollutants: a review[J]. Environmental Chemistry Letters, 2021, 19(1): 521-538. doi: 10.1007/s10311-020-01081-y [4] WANG Z, REN D, YU H, et al. Preparation optimization and stability comparison study of alkali-modified biochar immobilized laccase under multi-immobilization methods[J]. Biochemical Engineering Journal, 2022, 181: 108401-108412. doi: 10.1016/j.bej.2022.108401 [5] BRUGNARI T, PEREIRA M G, BUBNA G A, et al. A highly reusable MANAE-agarose-immobilized Pleurotus ostreatus laccase for degradation of bisphenol A[J]. Science of the Total Environment, 2018, 634: 1346-1351. doi: 10.1016/j.scitotenv.2018.04.051 [6] WANG Z, REN D, JIANG S, et al. The study of laccase immobilization optimization and stability improvement on CTAB-KOH modified biochar[J]. BMC Biotechnology, 2021, 21: 1-13. doi: 10.1186/s12896-020-00660-9 [7] PRIMOŽIČ M, KRAVANJA G, KNEZ Ž, et al. Immobilized laccase in the form of (magnetic) cross-linked enzyme aggregates for sustainable diclofenac (bio) degradation[J]. Journal of Cleaner Production, 2020, 275: 124121-124137. doi: 10.1016/j.jclepro.2020.124121 [8] REN D, WANG Z, JIANG S, et al. Recent environmental applications of and development prospects for immobilized laccase: A review[J]. Biotechnology and Genetic Engineering Reviews, 2020, 36(2): 81-131. doi: 10.1080/02648725.2020.1864187 [9] KOŁODZIEJCZAK-RADZIMSKA A, ZEMBRZUSKA J, SIWIŃSKA-CIESIELCZYK K, et al. Catalytic and physicochemical evaluation of a TiO2/ZnO/laccase biocatalytic system: Application in the decolorization of Azo and Anthraquinone dyes[J]. Materials, 2021, 14(20): 6030-6047. doi: 10.3390/ma14206030 [10] KOŁODZIEJCZAK-RADZIMSKA A, BUDNA A, CIESIELCZYK F, et al. Laccase from Trametes versicolor supported onto mesoporous Al2O3: Stability tests and evaluations of catalytic activity[J]. Process Biochemistry, 2020, 95: 71-80. doi: 10.1016/j.procbio.2020.05.008 [11] NEEDHIDASAN S, RAMALINGAM C. Stratagems employed for 2, 4-dichlorophenoxyacetic acid removal from polluted water sources[J]. Clean Technologies and Environmental Policy, 2017, 19: 1607-1620. doi: 10.1007/s10098-017-1371-8 [12] HAN Z, FAN X, YU S, et al. Metal-organic frameworks (MOFs): A novel platform for laccase immobilization and application[J]. Journal of Environmental Chemical Engineering, 2022: 108795-108821. [13] LI G, NANDGAONKAR A G, LU K, et al. Laccase immobilized on PAN/O-MMT composite nanofibers support for substrate bioremediation: a de novo adsorption and biocatalytic synergy[J]. RSC advances, 2016, 6(47): 41420-41427. doi: 10.1039/C6RA00220J [14] LE T T, MURUGESAN K, LEE C-S, et al. Degradation of synthetic pollutants in real wastewater using laccase encapsulated in core–shell magnetic copper alginate beads[J]. Bioresource Technology, 2016, 216: 203-210. doi: 10.1016/j.biortech.2016.05.077 [15] CHU G, ZHAO J, HUANG Y, et al. Phosphoric acid pretreatment enhances the specific surface areas of biochars by generation of micropores[J]. Environmental Pollution, 2018, 240: 1-9. doi: 10.1016/j.envpol.2018.04.003 [16] LIU Y, YANG X, ZHANG J, et al. Process Simulation of Preparing Biochar by Biomass Pyrolysis Via Aspen Plus and Its Economic Evaluation[J]. Waste and Biomass Valorization, 2022, 13(5): 2609-2622. doi: 10.1007/s12649-021-01671-z [17] CAMPBELL R M, ANDERSON N M, DAUGAARD D E, et al. Financial viability of biofuel and biochar production from forest biomass in the face of market price volatility and uncertainty[J]. Applied Energy, 2018, 230: 330-343. doi: 10.1016/j.apenergy.2018.08.085 [18] MRINAL B. Polymer nanocomposites: A comparison between carbon nanotubes, graphene, and clay as nanofillers[J]. Materials, 2016, 9(4): 262. doi: 10.3390/ma9040262 [19] VITHANAGE M, HERATH I, ALMAROAI Y A, et al. Effects of carbon nanotube and biochar on bioavailability of Pb, Cu and Sb in multi-metal contaminated soil[J]. Environmental geochemistry and health, 2017, 39: 1409-1420. doi: 10.1007/s10653-017-9941-6 [20] XU R, TANG R, ZHOU Q, et al. Enhancement of catalytic activity of immobilized laccase for diclofenac biodegradation by carbon nanotubes[J]. Chemical Engineering Journal, 2015, 262: 88-95. doi: 10.1016/j.cej.2014.09.072 [21] ZHANG W, YANG Q, LUO Q, et al. Laccase-carbon nanotube nanocomposites for enhancing dyes removal[J]. Journal of Cleaner Production, 2020, 242: 118425-118436. doi: 10.1016/j.jclepro.2019.118425 [22] ZHANG Y, PIAO M, HE L, et al. Immobilization of laccase on magnetically separable biochar for highly efficient removal of bisphenol A in water[J]. RSC advances, 2020, 10(8): 4795-4804. doi: 10.1039/C9RA08800H [23] COLEMAN H M, EGGINS B R, BYRNE J A, et al. Photocatalytic degradation of 17-β-oestradiol on immobilized TiO 2[J]. Applied Catalysis B Environmental, 2000, 24(1): 1-5. doi: 10.1016/S0926-3373(99)00091-0 [24] IMRAN, ALI, ZEID, et al. Supra molecular mechanism of the removal of 17-β-oestradiol endocrine disturbing pollutant from water on functionalized iron nano particles[J]. Journal of Molecular Liquids, 2017: 123-129. [25] XU F. Effects of redox potential and hydroxide inhibition on the pH activity profile of fungal laccases[J]. Journal of biological chemistry, 1997, 272(2): 924-928. doi: 10.1074/jbc.272.2.924 [26] HUAN W W, YANG Y X, WU B, et al. Degradation of 2, 4‐DCP by the immobilized laccase on the carrier of Fe3O4@ SiO2‐NH2[J]. Chinese Journal of Chemistry, 2012, 30(12): 2849-2860. doi: 10.1002/cjoc.201200718 [27] HAN Z, WANG H, ZHENG J, et al. Ultrafast synthesis of laccase-copper phosphate hybrid nanoflowers for efficient degradation of tetracycline antibiotics[J]. Environmental Research, 2023, 216: 114690-114701. doi: 10.1016/j.envres.2022.114690 [28] MAURYA S S, NADAR S S, RATHOD V K. Dual activity of laccase-lysine hybrid organic–inorganic nanoflowers for dye decolourization[J]. Environmental Technology & Innovation, 2020, 19: 100798-100811. [29] PANDEY D, DAVEREY A, DUTTA K, et al. Bioremoval of toxic malachite green from water through simultaneous decolorization and degradation using laccase immobilized biochar[J]. Chemosphere, 2022, 297: 134126-134134. doi: 10.1016/j.chemosphere.2022.134126 [30] HE L, YANG Y, KIM J, et al. Multi-layered enzyme coating on highly conductive magnetic biochar nanoparticles for bisphenol A sensing in water[J]. Chemical Engineering Journal, 2020, 384: 123276-123286. doi: 10.1016/j.cej.2019.123276 [31] LIU L, LI Y, FAN S. Preparation of KOH and H3PO4 modified biochar and its application in methylene blue removal from aqueous solution[J]. Processes, 2019, 7(12): 891-911. doi: 10.3390/pr7120891 [32] LEPORE M, PORTACCIO M. Optical detection of different phenolic compounds by means of a novel biosensor based on sol–gel immobilized laccase[J]. Biotechnology and Applied Biochemistry, 2017, 64(6): 782-792. doi: 10.1002/bab.1551 [33] BOKOV D O, MAHMOUD M Z, WIDJAJA G, et al. Transfer hydrogenation of nitroarenes using cellulose filter paper-supported Pd/C by filtration as well as sealed methods[J]. RSC Advances, 2022, 12(18): 10933-10949. doi: 10.1039/D2RA01151D [34] ZHU Y, YI B, YUAN Q, et al. Removal of methylene blue from aqueous solution by cattle manure-derived low temperature biochar[J]. RSC advances, 2018, 8(36): 19917-19929. doi: 10.1039/C8RA03018A [35] ZHENG Z, LIU W, ZHOU Q, et al. Effects of co-modified biochar immobilized laccase on remediation and bacterial community of PAHs-contaminated soil[J]. Journal of Hazardous Materials, 2023, 443: 130372-130383. doi: 10.1016/j.jhazmat.2022.130372 [36] PATEL S K, GUPTA R K, KIM S Y, et al. Rhus vernicifera Laccase Immobilization on Magnetic Nanoparticles to Improve Stability and Its Potential Application in Bisphenol A Degradation[J]. Indian Journal of Microbiology, 2020, 61(1): 45-54. [37] PATEL S K, ANWAR M Z, KUMAR A, et al. Fe2O3 yolk-shell particle-based laccase biosensor for efficient detection of 2, 6-dimethoxyphenol[J]. Biochemical Engineering Journal, 2018, 132: 1-8. doi: 10.1016/j.bej.2017.12.013 [38] WANG Z, REN D, WU J, et al. Study on adsorption-degradation of 2, 4-dichlorophenol by modified biochar immobilized laccase[J]. International Journal of Environmental Science and Technology, 2022, 19: 1393-1406. doi: 10.1007/s13762-021-03151-2 [39] YAOHUA G, PING X, FENG J, et al. Co-immobilization of laccase and ABTS onto novel dual-functionalized cellulose beads for highly improved biodegradation of indole[J]. Journal of hazardous materials, 2018, 365: 118-124. [40] IMAM A, SUMAN S K, SINGH R, et al. Application of laccase immobilized rice straw biochar for anthracene degradation[J]. Environmental Pollution, 2021, 268: 115827-115841. doi: 10.1016/j.envpol.2020.115827 [41] REN X, CHEN C, NAGATSU M, et al. Carbon nanotubes as adsorbents in environmental pollution management: A review[J]. Chemical Engineering Journal, 2011, 170(2-3): 395-410. doi: 10.1016/j.cej.2010.08.045 [42] 任海燕, 纪树兰, 崔成武, 等. 17α-乙炔基雌二醇的降解及其共基质代谢特性[J]. 环境科学研究, 2006, 19(4): 61-64. doi: 10.3321/j.issn:1001-6929.2006.04.012 [43] DARONCH N A, KELBERT M, PEREIRA C S, et al. Elucidating the choice for a precise matrix for laccase immobilization: A review[J]. Chemical Engineering Journal, 2020, 397: 125506-125521. doi: 10.1016/j.cej.2020.125506 [44] ASGHER M, NOREEN S, BILAL M. Enhancement of catalytic, reusability, and long-term stability features of Trametes versicolor IBL-04 laccase immobilized on different polymers[J]. International journal of biological macromolecules, 2017, 95: 54-62. doi: 10.1016/j.ijbiomac.2016.11.012 [45] SHAO B, LIU Z, ZENG G, et al. Immobilization of laccase on hollow mesoporous carbon nanospheres: noteworthy immobilization, excellent stability and efficacious for antibiotic contaminants removal[J]. Journal of hazardous materials, 2019, 362: 318-326. doi: 10.1016/j.jhazmat.2018.08.069 [46] LONAPPAN L, LIU Y, ROUISSI T, et al. Covalent immobilization of laccase on citric acid functionalized micro-biochars derived from different feedstock and removal of diclofenac[J]. Chemical Engineering Journal, 2018, 351: 985-994. doi: 10.1016/j.cej.2018.06.157 [47] LI G, NANDGAONKAR A G, WANG Q, et al. Laccase-immobilized bacterial cellulose/TiO2 functionalized composite membranes: Evaluation for photo-and bio-catalytic dye degradation[J]. Journal of membrane science, 2017, 525: 89-98. doi: 10.1016/j.memsci.2016.10.033 [48] A CHAUDHARI S, R KAR J, S SINGHAL R. Immobilization of proteins in alginate: Functional properties and applications[J]. Current Organic Chemistry, 2015, 19(17): 1732-1754. doi: 10.2174/1385272819666150429232110 [49] OLAJUYIGBE F M, FATOKUN C O. Biochemical characterization of an extremely stable pH-versatile laccase from Sporothrix carnis CPF-05[J]. International Journal of Biological Macromolecules, 2017, 94: 535-543. doi: 10.1016/j.ijbiomac.2016.10.037 [50] JAISWAL N, PANDEY V P, DWIVEDI U N. Purification of a thermostable alkaline laccase from papaya (Carica papaya) using affinity chromatography[J]. International Journal of Biological Macromolecules, 2015, 72: 326-332. doi: 10.1016/j.ijbiomac.2014.08.032 [51] 冯义平, 沈梦瑶, 张伊健, 等. 典型金属离子对漆酶催化降解溴代阻燃剂四溴双酚A的影响研究[J]. 环境科学学报, 2020, 40(6): 2082-2089. [52] YANG B, TANG K, WEI S, et al. Preparation of functionalized mesoporous silica as a novel carrier and immobilization of laccase[J]. Applied Biochemistry and Biotechnology, 2021, 193: 2547-2566. doi: 10.1007/s12010-021-03556-2 [53] YAMAK O, KALKAN N A, AKSOY S, et al. Semi-interpenetrating polymer networks (semi-IPNs) for entrapment of laccase and their use in Acid Orange 52 decolorization[J]. Process Biochemistry, 2009, 44(4): 440-445. doi: 10.1016/j.procbio.2008.12.008 [54] LU J, SHI Y, JI Y, et al. Transformation of triclosan by laccase catalyzed oxidation: The influence of humic acid-metal binding process[J]. Environmental Pollution, 2017, 220: 1418-1423. doi: 10.1016/j.envpol.2016.10.092 [55] WAGNER M, NICELL J A. Impact of dissolved wastewater constituents on peroxidase‐catalyzed treatment of phenol[J]. Journal of Chemical Technology & Biotechnology: International Research in Process, Environmental & Clean Technology, 2002, 77(4): 419-428. [56] BRZYSKA M, CIESZCZYK M, ŁOBARZEWSKI J. The effect of the simultaneous operation of two metal ions on soluble and immobilized peroxidase[J]. Journal of Chemical Technology & Biotechnology: International Research in Process, Environmental and Clean Technology, 1997, 68(1): 101-109. -



 下载:
下载: